Las terapias biológicas han cambiado el manejo y tratamiento de diversos trastornos inmunomediados, incluyendo la psoriasis. Dichas terapias incluyen los inhibidores del factor de necrosis tumoral y los anticuerpos monoclonales que focalizan el eje IL-23/IL-17, conocidos por su papel en la patogenia de la enfermedad1.
Risankizumab es un inhibidor selectivo de IL-23 con eficacia probada y perfil de seguridad favorable2. Sin embargo, su uso en pacientes gravemente inmunocomprometidos es limitado, ya que dichos pacientes son excluidos frecuentemente de los ensayos clínicos.
Reportamos dos casos clínicos de pacientes con psoriasis en placas severa, con inmunosupresión por trasplante de órganos sólidos. En ambos pacientes se inició terapia con risankizumab debido a su eficacia y perfil de seguridad.
El caso clínico #1 es un varón de 49 años con infección por hepatitis B (HepB) crónica no tratada, que desarrolló hepatitis tóxica severa tras tratamiento por tuberculosis pulmonar latente con isoniazid, que finalmente se tradujo en trasplante de hígado. Se inició terapia inmunosupresora con tacrolimus y micofenolato mofetil (MMF) junto con terapia supresora para infección por HepB. El paciente fue derivado a nuestro centro debido a psoriasis severa, con PASI (Psoriasis Area Severity Index) basal de 14. Se inició terapia con risankizumab.
Se logró la eliminación completa de la piel (PASI100) en la 16ª semana sin episodios adversos reportados. Debido a la remisión clínica sostenida, se espaciaron los intervalos entre las diferentes administraciones de risankizumab durante 20 semanas. Actualmente, en la semana 58ª, el paciente sigue en remisión clínica sin haberse reportado episodios adversos ni incremento de la carga viral de HepB.
El caso clínico #2 es un varón de 55 años con psoriasis en placas, diabetes tipo 2, cardiopatía coronaria y enfermedad renal crónica progresiva. En 2014, el paciente fue sometido a trasplante renal por enfermedad renal terminal, e inició terapia inmunosupresora con tacrolimus, MMF y prednisona. Transcurrido un año del trasplante se produjo un brote de psoriasis notable, con PASI basal de 14, derivándose finalmente al paciente a nuestro centro. Se intentó un curso de ciclosporina, pero, al no observarse mejora clínica significativa, se inició terapia de risankizumab.
En la semana 16ª, se logró PASI100 sin reacciones adversas registradas, ni alteración de la función renal. Actualmente, en la semana 42ª, y debido a la remisión clínica sostenida, el paciente sigue con terapia de risankizumab cada 20 semanas, siendo supervisado de manera rutinaria.
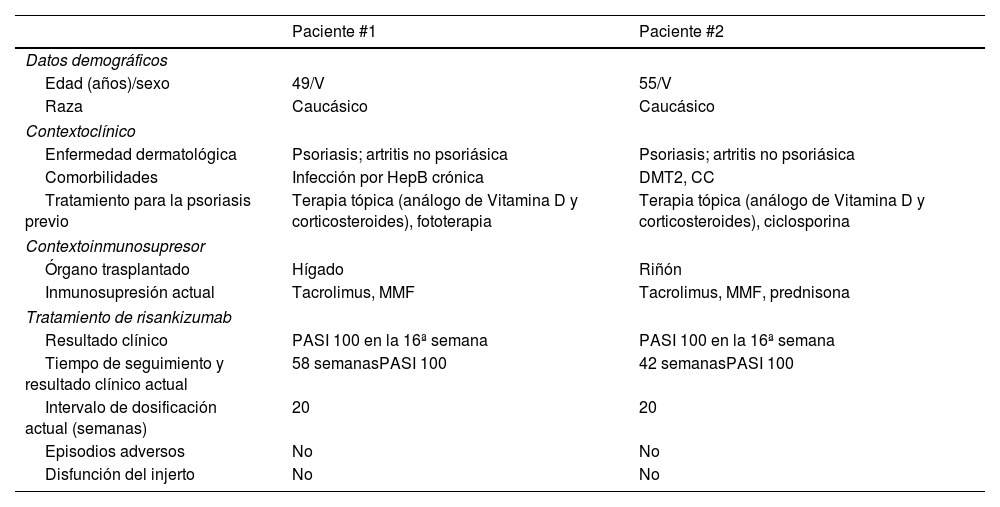
Se muestran datos clínicos adicionales en la tabla 1.
Características clínicas de los receptores de trasplantes de órganos sólidos con psoriasis en placas severa que reciben risankizumab
| Paciente #1 | Paciente #2 | |
|---|---|---|
| Datos demográficos | ||
| Edad (años)/sexo | 49/V | 55/V |
| Raza | Caucásico | Caucásico |
| Contextoclínico | ||
| Enfermedad dermatológica | Psoriasis; artritis no psoriásica | Psoriasis; artritis no psoriásica |
| Comorbilidades | Infección por HepB crónica | DMT2, CC |
| Tratamiento para la psoriasis previo | Terapia tópica (análogo de Vitamina D y corticosteroides), fototerapia | Terapia tópica (análogo de Vitamina D y corticosteroides), ciclosporina |
| Contextoinmunosupresor | ||
| Órgano trasplantado | Hígado | Riñón |
| Inmunosupresión actual | Tacrolimus, MMF | Tacrolimus, MMF, prednisona |
| Tratamiento de risankizumab | ||
| Resultado clínico | PASI 100 en la 16ª semana | PASI 100 en la 16ª semana |
| Tiempo de seguimiento y resultado clínico actual | 58 semanasPASI 100 | 42 semanasPASI 100 |
| Intervalo de dosificación actual (semanas) | 20 | 20 |
| Episodios adversos | No | No |
| Disfunción del injerto | No | No |
CC: cardiopatía coronaria; HepB: hepatitis B; V: varón; MMF: micofenolato mofetil; PASI: Psoriasis Area and Severity Index; DMT2: diabetes mellitus tipo 2.
IL-23 juega un papel esencial en el sostenimiento de la inflamación crónica a través de la activación y diferenciación de las células Th17, lo cual, produce a su vez citocinas proinflamatorias tales como IL-17. Risankizumab focaliza selectivamente IL-23, uniéndose a la subunidad p19, interrumpiendo así el proceso inflamatorio3.
El potencial inmunosupresor de las terapias biológicas ha suscitado grandes preocupaciones sobre seguridad, limitándose su uso en los casos de riesgo incrementado de infección y malignidad, como en los pacientes inmunocomprometidos por trasplante de órganos sólidos. Sin embargo, la evidencia ha confirmado el perfil de seguridad favorable de los agentes biológicos que focalizan selectivamente IL-23. Esto se atribuye probablemente a la función reguladora y no supresora de IL-231.
De hecho, risankizumab no ha mostrado un riesgo incrementado de desarrollo de infección oportunista grave. Por ejemplo, risankizumab parece ser seguro en pacientes con tuberculosis latente (TB), no existiendo evidencia sugestiva de riesgo incrementado de reactivación de la enfermedad, aun en pacientes que inician profilaxis de TB4. Además, un ensayo retrospectivo reciente que evaluó el perfil de seguridad de risankizumab en pacientes con hepatitis vírica crónica confirmó la ausencia de reducción de la función hepática o la elevación de las cargas víricas. En su lugar, los pacientes tratados experimentaron una reducción de la progresión de fibrosis hepática. Este resultado positivo se atribuye probablemente al compromiso de IL-23 en este proceso patológico5.
De igual modo, el riesgo de neoplasias no parece incrementarse con el uso a largo plazo de inhibidores de IL-236. Los estudios preclínicos han reflejado que los niveles de IL-23 se correlacionan con un peor pronóstico en muchas neoplasias humanas. Debido a los efectos estimuladores de tumores observados de IL-23, se ha sugerido que la inhibición de esta citocina, y sus vías descendentes, pueden tener efectos protectores frente a la tumorigénesis y metástasis7.
Por último, la posibilidad de incrementar el intervalo entre las dosis de risankizumab puede ser relevante para los pacientes complejos tales como los reportados anteriormente. En el ensayo clínico de fase III IMMhance, se observó una durabilidad significativa de la respuesta tras la retirada de risankizumab, observándose un hallazgo similar con guselkumab, otro inhibidor de IL-238. Además, el estudio GUIDE está evaluando actualmente la posibilidad de incrementar el intervalo de las dosis en los pacientes con terapia de guselkumab, y los datos preliminares han reflejado la idoneidad de ampliarlo a un intervalo cada 16 semanas en un subgrupo de pacientes9. Recientemente se ha observado que administrar risankizumab “según necesidad”, una vez lograda la remisión clínica, podría ser un plan de mantenimiento factible par los pacientes con psoriasis. Este fenómeno clínico está probablemente relacionado con los efectos de la inhibición de IL-23 en las células de memoria residentes en los tejidos y las células T reguladoras10.
En conclusión, debido a su mecanismo de acción, eficacia y perfil de seguridad, risankizumab puede considerarse una opción segura para pacientes complejos con psoriasis e inmunosupresión concomitante, como en el caso de los receptores de trasplantes de tumores sólidos.
Conflicto de interesesM.L. y A.M.L. no tienen conflicto de intereses. T.T. declara los conflictos de interés siguientes: AbbVie, Almirall, Amgen, Arena Pharmaceuticals, Biocad, Biogen, Boehringer Ingelheim, Bristol Myers Squibb, Celgene, Fresenius Kabi, Janssen, LEO Pharma, Eli Lilly, MSD, Mylan, Novartis, Pfizer, Samsung-Bioepis, Sanofi-Genzyme, Sandoz y UCB.