La hidradenitis supurativa (HS) es una enfermedad inflamatoria crónica del folículo piloso caracterizada por nódulos, abscesos, fístulas y cicatrices. Sus principales comorbilidades incluyen la obesidad, la diabetes mellitus (DM), el síndrome metabólico (SM) y el síndrome del ovario poliquístico (SOP)1.
La metformina, principal tratamiento para la DM 2, debido a su capacidad para mejorar la sensibilidad tisular a la insulina, también exhibe propiedades pleiotrópicas antiinflamatorias e inmunorreguladoras, según el reciente trabajo de Petrasca et al.1. Este estudio señala la capacidad de la metformina para atenuar la glicólisis y la vía de la diana de la rapamicina en mamíferos (mTOR). Además, se evidenció su capacidad para normalizar los perfiles de expresión de interleucina (IL)-17A, interferón-gamma e IL-6 en neutrófilos y explantes cutáneos de pacientes con HS2.
El uso de la metformina como segunda línea en HS en la práctica clínica es frecuente1. Sin embargo, pese a incluirse en las guías americana (nivel de recomendación 3) y británica (good practice point), no existen ensayos clínicos que evalúen su eficacia3,4.
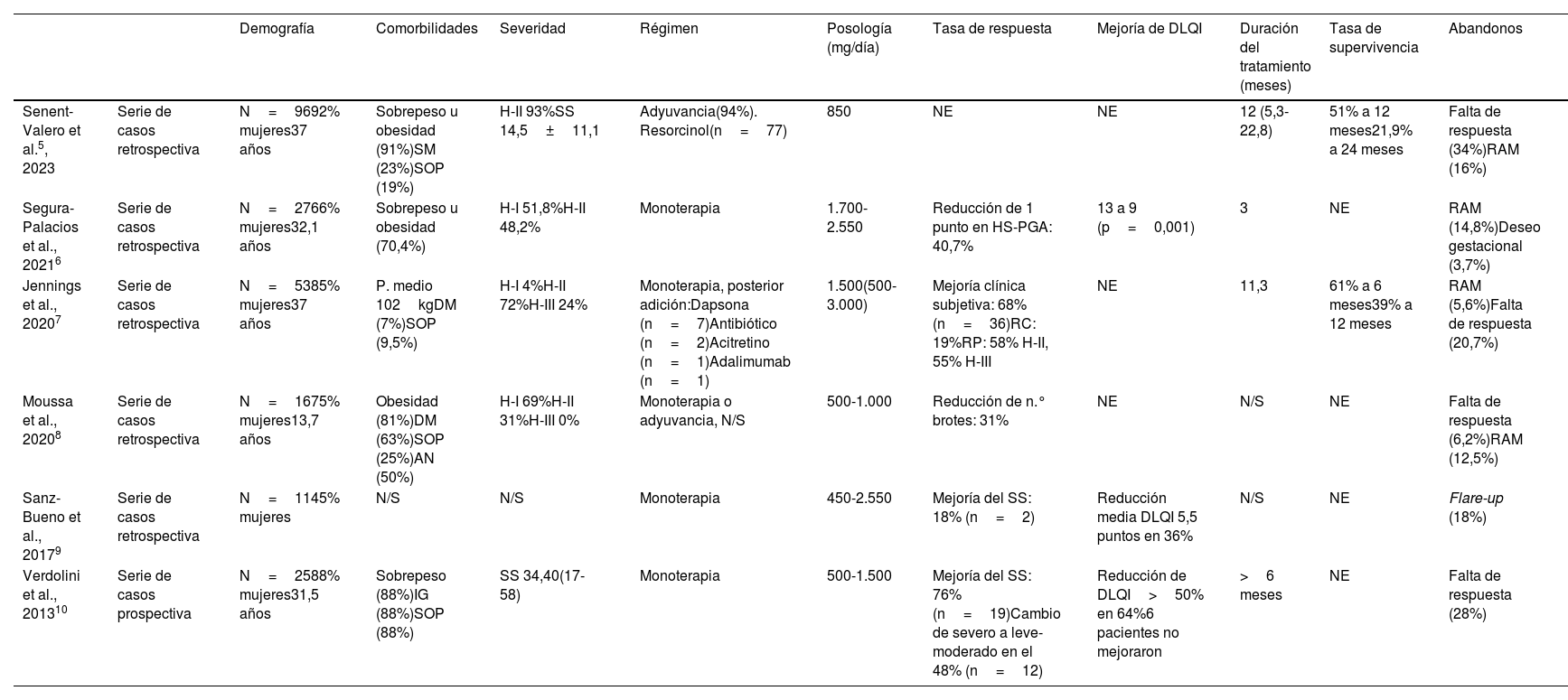
La evidencia actual proviene de 6 series de casos (tabla 1)1,5, abarcando 228 pacientes tratados con metformina, mayoritariamente mujeres (83,3%), con una edad media de 38,4 años. Más del 50% de los casos presentaban sobrepeso u obesidad, y comorbilidades como SOP (21,2%) o DM (9,6%). Una serie registró 16 pacientes pediátricos. La escala de Hurley fue la más empleada para definir la gravedad y el estadio Hurley II el más representado (139 pacientes).
Resumen de las series de casos publicadas de pacientes con HS tratados con metformina
| Demografía | Comorbilidades | Severidad | Régimen | Posología (mg/día) | Tasa de respuesta | Mejoría de DLQI | Duración del tratamiento (meses) | Tasa de supervivencia | Abandonos | ||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Senent-Valero et al.5, 2023 | Serie de casos retrospectiva | N=9692% mujeres37 años | Sobrepeso u obesidad (91%)SM (23%)SOP (19%) | H-II 93%SS 14,5±11,1 | Adyuvancia(94%). Resorcinol(n=77) | 850 | NE | NE | 12 (5,3-22,8) | 51% a 12 meses21,9% a 24 meses | Falta de respuesta (34%)RAM (16%) |
| Segura-Palacios et al., 20216 | Serie de casos retrospectiva | N=2766% mujeres32,1 años | Sobrepeso u obesidad (70,4%) | H-I 51,8%H-II 48,2% | Monoterapia | 1.700-2.550 | Reducción de 1 punto en HS-PGA: 40,7% | 13 a 9 (p=0,001) | 3 | NE | RAM (14,8%)Deseo gestacional (3,7%) |
| Jennings et al., 20207 | Serie de casos retrospectiva | N=5385% mujeres37 años | P. medio 102kgDM (7%)SOP (9,5%) | H-I 4%H-II 72%H-III 24% | Monoterapia, posterior adición:Dapsona (n=7)Antibiótico (n=2)Acitretino (n=1)Adalimumab (n=1) | 1.500(500-3.000) | Mejoría clínica subjetiva: 68% (n=36)RC: 19%RP: 58% H-II, 55% H-III | NE | 11,3 | 61% a 6 meses39% a 12 meses | RAM (5,6%)Falta de respuesta (20,7%) |
| Moussa et al., 20208 | Serie de casos retrospectiva | N=1675% mujeres13,7 años | Obesidad (81%)DM (63%)SOP (25%)AN (50%) | H-I 69%H-II 31%H-III 0% | Monoterapia o adyuvancia, N/S | 500-1.000 | Reducción de n.° brotes: 31% | NE | N/S | NE | Falta de respuesta (6,2%)RAM (12,5%) |
| Sanz-Bueno et al., 20179 | Serie de casos retrospectiva | N=1145% mujeres | N/S | N/S | Monoterapia | 450-2.550 | Mejoría del SS: 18% (n=2) | Reducción media DLQI 5,5 puntos en 36% | N/S | NE | Flare-up (18%) |
| Verdolini et al., 201310 | Serie de casos prospectiva | N=2588% mujeres31,5 años | Sobrepeso (88%)IG (88%)SOP (88%) | SS 34,40(17-58) | Monoterapia | 500-1.500 | Mejoría del SS: 76% (n=19)Cambio de severo a leve-moderado en el 48% (n=12) | Reducción de DLQI>50% en 64%6 pacientes no mejoraron | >6 meses | NE | Falta de respuesta (28%) |
AN: acantosis nigricans; DLQI: Dermatology Life Quality Index; DM: diabetes mellitus; HS-PGA: Hidradenitis Suppurativa Physician Global Assessment; IG: intolerancia glucídica; RAM: reacción adversa medicamentosa; SM: síndrome metabólico; SOP: síndrome de ovario poliquístico.
Existen importantes disparidades en los métodos de evaluación utilizados, solo empleándose herramientas estandarizadas (Sartorius Score, Physician Global Assestment) en 3 de los estudios. El resto emplearon descriptores de actividad (número de brotes, supuración y dolor). Pese a la heterogeneidad, la mayoría de los estudios recogieron mejorías clínicas en el 31-76% de los pacientes. La falta de respuesta fue la causa más frecuente de abandono (6,2-34%). La metformina fue bien tolerada y las molestias digestivas transitorias el efecto adverso más reportado y, aunque la serie pediátrica describió 2 casos de cambios de humor, no precisaron suspensión. Tres estudios describieron cambios en el Dermatology Quality of Life Index (DLQI), y su reducción en 4 puntos demostró ser significativa (p<0,01) en una serie de 27 sujetos. Esta misma serie mostró una tasa de supervivencia a 12 meses del 31%. Solo 2 series han aportado datos de supervivencia, la más reciente por Senent-Valero et al., quienes mostraron una persistencia del fármaco del 51% a 12 meses y del 21,9% a 24 meses en una cohorte de 96 pacientes, la mayor publicada hasta la fecha5.
Así, a pesar de la heterogenicidad de los datos disponibles, la metformina se presenta como opción terapéutica, económica y bien tolerada, con propiedades prometedoras para pacientes con HS leve-moderada. Es posible que el bajo porcentaje de pacientes con comorbilidades (DM, SOP) incluidos en las series subestime el efecto real del fármaco en estos subgrupos. Aunque los datos recogidos apoyan el uso de metformina en HS, se requieren estudios adicionales para evaluar con precisión su eficacia y seguridad.