INTRODUCCION
El angioedema es un edema de la dermis profunda que se localiza fundamentalmente en los labios, la lengua y en la zona periorbitaria, aunque en ocasiones afecta a manos, pies y genitales. El angioedema suele ser idiopático, aunque a veces se relaciona con alergias a determinados alimentos y fármacos por un mecanismo mediado por IgE. En otras ocasiones se asocia a un déficit (hereditario o adquirido) del inhibidor de la C-1 esterasa1. El angioedema producido por medicamentos puede no ser mediado por IgE, como por ejemplo el producido por los inhibidores de la enzima convertidora de angiotensina (IECA) y los antagonistas de los receptores de angiotensina II (ARA II).
DESCRIPCION DEL CASO
Un varón de 70 años, con antecedentes personales de enfermedad pulmonar obstructiva crónica e hipertensión arterial (HTA) sufrió un episodio de angioedema 2 meses después de la toma de un IECA (captropil 25 mg/12 h), que se resolvió al suprimir la medicación y sustituirla por hidroclorotiazida (50 mg/24 h). Seis meses después, el paciente no presentaba buen control de su HTA, por lo que se inició tratamiento con un ARA II (losartán 12,5 mg/24 h).
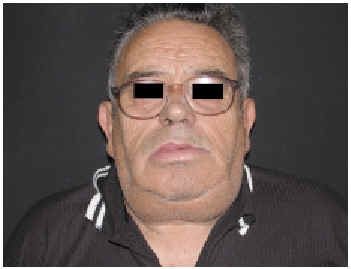
Tres meses después, el paciente volvió a presentar un episodio de angioedema, localizado en el labio inferior, sin edema en orofaringe ni disnea (fig. 1). Se trató con prednisolona 80 mg por vía intramuscular y dexclorfeniramina 5 mg por vía intramuscular con una mejoría leve del edema. Se retiró el losartán y se administró tratamiento ambulatorio con prednisona a dosis de 60 mg/24 h y dexclorfeniramina 2 mg/12 h. A las 48 h de empezar el tratamiento, las lesiones habían desaparecido, por lo que se suprimió la medicación. El paciente se encuentra actualmente en tratamiento con un antagonista del calcio (amlodipino 10 mg/24 h), sin que hayan aparecido nuevos episodios de angioedema y con un control adecuado de su HTA, tras 6 meses de seguimiento.
Fig. 1.--Angioedema localizado en labio inferior.
DISCUSION
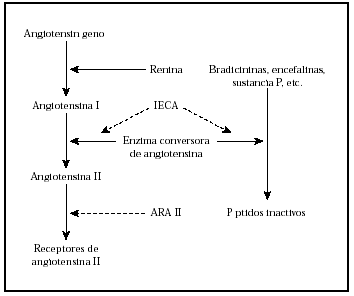
Dentro del grupo de los IECA2,3 se incluyen el benazepril, captopril, cilazapril, enalapril, espirapril, fosinopril, perindopril, quinapril, ramipril, trandopril y lisinopril. Actúan a nivel del sistema renina-angiotensina (SRA), inhibiendo el paso de angiotensina I a angiotensina II, al unirse a la enzima conversora de angiotensina (ECA) por su zona activa (fig. 2).
Fig. 2.--Representación esquemática del sistema renina-angiotensina. IECA: inhibidor de la enzima conversora de angiotensina. ARA II: antagonista de los receptores de angiotensina II.
Los efectos secundarios de los IECA son poco frecuentes4-7 e incluyen varios efectos adversos cutáneos (erupciones ampollosas, prurito, urticaria, pitiriasis rosada, vasculitis, fotosensibilidad, erupciones psoriasiformes, maculopapulares o liquenoides)7. El angioedema, ocurre en un 0,1-1 % de los pacientes tratados5,6 y es el más importante por su posible compromiso vital. Al no tener un mecanismo inmunológico, los corticoides y los antihistamínicos no suelen influir en su evolución8, siendo el tratamiento de elección la retirada de la medicación. El tiempo transcurrido entre la toma del fármaco y la aparición del angioedema7 puede variar de días a meses y el angioedema se puede resolver de forma espontánea a pesar de continuar con el tratamiento. Factores que parecen predisponer a la aparición del angioedema incluyen la raza negra, pacientes con angioedema idiopático o pacientes con historia de manipulación de vías aéreas superiores7.
Los ARA II incluyen losartán, candesartán, eprosartán, irbesartán, telmisartán y valsartán. Su mecanismo de acción también implica al SRA, al impedir la unión de la angiotensina II a sus receptores (fig. 2). Aunque los ARA II evitan algunos de los efectos secundarios de los IECA, se han descrito casos de angioedema8-14 así como otras reacciones cutáneas, como vasculitis15 o seudolinfomas16 asociados a losartán.
En la literatura médica española sólo hemos encontrado un caso similar en 199914.
Las características clínicas del angioedema inducido por ARA II son muy parecidas a las del inducido por IECA, incluyendo el tiempo de latencia variable, que puede prolongarse hasta un año12.
El origen del angioedema asociado a IECA no está claro; una posible causa sería la acumulación de péptidos vasoactivos (bradicinina, sustancia P, histamina y prostaglandinas), los cuales son inactivados en condiciones normales por la ECA (fig. 2)17,18 explicaría por qué el angioedema se produce incluso cuando se cambia de IECA, pero esta hipótesis no explicaría la aparición de angioedema en pacientes que están siendo tratados con ARA II, pues en estos pacientes la ECA es funcionante y no se produce la acumulación de péptidos (fig. 2).
Una posible explicación se basa en la existencia de un SRA completo a nivel cutáneo, incluyendo el angiotensinógeno, la angiotensina II, la ECA, la renina y los receptores de angiotensina AT1 y AT2, que actuaría a nivel local de forma autocrina y paracrina. Aunque su función fisiológica no es bien conocida, y tampoco se conocen las consecuencias de una disminución de su síntesis, Steckelings et al7 han propuesto como posible causa del angioedema y de otros efectos cutáneos de los IECA y los ARA II la afectación de este SRA cutáneo.
Algunos pacientes con angioedema relacionado con ARA II han presentado antes episodios de angioedema relacionados con la toma de IECA10,13,14, como en nuestro caso, lo que parece indicar un mecanismo común en ambos procesos. Este dato es importante en el manejo diario de pacientes con HTA, para evitar administrar un ARA II a un paciente que ha tenido previamente un episodio de angioedema relacionado con IECA. Al no tratarse de un mecanismo mediado por IgE la realización de pruebas epicutáneas o prueba por punción (prick-test) no resulta útil en estos pacientes, y la provocación oral con otros IECA o ARA II puede poner en peligro la vida, por lo que no se debe realizar. Sin embargo, en otras reacciones cutáneas provocadas por IECA19,20 se ha demostrado mediante pruebas epicutáneas y pruebas de provocación oral, que no hay reacciones cruzadas, por lo que en estos casos sí podría hacerse un intento terapéutico con otros fármacos de la familia.