El angiosarcoma es un tumor de origen endotelial de comportamiento agresivo de mal pronóstico. Nuevos tratamientos como el bevacizumab basan su eficacia en su capacidad anti-angiogénica, actuando sobre el factor de crecimiento vascular endotelial (VEGF) implicado en la patogenia1,2.
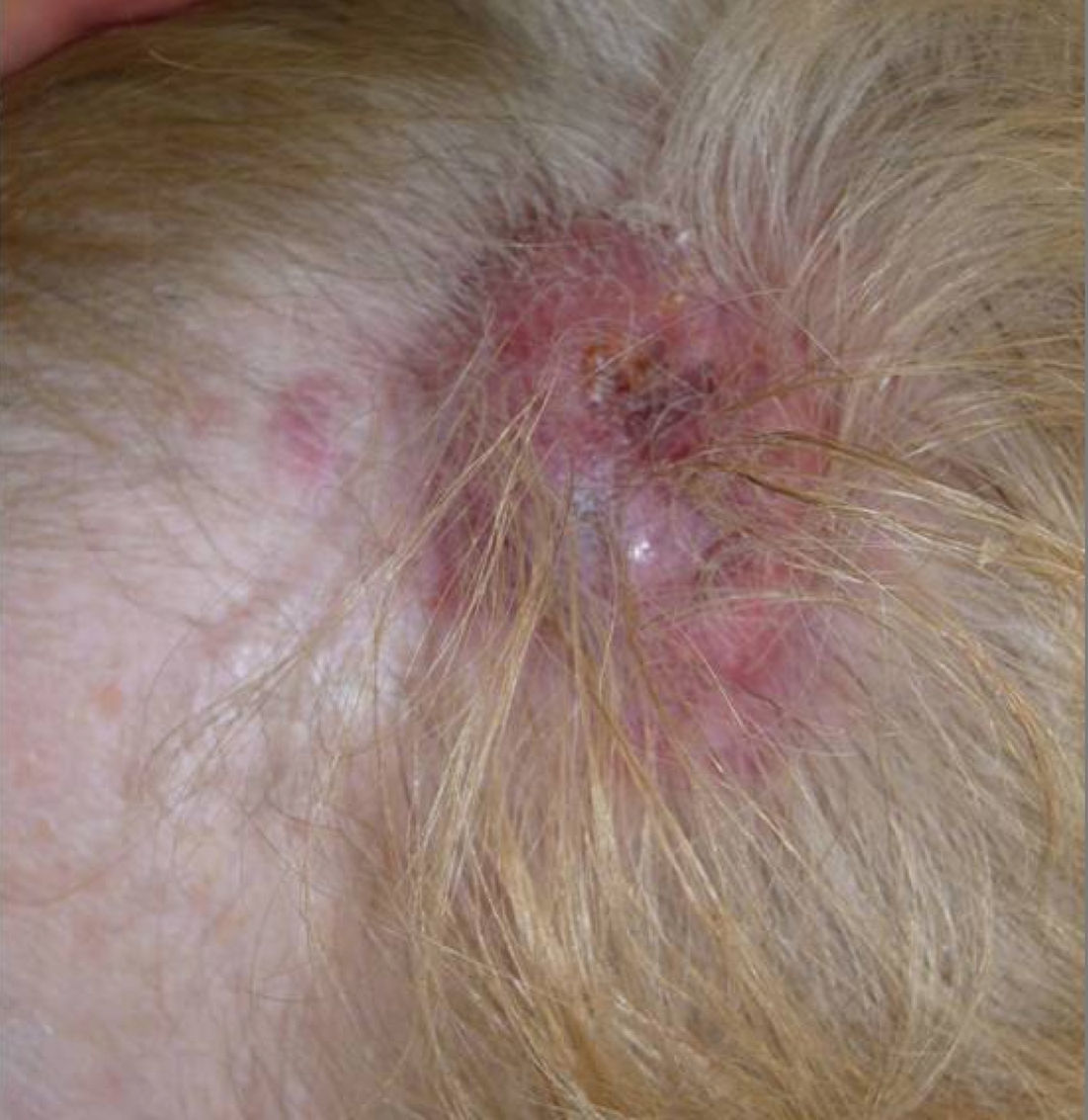
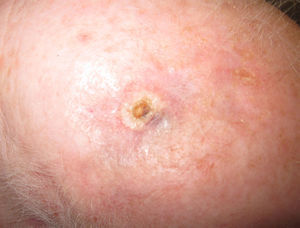
Presentamos el caso de una mujer de 68 años que consultó por una lesión tumoral, eritematoviolácea, de 1cm de diámetro, localizada en el cuero cabelludo. La biopsia cutánea fue compatible con un angiosarcoma pobremente diferenciado. En un período de un mes la lesión creció rápidamente convirtiéndose en una tumoración multilobulada y ulcerada que asentaba sobre un área que abarcaba toda la mitad izquierda del cuero cabelludo y la región occipital derecha, en la que se identificaban máculas de 1-2cm de diámetro rojo-vinosas (fig. 1).
Se realizó una tomografía axial computarizada (TAC) que descartó afectación a distancia, por lo que se estableció el diagnóstico de angiosarcoma pobremente diferenciado (T2b, N0, M0) estadio iii de la American Joint Committee on Cancer 2010 (AJCC 2010).
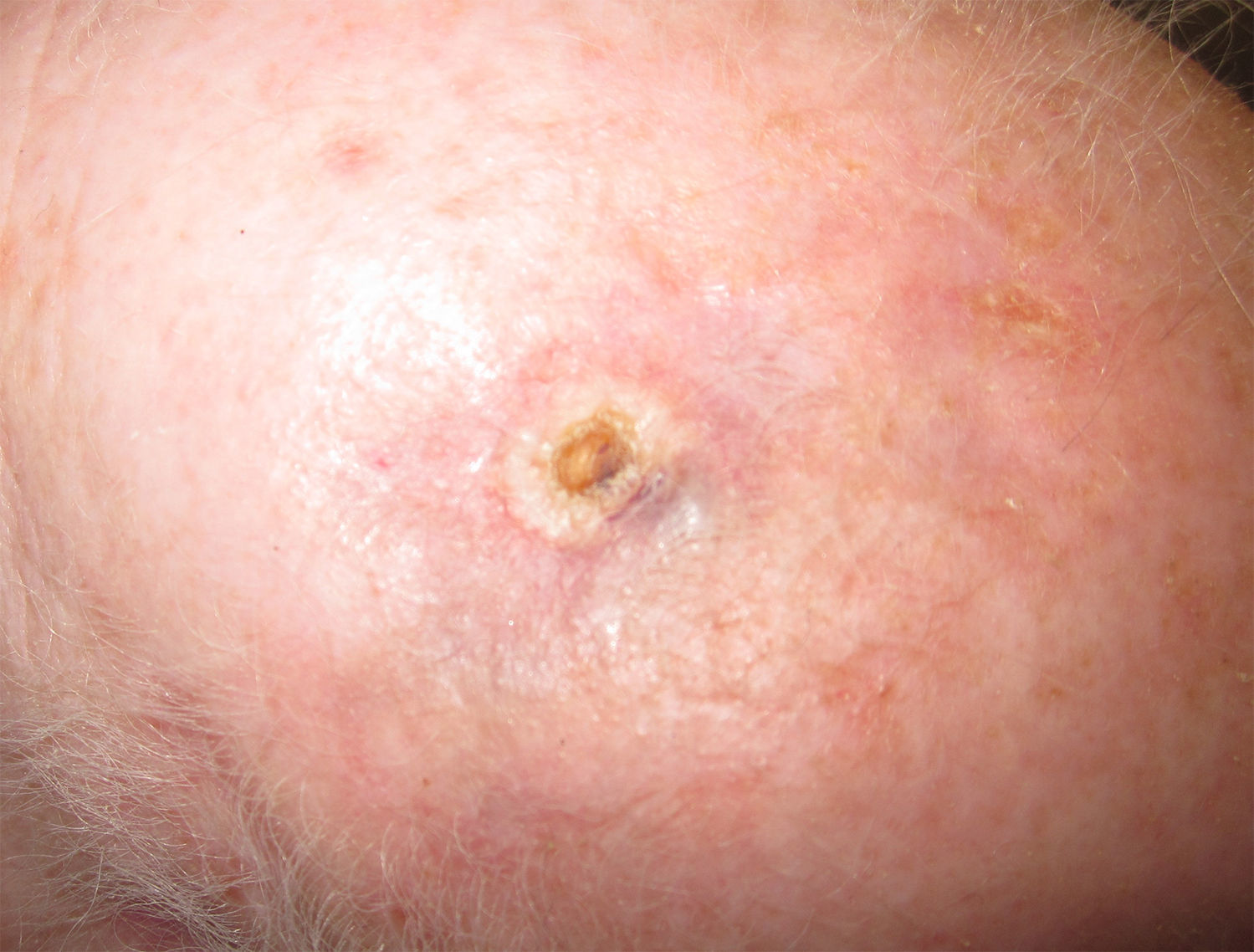
Se descartó tratamiento quirúrgico inicial dada la extensión de la lesión, que ocupaba más de la mitad del cuero cabelludo, y se inició tratamiento neoadyuvante con paclitaxel (80mg/m2 semanal) y bevacizumab (en uso compasivo, 10mg/kg cada 15 días), con una rápida respuesta de la lesión (fig. 2). Finalizó el tratamiento tras 14 ciclos (cada ciclo consistió en una infusión de bevacizumab y 2 de paclitaxel) con buena tolerancia. Se realizó extirpación quirúrgica de la lesión cicatricial sin evidencia de angiosarcoma en esta área en el estudio anatomopatológico. Posteriormente se inició radioterapia adyuvante (fracciones de 2Gy al día, hasta alcanzar una dosis total de 50Gy) concomitante con bevacizumab (5mg/kg cada 2 semanas) ante la persistencia de una lesión macular rojo-vinosa en el área preauricular izquierda, y a pesar de la biopsia no confirmatoria de angiosarcoma. Al finalizar ambos tratamientos mantenía respuesta completa de la enfermedad.
Dos meses después empeoró su estado general y se detectó recidiva clínica del angiosarcoma en la región preauricular izquierda. En la TAC se evidenciaron metástasis óseas. Se reinició la terapia combinada con paclitaxel y bevacizumab, pero la enfermedad progresó y la paciente falleció 14 meses después del diagnóstico.
El angiosarcoma es un tumor poco frecuente con comportamiento muy agresivo y una elevada capacidad metastásica. Se clasifica en 3 formas diferentes, siendo la clásica (de cabeza y cuello) la más frecuente3. El tratamiento de elección es quirúrgico, con márgenes amplios, seguido de radioterapia adyuvante a dosis elevadas (>50Gy)1,4,5 sobre campos amplios. En estadios avanzados o tumores irresecables la quimioterapia es la única opción terapéutica, pero no existen ensayos clínicos que avalen la eficacia de los diferentes regímenes terapéuticos1,2. Las pautas de quimioterapia muchas veces están limitadas por su toxicidad1. Las más utilizadas actualmente incluyen antraciclinas y taxanos, pero la respuesta es limitada. En estudios prospectivos de tratamiento del angiosarcoma cutáneo con paclitaxel la supervivencia media fue de 8 meses con un tiempo medio libre de progresión de la enfermedad de 4 meses2.
Por todos estos motivos interesa la búsqueda de nuevos fármacos que añadan eficacia y tolerabilidad a los tratamientos. Actualmente las moléculas antiangiogénicas son objetivo de estudio en este campo.
El angiosarcoma se desarrolla a partir de células endoteliales vasculares. Existen varios factores implicados en su patogenia, siendo uno de los más importantes el factor de crecimiento VEGF-A1,2. El VEGF-A es un factor de crecimiento implicado en la formación de nuevos vasos sanguíneos mediante la estimulación de receptores con actividad tirosín-cinasa de la superficie de células endoteliales. Su sobreexpresión por parte de las células neoplásicas, demostrada tanto en el angiosarcoma como en otros tumores (pulmón, mama, colorrectal), favorece la angiogénesis y, por lo tanto, el aporte sanguíneo y el crecimiento tumoral2,6. El bevacizumab es un anticuerpo monoclonal dirigido contra el VEGF-A que actúa impidiendo la unión a su receptor y, por lo tanto, inhibiendo la angiogénesis. No obstante las recidivas y los periodos libres de progresión observados, de una duración limitada, hacen suponer otros mecanismos implicados que hacen que el bloqueo de VEGF no sea suficiente para impedir el desarrollo de este tumor7.
Existen 5 casos publicados hasta la fecha de angiosarcoma cutáneo tratado con bevacizumab, solo o asociado a otros tratamientos. En todos ellos la respuesta fue favorable, con tiempos de supervivencia mayores de los obtenidos con otras terapias, y con buena tolerabilidad por parte de los pacientes (tabla 1).
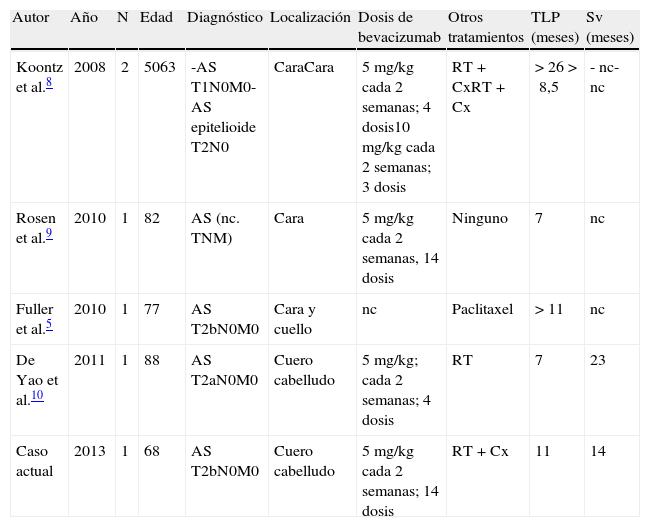
Casos de angiosarcomas tratados con bevacizumab publicados hasta la fecha
| Autor | Año | N | Edad | Diagnóstico | Localización | Dosis de bevacizumab | Otros tratamientos | TLP (meses) | Sv (meses) |
| Koontz et al.8 | 2008 | 2 | 5063 | -AS T1N0M0-AS epitelioide T2N0 | CaraCara | 5mg/kg cada 2 semanas; 4 dosis10mg/kg cada 2 semanas; 3 dosis | RT+CxRT+Cx | >26>8,5 | - nc- nc |
| Rosen et al.9 | 2010 | 1 | 82 | AS (nc. TNM) | Cara | 5mg/kg cada 2 semanas, 14 dosis | Ninguno | 7 | nc |
| Fuller et al.5 | 2010 | 1 | 77 | AS T2bN0M0 | Cara y cuello | nc | Paclitaxel | >11 | nc |
| De Yao et al.10 | 2011 | 1 | 88 | AS T2aN0M0 | Cuero cabelludo | 5mg/kg; cada 2 semanas; 4 dosis | RT | 7 | 23 |
| Caso actual | 2013 | 1 | 68 | AS T2bN0M0 | Cuero cabelludo | 5mg/kg cada 2 semanas; 14 dosis | RT+Cx | 11 | 14 |
AS: angiosarcoma; Cx: cirugía; N: número de pacientes; nc: no consta; RT: radioterapia; Sv: Supervivencia; TLP: tiempo libre de progresión.
Recientemente han sido publicados los resultados del primer ensayo clínico en fase ii sobre la utilización del bevacizumab en monoterapia para el tratamiento del angiosarcoma metastásico o localmente avanzado. Los resultados de Agulnik et al. son prometedores, ya que un 50% de los sujetos del estudio presentaron una estabilización de su enfermedad con un tiempo medio hasta la progresión de la enfermedad de 26 semanas2.
Consideramos que bevacizumab podría ser tenido en cuenta para su utilización en casos similares al presentado, dada la escasa disponibilidad de tratamientos eficaces y los resultados observados en los casos publicados y en los recientes ensayos clínicos. Además, todo parece indicar que en el futuro bevacizumab en combinación con otros fármacos podría mejorar el pronóstico de estos pacientes.