Existen diversas opciones terapéuticas para los hemangiomas infantiles (HI). El propranolol se utiliza con base en un ensayo pivotal. Nuestro objetivo fue describir las características del HI en la práctica clínica, incluyendo las terapias utilizadas, así como comparar las características de los pacientes tratados con propranolol y las de los pacientes del ensayo, para valorar su validez externa.
MétodosSe incluyó consecutivamente a los pacientes que acudieron a doce hospitales españoles desde junio de 2016 a octubre de 2019 (n=601).
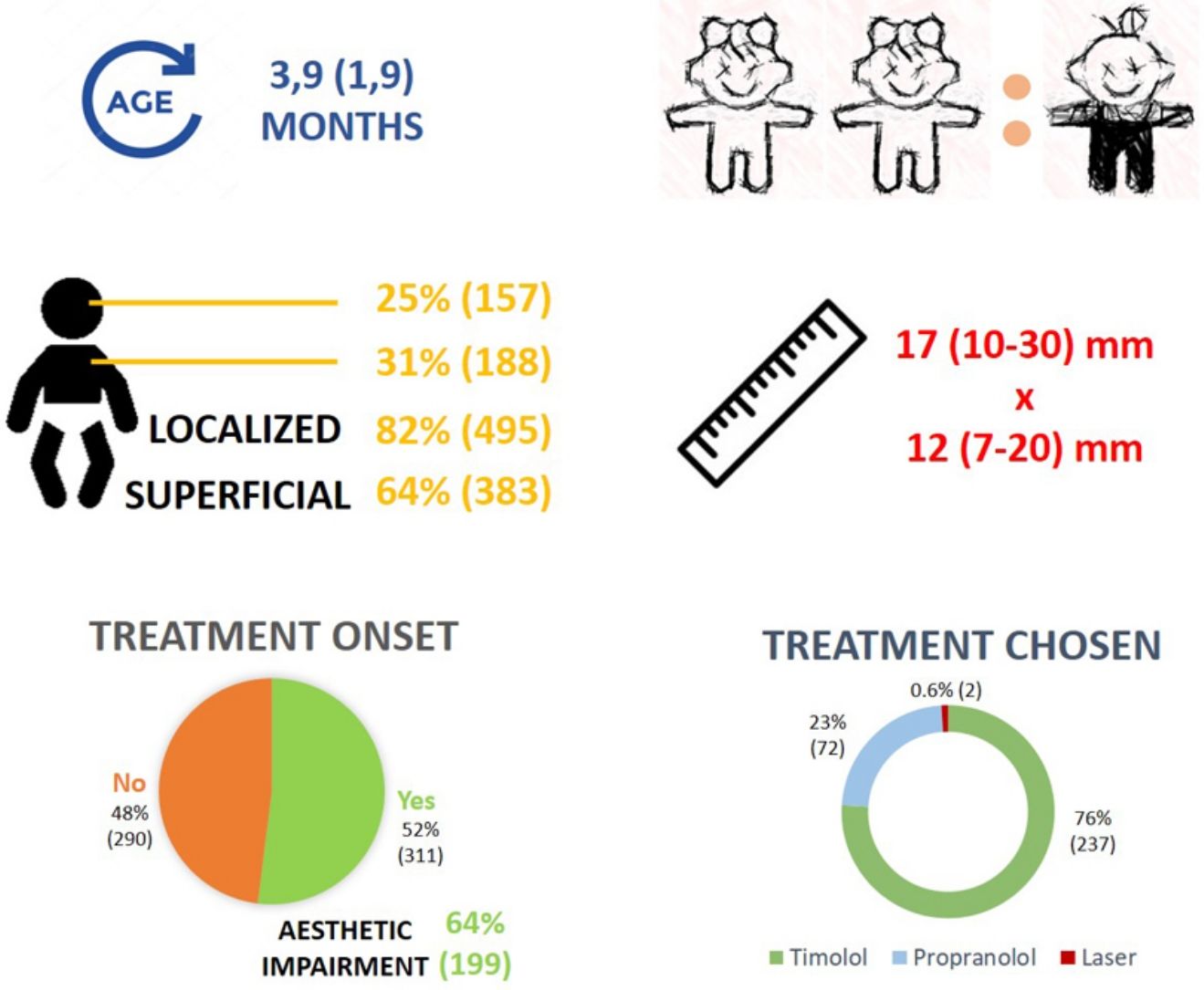
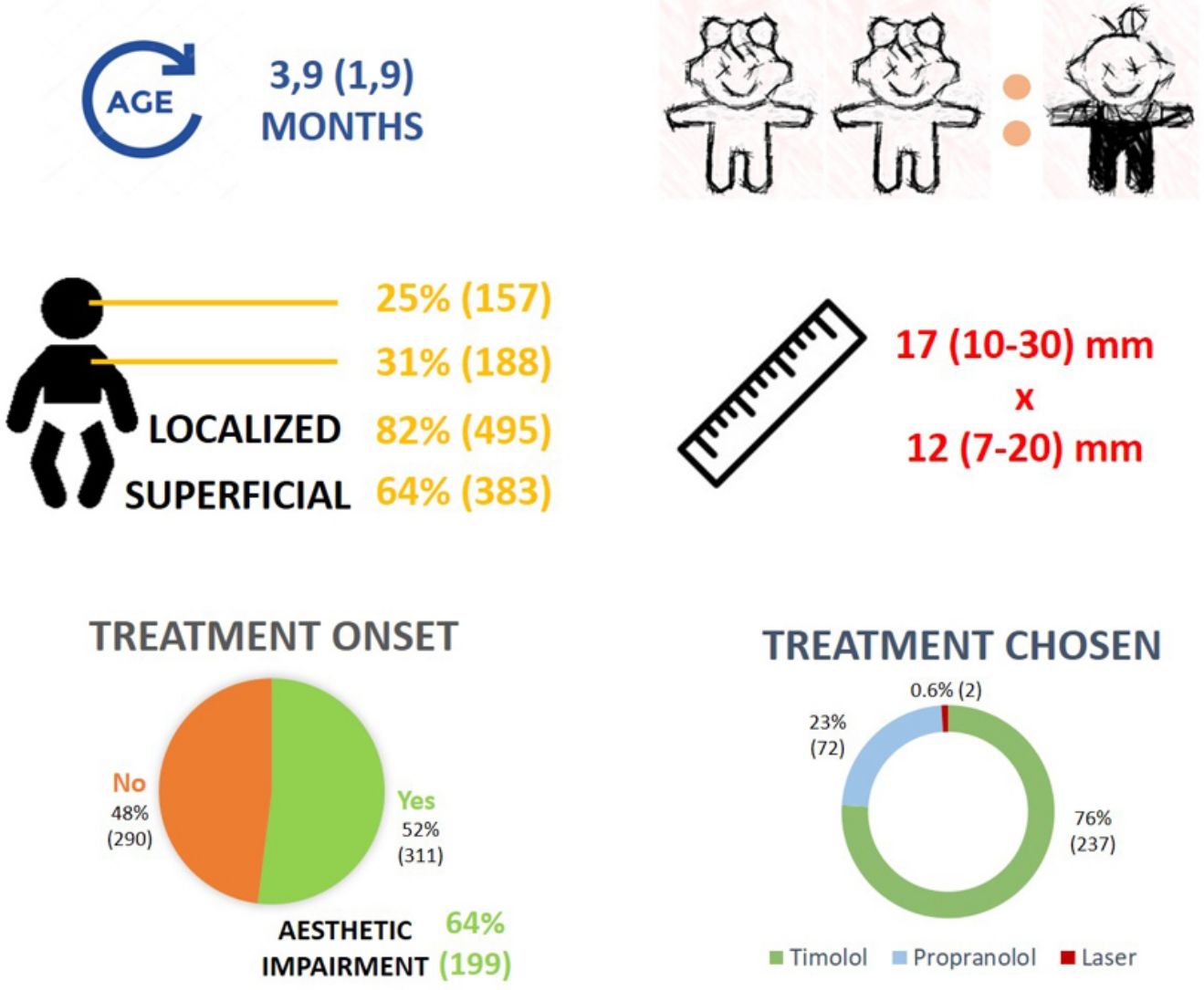
ResultadosLa edad media fue de 3,9 (DE:1,9) meses, con una ratio mujer-varón de 2:1. La mayoría de los HI fueron de tipo localizado (82%, 495), superficial (64%, 383) y ubicados en cara (25%, 157) y tronco (31%, 188). El tamaño mediano fue de 17 (RI: 10-30) x 12 (RI: 7-20) mm. Se encontraron complicaciones en 16 (3%) pacientes. Se inició tratamiento en el 52% (311) de los casos. La mayoría de los pacientes recibió timolol (76%, 237), reservándose propranolol para las complicaciones o los HI de alto riesgo. El compromiso estético fue el principal motivo de iniciar la terapia (64%, 199). Las diversas características de los pacientes y de los HI tratados con propranolol fueron similares a las del ensayo clínico pivotal, aunque 1/3 de los HI no alcanzó el diámetro mínimo para cumplir los criterios de inclusión, y no se comunicó información pronóstica importante.
ConclusionesDado que muchos pacientes reciben tratamiento debido al compromiso estético, existe una necesidad de conocer mejor los resultados estéticos de las terapias e incrementar la evidencia sobre el uso de timolol, que actualmente es la terapia más común. El propranolol está siendo utilizado en una población generalmente similar a la del ensayo; sin embargo, esta afirmación no puede confirmarse de manera definitiva.
There are several therapeutic options for infantile haemangiomas (IH). Propranolol is used according to a pivotal trial. We aimed to describe the characteristics of IH in clinical practice, including the therapies used, and to compare the characteristics of patients treated with propranolol with those of the trial to assess its external validity.
MethodsConsecutive patients attending 12 Spanish hospitals from June 2016 to October 2019 were included (n=601).
ResultsThe mean age was 3.9 (SD:1.9) months, with a 2:1 female-to-male ratio. Most IHs were localized (82%, 495), superficial (64%, 383) and located in the face (25%, 157) and trunk (31%, 188). Median size was 17 (IR: 10-30) x 12 (IR: 7-20) mm. Complications were found in 16 (3%) patients. Treatment was initiated for 52% (311). Most patients received timolol (76%, 237); propranolol was reserved for complications or high-risk IHs. Aesthetic impairment was the main reason for starting therapy (64%, 199). Several characteristics of the patients and IHs treated with propranolol are similar to those of the pivotal clinical trial, but 1/3 of IHs did not reach the minimum diameter to meet the inclusion criteria, and important prognostic information was not reported.
ConclusionsAs most patients receive treatment for aesthetic impairment, there is a need to better understand the aesthetic results of therapies and to increase evidence on the use of timolol, which is currently the most common therapy. Propranolol is being used in a population generally similar to that of the trial; however, this statement cannot be definitely confirmed.
Los hemangiomas infantiles (HI) son los tumores de tejidos blandos más comunes en la infancia1, con una ratio mujer-varón que oscila entre 2:1 y 5:12,3. La prevalencia se estima cercana al 10% de los recién nacidos2. Una de las principales localizaciones de los HI es la de cabeza y cuello2,4–8, con implicaciones estéticas posteriores. En ciertas localizaciones, los HI pueden interferir incluso en el desarrollo de las funciones vitales o afectar a la calidad de vida tanto de los niños como de sus padres9–11. Aproximadamente el 10% de los HI desarrollan ulceraciones, especialmente aquellos con componente superficial12,13.
Aunque todos los HI involucionan con el tiempo, entre el 46% y el 69% pueden dejar secuelas en ausencia de tratamiento, tales como tejido fibroadiposo, anetoderma, atrofia, telangiectasias, cambios de la coloración de la piel o cicatrices, de haberse producido ulceración. Se han realizado muchos estudios que evalúan las secuelas o las características epidemiológicas de los HI con carácter previo al uso de propranolol, que ha cambiado el paradigma del tratamiento de estas lesiones una vez que ha quedado demostrada su efectividad en un ensayo clínico, y que su uso ha sido aprobado para tratar los HI17. Sin embargo, aunque el compromiso estético parece ser un motivo importante para iniciar el tratamiento con propranolol, en el ensayo se evaluaron las respuestas completas o casi completas al tratamiento, pero no se analizaron las posibles secuelas tras el mismo, y el compromiso estético no fue un criterio de inclusión. Además, los estudios previos encontraron que el 91% de los pacientes tratados con propranolol presentaron secuelas, y el 74% presentaron secuelas graves, aunque los criterios de inclusión fueron restrictivos y las dosificaciones de propranolol subóptimas18.
Dado el contexto clínico cambiante de este tumor común, que puede afectar gravemente a los niños, la falta de buenas descripciones de la fase involutiva y de las posibles secuelas en los estudios prospectivos a largo plazo19,20, así como la aparición de un nuevo tratamiento eficaz, decidimos iniciar una cohorte prospectiva española de HI
Los objetivos del presente artículo fueron 1) describir los HI observados en la práctica clínica, incluyendo las características demográficas y clínicas y las terapias utilizadas, y 2) comparar nuestros datos sobre los pacientes tratados con propranolol en la práctica común y los del ensayo clínico aleatorizado pivotal17, para evaluar la validez externa del mismo.
Pacientes y métodosDiseñoLa Academia Española de Dermatología y Venereología (AEDV) inició una cohorte prospectiva nacional de HI en junio de 2016, extendiéndose el periodo de estudio a octubre de 2019. Los pacientes fueron reclutados de doce hospitales españoles con departamentos de dermatología pediátrica. Inicialmente se planificó un estudio de seguimiento a cinco años, que sigue en curso. Este artículo describe los datos basales de dicha cohorte.
Criterios de inclusiónSe incluyeron recién nacidos menores de nueve meses con uno o más HI diagnosticados por sus características clínicas específicas o, en caso de duda, por tinción inmunohistoquímica GLUT-1. Se incluyeron consecutivamente todos los pacientes que acudieron a uno de los hospitales participantes, independientemente de la terapia propuesta (observación clínica o tratamiento). Dado que se trata de un estudio observacional basado en la clínica, el enfoque terapéutico fue decidido durante la práctica clínica rutinaria.
Criterios de exclusiónSe excluyó a los pacientes siguientes: aquellos pacientes cuyos familiares tenían planificado un traslado a corto plazo que dificultara el seguimiento; los pacientes que habían iniciado ya algún tipo de tratamiento para HI en el momento de la visita basal; y los pacientes que rechazaron participar en el estudio.
Variables de interésSe registraron al inicio del seguimiento la historia obstétrica materna, las características demográficas y biométricas de los pacientes, las localizaciones de los HI y sus características, tales como los subtipos morfológicos y clínicos, el tamaño, la altura o el tipo de superficie y borde, la presencia o probabilidad de desarrollo de complicaciones, el inicio del tratamiento y los motivos de iniciar la terapia. Todo lo anterior constituyó los datos utilizados en este artículo. Los HI fueron clasificados en función de su distribución (subtipos morfológicos: localizado, indeterminado, segmentario y multifocal), y de su profundidad y bordes (subtipos clínicos: superficial, mixto-sésil, mixto-pedunculado, profundo y abortivo). Las complicaciones se definieron como la presencia de cualquiera de las situaciones siguientes: compromiso ocular, de la vía aérea o visceral, ulceraciones o compromiso funcional (visual, nasal, alimentario, de la vía aérea, tortícolis, obstrucción del conducto auditivo externo o cualquier otra función que el facultativo considerara importante). Las definiciones fueron registradas en el protocolo del estudio, y se creó un atlas fotográfico para garantizar la homogeneidad de la recopilación de los datos sobre las características de los HI.
Los datos fueron recabados por médicos experimentados (los dermatólogos responsables de los departamentos de dermatología pediátrica de cada hospital participante) utilizando un sistema de recopilación de datos online (Openclinica 3.1). El control de calidad consistió en la monitorización continua online mensual y además una monitorización anual presencial de una muestra aleatoria simple de 10 pacientes de cada uno de los hospitales (aprox. el 20% de los pacientes incluidos por año).
Análisis estadísticoSe utilizaron estadísticos descriptivos para explorar las características de la muestra. Utilizamos la prueba Shapiro-Wilk e histogramas para explorar la normalidad de las variables. Las variables continuas se expresaron como media y desviación estándar (DE) o mediana (percentiles 25-75). En cuanto a las variables cualitativas, se calcularon las frecuencias absoluta y relativa. Se evaluaron las diferencias entre las variables cualitativas mediante las pruebas χ2 o exacta de Fisher, según necesidad. Se evaluaron las diferencias entre las variables continuas mediante la prueba t de Student o la prueba U de Mann-Whitney. Los análisis estadísticos se realizaron utilizando el software estadístico STATA (versión 16.0; Statacorp, College Station, TX, EE. UU.).
ÉticaEl protocolo del estudio fue aprobado por el Comité del Hospital Santa Creu i Sant Pau (Barcelona, 16/079). Todos los padres o tutores de los pacientes firmaron un consentimiento informado escrito en el momento de su inclusión.
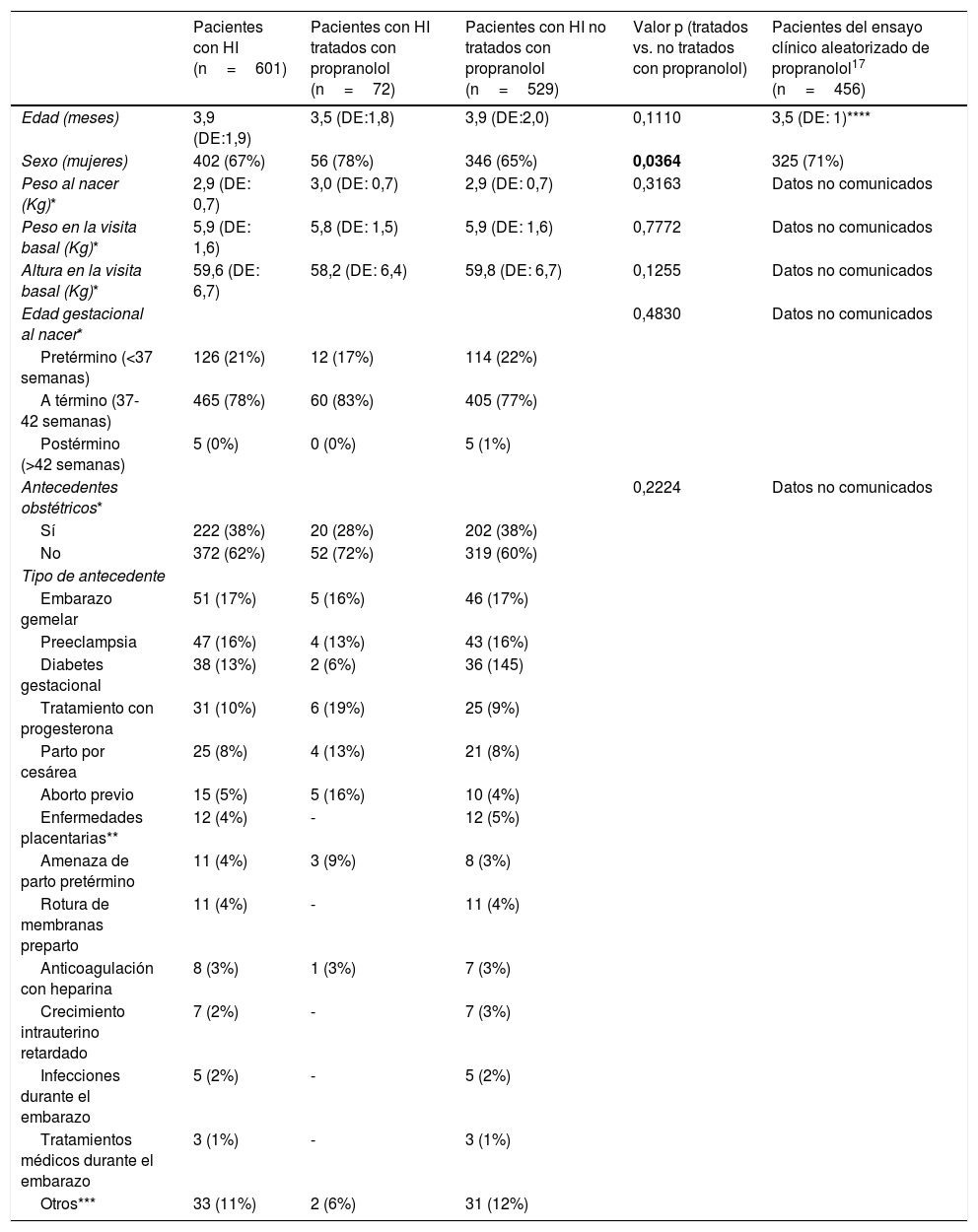
ResultadosCaracterísticas basalesLas características basales de la muestra se reflejan en la tabla 1. La edad media fue de aproximadamente 4 meses. Distinguiendo entre los subtipos clínicos de HI, la edad media de los pacientes con HI profundos fue de 4,5 meses, mientras que en los pacientes con HI con componente superficial fue de 3,8 meses (p=0,0075). Hubo una proporción superior de mujeres (ratio 2:1). El peso y altura medios en la visita basal fueron normales para la edad, al igual que el peso al nacer. La mayoría de recién nacidos llegaron a término. Más del 60% de las madres no tuvo antecedentes obstétricos de interés. Entre aquellas madres con antecedentes obstétricos, el embarazo gemelar, la preeclampsia, la diabetes gestacional y el tratamiento con progesterona fueron las situaciones más prevalentes. Los pacientes cuyas madres fueron tratadas con progesterona no mostraron diferencias en cuanto a complicaciones, tamaño medio o proporción de HI segmentario en comparación con aquellos pacientes cuyas madres no recibieron progesterona.
Características basales de la muestra
| Pacientes con HI (n=601) | Pacientes con HI tratados con propranolol (n=72) | Pacientes con HI no tratados con propranolol (n=529) | Valor p (tratados vs. no tratados con propranolol) | Pacientes del ensayo clínico aleatorizado de propranolol17 (n=456) | |
|---|---|---|---|---|---|
| Edad (meses) | 3,9 (DE:1,9) | 3,5 (DE:1,8) | 3,9 (DE:2,0) | 0,1110 | 3,5 (DE: 1)**** |
| Sexo (mujeres) | 402 (67%) | 56 (78%) | 346 (65%) | 0,0364 | 325 (71%) |
| Peso al nacer (Kg)* | 2,9 (DE: 0,7) | 3,0 (DE: 0,7) | 2,9 (DE: 0,7) | 0,3163 | Datos no comunicados |
| Peso en la visita basal (Kg)* | 5,9 (DE: 1,6) | 5,8 (DE: 1,5) | 5,9 (DE: 1,6) | 0,7772 | Datos no comunicados |
| Altura en la visita basal (Kg)* | 59,6 (DE: 6,7) | 58,2 (DE: 6,4) | 59,8 (DE: 6,7) | 0,1255 | Datos no comunicados |
| Edad gestacional al nacer* | 0,4830 | Datos no comunicados | |||
| Pretérmino (<37 semanas) | 126 (21%) | 12 (17%) | 114 (22%) | ||
| A término (37-42 semanas) | 465 (78%) | 60 (83%) | 405 (77%) | ||
| Postérmino (>42 semanas) | 5 (0%) | 0 (0%) | 5 (1%) | ||
| Antecedentes obstétricos* | 0,2224 | Datos no comunicados | |||
| Sí | 222 (38%) | 20 (28%) | 202 (38%) | ||
| No | 372 (62%) | 52 (72%) | 319 (60%) | ||
| Tipo de antecedente | |||||
| Embarazo gemelar | 51 (17%) | 5 (16%) | 46 (17%) | ||
| Preeclampsia | 47 (16%) | 4 (13%) | 43 (16%) | ||
| Diabetes gestacional | 38 (13%) | 2 (6%) | 36 (145) | ||
| Tratamiento con progesterona | 31 (10%) | 6 (19%) | 25 (9%) | ||
| Parto por cesárea | 25 (8%) | 4 (13%) | 21 (8%) | ||
| Aborto previo | 15 (5%) | 5 (16%) | 10 (4%) | ||
| Enfermedades placentarias** | 12 (4%) | - | 12 (5%) | ||
| Amenaza de parto pretérmino | 11 (4%) | 3 (9%) | 8 (3%) | ||
| Rotura de membranas preparto | 11 (4%) | - | 11 (4%) | ||
| Anticoagulación con heparina | 8 (3%) | 1 (3%) | 7 (3%) | ||
| Crecimiento intrauterino retardado | 7 (2%) | - | 7 (3%) | ||
| Infecciones durante el embarazo | 5 (2%) | - | 5 (2%) | ||
| Tratamientos médicos durante el embarazo | 3 (1%) | - | 3 (1%) | ||
| Otros*** | 33 (11%) | 2 (6%) | 31 (12%) | ||
Las variables continuas se expresan como media (desviación estándar). Las variables cualitativas se expresan como frecuencias absolutas (relativas). Los valores p estadísticamente significativos figuran en negrita.
Placenta previa (6), desprendimiento de placenta (4), hematoma placentario (1) y corioamnionitis (1).
Esta categoría incluye amenaza de aborto (6), hipotiroidismo (6), hipertensión (4), parto inducido (3), colestasis intrahepática del embarazo (3), hipertiroidismo (2), lupus (2), síndrome de HELLP (2), enfermedad de Crohn (1), consumo de drogas (1), nefropatía (1), esclerosis múltiple (1), neumotórax (1) y prolapso del saco amniótico (1). Adviértase que hubo madres con varias complicaciones.
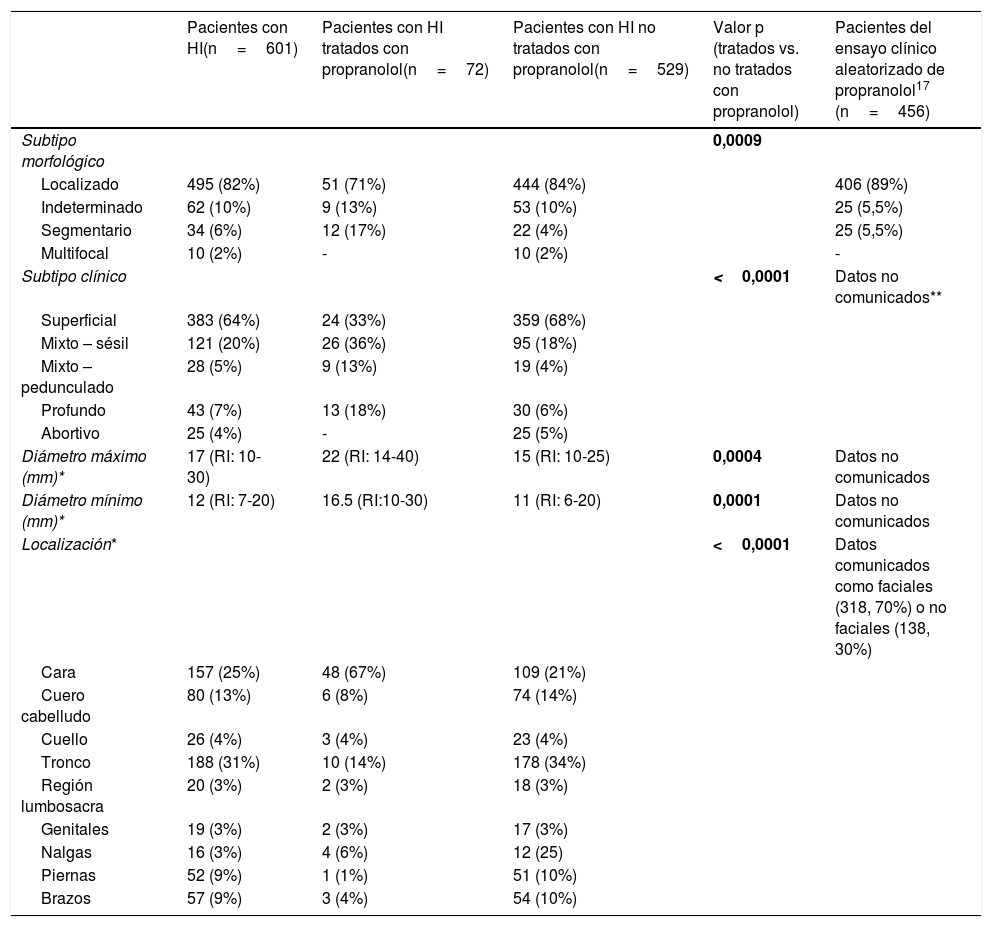
Las características y localizaciones de los HI se reflejan en la tabla 2. La mayoría de los HI fueron localizados y superficiales. El tamaño mediano (diámetro máximo x mínimo) fue de 17mm x 12mm. Las localizaciones más frecuentes fueron el tronco y la cara. Entre los hemangiomas con componente superficial, los HI superficiales tenían un borde abrupto con más frecuencia, mientras que los HI mixtos tenían mayor probabilidad de tener un borde progresivo (p<0,05). La mayoría de los HI tenían una superficie lisa. La altura del componente superficial fue mayor en los HI mixtos (p<0,0001).
Características y localizaciones de los hemangiomas infantiles
| Pacientes con HI(n=601) | Pacientes con HI tratados con propranolol(n=72) | Pacientes con HI no tratados con propranolol(n=529) | Valor p (tratados vs. no tratados con propranolol) | Pacientes del ensayo clínico aleatorizado de propranolol17 (n=456) | |
|---|---|---|---|---|---|
| Subtipo morfológico | 0,0009 | ||||
| Localizado | 495 (82%) | 51 (71%) | 444 (84%) | 406 (89%) | |
| Indeterminado | 62 (10%) | 9 (13%) | 53 (10%) | 25 (5,5%) | |
| Segmentario | 34 (6%) | 12 (17%) | 22 (4%) | 25 (5,5%) | |
| Multifocal | 10 (2%) | - | 10 (2%) | - | |
| Subtipo clínico | <0,0001 | Datos no comunicados** | |||
| Superficial | 383 (64%) | 24 (33%) | 359 (68%) | ||
| Mixto – sésil | 121 (20%) | 26 (36%) | 95 (18%) | ||
| Mixto – pedunculado | 28 (5%) | 9 (13%) | 19 (4%) | ||
| Profundo | 43 (7%) | 13 (18%) | 30 (6%) | ||
| Abortivo | 25 (4%) | - | 25 (5%) | ||
| Diámetro máximo (mm)* | 17 (RI: 10-30) | 22 (RI: 14-40) | 15 (RI: 10-25) | 0,0004 | Datos no comunicados |
| Diámetro mínimo (mm)* | 12 (RI: 7-20) | 16.5 (RI:10-30) | 11 (RI: 6-20) | 0,0001 | Datos no comunicados |
| Localización* | <0,0001 | Datos comunicados como faciales (318, 70%) o no faciales (138, 30%) | |||
| Cara | 157 (25%) | 48 (67%) | 109 (21%) | ||
| Cuero cabelludo | 80 (13%) | 6 (8%) | 74 (14%) | ||
| Cuello | 26 (4%) | 3 (4%) | 23 (4%) | ||
| Tronco | 188 (31%) | 10 (14%) | 178 (34%) | ||
| Región lumbosacra | 20 (3%) | 2 (3%) | 18 (3%) | ||
| Genitales | 19 (3%) | 2 (3%) | 17 (3%) | ||
| Nalgas | 16 (3%) | 4 (6%) | 12 (25) | ||
| Piernas | 52 (9%) | 1 (1%) | 51 (10%) | ||
| Brazos | 57 (9%) | 3 (4%) | 54 (10%) |
| Subtipo superficial | Subtipo mixto | Subtipo superficial | Subtipo mixto | Subtipo superficial | Subtipo mixto | |||
|---|---|---|---|---|---|---|---|---|
| Borde del componente superficial* | 0,0395 | Datos no comunicados | ||||||
| Bien definido | 171 (46%) | 52 (37%) | 9 (38%) | 9 (26%) | 162 (47%) | 43 (40%) | ||
| Progresivo | 199 (54%) | 90 (63%) | 15 (62%) | 25 (74%) | 184 (53%) | 65 (60%) | ||
| Superficie del componente superficial* | 0,0020 | Datos no comunicados | ||||||
| Lisa | 249 (68%) | 102 (73%) | 20 (87%) | 26 (87%) | 229 (67%) | 76 (69%) | ||
| En empedrado | 116 (32%) | 38 (27%) | 3 (13%) | 4 (13%) | 113 (33%) | 34 (31%) | ||
| Altura del componente superficial* | 0,0172 | Datos comunicados como ligeros (114, 25%), moderados (148, 33%) o marcados (157, 34%) | ||||||
| <1 mm | 166 (46%) | 53 (38%) | 7 (29%) | 16 (50%) | 159 (48%) | 37 (34%) | ||
| 1-2 mm | 133 (37%) | 43 (31%) | 8 (33%) | 5 (15%) | 125 (38%) | 38 (35%) | ||
| 2-5 mm | 57 (16%) | 29 (20%) | 7 (29%) | 8 (25%) | 50 (15%) | 21 (19%) | ||
| >5 mm | 2 (1%) | 15 (11%) | 2 (8%) | 3 (9%) | - | 12 (11%) |
Las variables continuas se expresan como medianas (percentiles 25-75). Las variables cualitativas se expresan como frecuencias absolutas (relativas). Los valores p estadísticamente significativos figuran en negrita.
La evaluación del color fue rojo brillante en 460 (78%) de los casos, rosa pálido en 84 (14%), escasamente perceptible en 32 (6%) e imperceptible en 11 (2%).
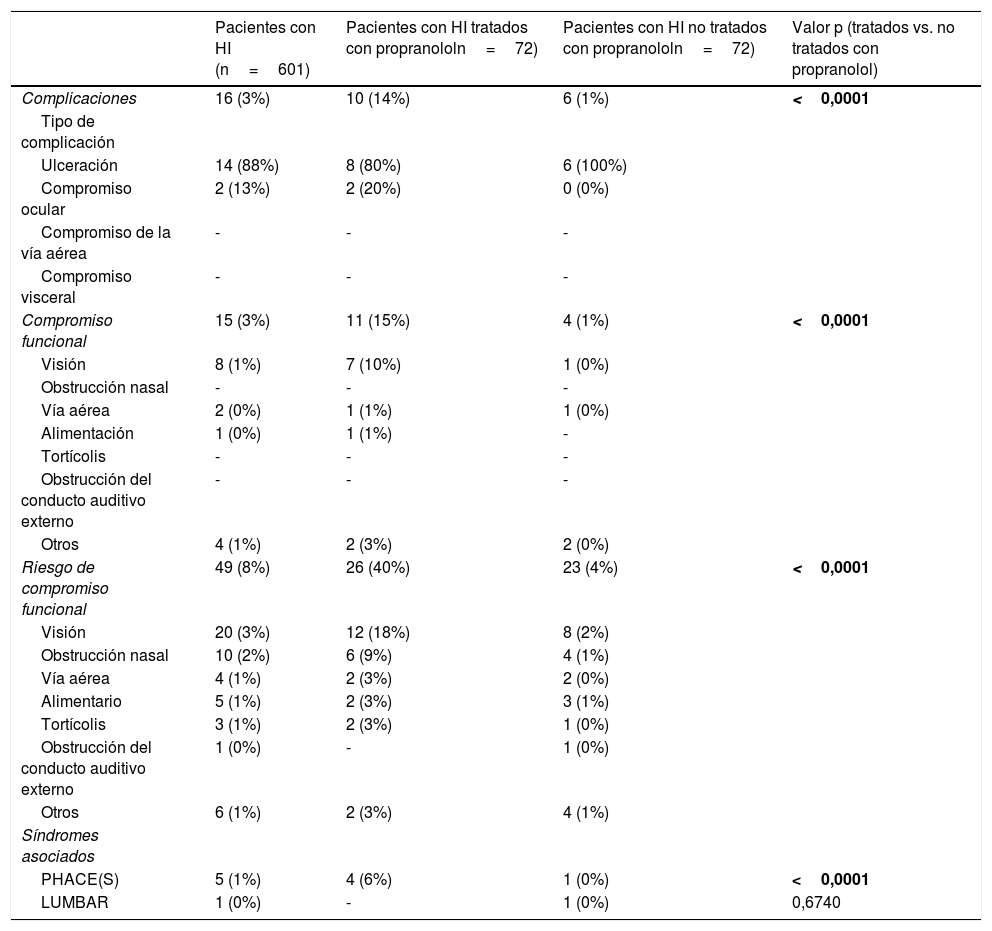
ComplicacionesSolo 16 (3%) pacientes presentaron complicaciones en la visita basal, principalmente ulceraciones, y 15 (3%) presentaron compromiso funcional, principalmente de tipo visual (tabla 3). Cuarenta y nueve (8%) pacientes presentaron riesgo de compromiso funcional, siendo de nuevo la visión la función más comprometida. Cinco (1%) pacientes presentaron síndrome de PHACE, y 1 (0%) paciente presentó síndrome de LUMBAR.
Complicaciones, compromiso funcional, riesgo de compromiso funcional y síndromes asociados al HI
| Pacientes con HI (n=601) | Pacientes con HI tratados con propranololn=72) | Pacientes con HI no tratados con propranololn=72) | Valor p (tratados vs. no tratados con propranolol) | |
|---|---|---|---|---|
| Complicaciones | 16 (3%) | 10 (14%) | 6 (1%) | <0,0001 |
| Tipo de complicación | ||||
| Ulceración | 14 (88%) | 8 (80%) | 6 (100%) | |
| Compromiso ocular | 2 (13%) | 2 (20%) | 0 (0%) | |
| Compromiso de la vía aérea | - | - | - | |
| Compromiso visceral | - | - | - | |
| Compromiso funcional | 15 (3%) | 11 (15%) | 4 (1%) | <0,0001 |
| Visión | 8 (1%) | 7 (10%) | 1 (0%) | |
| Obstrucción nasal | - | - | - | |
| Vía aérea | 2 (0%) | 1 (1%) | 1 (0%) | |
| Alimentación | 1 (0%) | 1 (1%) | - | |
| Tortícolis | - | - | - | |
| Obstrucción del conducto auditivo externo | - | - | - | |
| Otros | 4 (1%) | 2 (3%) | 2 (0%) | |
| Riesgo de compromiso funcional | 49 (8%) | 26 (40%) | 23 (4%) | <0,0001 |
| Visión | 20 (3%) | 12 (18%) | 8 (2%) | |
| Obstrucción nasal | 10 (2%) | 6 (9%) | 4 (1%) | |
| Vía aérea | 4 (1%) | 2 (3%) | 2 (0%) | |
| Alimentario | 5 (1%) | 2 (3%) | 3 (1%) | |
| Tortícolis | 3 (1%) | 2 (3%) | 1 (0%) | |
| Obstrucción del conducto auditivo externo | 1 (0%) | - | 1 (0%) | |
| Otros | 6 (1%) | 2 (3%) | 4 (1%) | |
| Síndromes asociados | ||||
| PHACE(S) | 5 (1%) | 4 (6%) | 1 (0%) | <0,0001 |
| LUMBAR | 1 (0%) | - | 1 (0%) | 0,6740 |
Los datos se expresan como frecuencias absolutas (relativas). Los valores p estadísticamente significativos figuran en negrita.
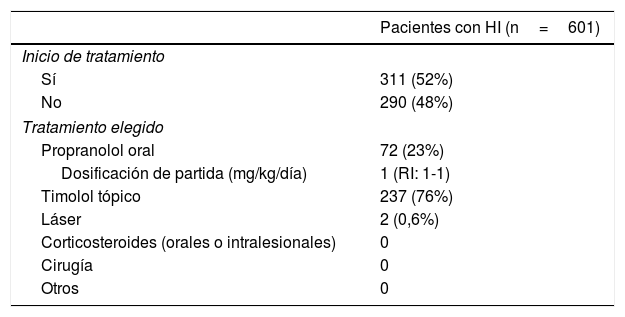
El inicio y los motivos del tratamiento se reflejan en la tabla 4. Algo más del 50% de los pacientes inició tratamiento en la visita basal. De entre estos pacientes, aproximadamente el 75% inició tratamiento con timolol tópico (5mg/ml dos veces al día; se dispuso de datos en el 80% de los casos, pero ya que esta es la posología recomendada en estudios anteriores21, es esperable que esta dosificación fuera usada en la mayoría de los pacientes), y aproximadamente el 25% inició tratamiento con propranolol oral (dosificación inicial mediana: 1mg/kg/día, según las recomendaciones de la Agencia Europea del Medicamento22; se dispuso de datos sobre la dosis de partida en el 76% de los casos, aunque es esperable que esta posología fuera utilizada en la mayoría de los pacientes). Solo dos pacientes iniciaron tratamiento con láser, y no hubo otras terapias.
Inicio del tratamiento y sus causas
| Pacientes con HI (n=601) | |
|---|---|
| Inicio de tratamiento | |
| Sí | 311 (52%) |
| No | 290 (48%) |
| Tratamiento elegido | |
| Propranolol oral | 72 (23%) |
| Dosificación de partida (mg/kg/día) | 1 (RI: 1-1) |
| Timolol tópico | 237 (76%) |
| Láser | 2 (0,6%) |
| Corticosteroides (orales o intralesionales) | 0 |
| Cirugía | 0 |
| Otros | 0 |
| Pacientes con HI que recibieron tratamiento (n=311) | Pacientes con HI tratados con propranolol(n=72) | Pacientes con HI tratados con timolol(n=237) | |
|---|---|---|---|
| Causas del inicio del tratamiento | |||
| Compromiso visual | 21 (6,8%) | 19 (26%) | 2 (0,8%) |
| Hemangioma en el campo visual | 7 (2,3%) | 6 (8,3%) | 1 (0,4%) |
| Cierre palpebral sin oclusión de la pupila | 12 (3,9%) | 11 (15%) | 1 (0,4%) |
| Cierre palpebral con oclusión de la pupila | 1 (0,3%) | 1 (1,4%) | - |
| Compresión del globo ocular sin desviación | 1 (0,3%) | 1 (1,4%) | - |
| Compromiso de la vía aérea | 4 (1,2%) | 4 (5,6%) | - |
| HI de la vía aérea asintomático | 2 (0,6%) | 2 (2,8%) | - |
| HI que causa estridor | 2 (0,6%) | 2 (2,8%) | - |
| Compromiso estético | 199 (64%) | 57 (79%) | 140 (52%) |
| Compromiso bajo | 141 (45%) | 19 (26%) | 121 (51%) |
| Compromiso moderado | 55 (18%) | 35 (49%) | 19 (8%) |
| Compromiso grave | 3 (1%) | 3 (4,2%) | - |
| Ulceración | 13 (4,2%) | 10 (14%) | 1 (0,4%) |
| <10% | 3 (1%) | 2 (2,8%) | 1 (0,4%) |
| 10-25% | 5 (1,6%) | 4 (5,6%) | - |
| 25-50% | 4 (1,3%) | 4 (5,6%) | - |
| >50% | 1 (0,3%) | - | - |
| Dolor | 8 (2,6%) | 6 (8,3%) | - |
| Leve malestar | 3 (1%) | 2 (2,8%) | - |
| El dolor despierta al paciente | 4 (1,3%) | 3 (4,2%) | - |
| Se requiere analgesia | 1 (0,3%) | 1 (1,4%) | |
| Nada de lo anterior o causa no notificada | 103 (33%) | 7 (9,7%) | 96 (41%) |
Las variables continuas se expresan como medianas (percentiles 25-75). Las variables cualitativas se expresan como frecuencias absolutas (relativas).
En términos de características sociodemográficas, una mayor proporción de mujeres inició tratamiento con propranolol (tabla 1). En comparación con el ensayo pivotal, la edad fue similar y la ratio mujer-varón fue superior. Los demás datos no fueron comunicados en el ensayo.
En cuanto a las características de los HI, en los pacientes con HI segmentario, HI mixto y HI profundo, HI con mayor diámetro, mayor altura, borde progresivo, superficie lisa, y HI localizados en la cara fue más frecuente el inicio del tratamiento con propranolol. En comparación con la población del ensayo, se encontraron proporciones superiores de HI indeterminado y HI segmentario tratados con propranolol, y proporciones similares de HI superficial y HI facial. No se comunicaron en el ensayo otros datos acerca de las características de los HI (tabla 2).
Los pacientes con complicaciones, compromiso funcional, o riesgo de compromiso funcional, y aquellos con síndrome PHACE iniciaron el tratamiento con propranolol con mayor frecuencia (tabla 3). En el ensayo no se comunicaron los datos relativos a las complicaciones.
El principal motivo para iniciar tratamiento, tanto con propranolol (79%) como con timolol (52%), fue el compromiso estético (tabla 4). Solo en 47 (66%) pacientes tratados con propranolol y 260 (50%) pacientes no tratados con propranolol se observó un diámetro de los HI superior a 15mm (lo cual era un criterio de inclusión para el ensayo). Los pacientes que iniciaron el tratamiento debido a un compromiso estético tuvieron mayor probabilidad de haber recibido timolol (70%, 140) que propranolol (29%, 57). La información acerca de los motivos de iniciar el tratamiento no fue comunicada en el ensayo clínico.
ComentarioEn este estudio comunicamos las características basales de la cohorte de pacientes con HI de la AEDV. La edad en la primera visita fue de aproximadamente cuatro meses y la mayoría de los HI fueron localizados, superficiales y ubicados en tronco y cara. Observamos que el compromiso estético fue el principal motivo de inicio del tratamiento, y que timolol fue el tratamiento más frecuentemente utilizado en la práctica clínica diaria en España, mientras que el propranolol se reserva para los HI con complicaciones o para los HI de alto riesgo. Las características de los pacientes que recibieron propranolol en práctica clínica habitual se asemejan en diversos aspectos a aquellas del ensayo clínico, aunque existieron diferencias.
Características demográficas y clínicas de la cohorte de la AEDVLa edad en la visita basal de nuestra cohorte fue similar a la de los diversos estudios publicados desde el primer uso del propranolol18,23, comunicado por primera vez como tratamiento de los HI en 200824, e inferior a la edad comunicada en los estudios realizados previamente19,25. Este hallazgo podría reflejar el incremento de capacitación y formación de los facultativos de atención primaria, reflejado en una mayor precisión diagnóstica y una derivación a los dermatólogos más rápida. Sin embargo, los pacientes siguen siendo valorados con cierto retraso por los dermatólogos, dado que muchos HI aparecen aproximadamente a las dos semanas de edad, y que la etapa de mayor crecimiento se produce durante el segundo mes de vida1. Otras características demográficas, tales como la ratio de sexo, el peso al nacer o la edad gestacional fueron similares a las comunicadas en estudios previos18,26,27.
El subtipo morfológico más frecuente fue el localizado, tal y como ha sido comunicado previamente28,29. Se ha notificado mayor incidencia de secuelas y de peores resultados estéticos en los HI superficiales y mixtos, así como en los HI con borde abrupto14,15,18. En comparación con estos estudios, en nuestra cohorte observamos una mayor proporción de HI superficiales y una menor proporción de HI mixtos. La prevalencia de la superficie en empedrado, que ha sido asociada a anetoderma15, fue similar entre los HI superficiales y los HI mixtos.
El tamaño mediano de los HI de nuestra muestra fue menor que el comunicado por Chamlin et al. en 200712, lo cual podría reflejar también una detección y una consulta dermatológica de los HI más tempranas. En cuanto a la localización, la cara y el tronco fueron las zonas más frecuentemente afectadas.
La proporción de pacientes con HI en nuestra muestra, que sufrieron ulceración u otras complicaciones, fue inferior a la comunicada previamente al uso de propanolol12,26. Estas diferencias pueden deberse a la efectividad del tratamiento, pero también a la exclusión de los pacientes que ya habían iniciado el tratamiento en el momento de la visita basal en nuestro estudio. La visión fue la función más frecuentemente afectada, ya que la localización periorbital es relativamente común16.
Enfoque terapéuticoMás del 50% de los pacientes inició el tratamiento en la visita basal. El rápido incremento del uso de betabloqueantes para el tratamiento de los HI ha originado una mayor proporción de pacientes que reciben terapias, en comparación con lo anteriormente comunicado27. El principal motivo de iniciar el tratamiento fue el compromiso estético. El timolol fue el tratamiento más frecuente. Este fármaco tiene una tasa de respuesta similar a la de propranolol, y superior al láser y a la observación, con arreglo a un metaanálisis reciente21. Sin embargo, no existen ensayos clínicos que valoren su efectividad, y actualmente se usa fuera de ficha técnica. La presencia de complicaciones en los HI fue un motivo importante para iniciar el tratamiento con propranolol, aunque el principal motivo, como en el caso de timolol, fue el compromiso estético. Las pacientes femeninas y aquellos pacientes con HI segmentarios (que están asociados a ulceración y complicaciones7,12,28), con HI mixtos o profundos, HI de mayor altura y tamaño, o HI localizados en la cara, fueron más propensos a recibir propranolol. Sin embargo, los HI superficiales, HI con borde abrupto, y HI con superficie en empedrado, que son factores relacionados con peores resultados estéticos14,15,18, fueron tratados menos frecuentemente con propranolol. Un hecho destacable es que 4 de los 5 pacientes con síndrome de PHACE recibieron propranolol, ya que actualmente se considera un tratamiento seguro en ausencia de arteriopatías graves30,31. Los dos pacientes que no recibieron tratamiento con betabloqueantes tenían HI ulcerados, y recibieron en cambio tratamiento con láser.
Comparación con el ensayo clínicoEl uso de propranolol se basa principalmente en los resultados de un ensayo clínico17, aunque los criterios restrictivos de elegibilidad podrían limitar la generalización de sus resultados. Los pacientes elegibles tenían de 35 a 150 días de edad, con un HI proliferativo que requiría terapia sistémica, con un diámetro mayor de al menos 15mm. Los criterios de exclusión eran, entre otros, los HI en el área del pañal, HI con amenaza funcional, HI ulcerados con falta de respuesta a curas simples, pacientes que habían recibido previamente tratamiento, HI con diagnóstico clínicamente incierto (particularmente lesiones subdérmicas) o pacientes nacidos pretérmino que no habían alcanzado aún la edad equivalente al término.
En nuestro estudio, la edad de los pacientes que iniciaron tratamiento con propranolol en la visita basal fue similar a la de los pacientes del ensayo clínico, mientras que la ratio mujer-varón fue superior (3.5:1 vs. 2.5:1). El resto de características demográficas no se comunicaron en el ensayo. En comparación con el ensayo clínico, la proporción de HI localizados fue inferior, la de HI indeterminados y segmentarios superior, y la de HI superficiales similar. El tamaño no fue notificado en el ensayo, aunque el tamaño mínimo para cumplir los criterios de inclusión fue de 15mm, como hemos comentado anteriormente. En nuestra cohorte, solo 47 (66%) pacientes tratados con propranolol tenían un HI con diámetro superior a 15mm. La proporción de afectación facial/no facial fue similar. En el ensayo clínico, el componente superficial se definió únicamente como plano o elevado, y la última categoría se subdividió entre ligero, moderado y marcado, lo cual dificulta la comparación con nuestros resultados. Los datos acerca de otras características, complicaciones y causas del inicio del tratamiento de los HI no fueron comunicados en el ensayo clínico, lo cual limita la comparación de los datos. Por tanto, aunque 1/3 de nuestros pacientes no habrían sido incluidos en el ensayo debido al tamaño de su HI y aunque la proporción de HI segmentarios (relacionado con peores resultados) es superior, parece que propranolol está siendo utilizado en una población general similar a la del ensayo, aunque esta afirmación no puede confirmarse definitivamente debido a la carencia de datos.
Fortalezas y limitacionesLa principal fortaleza de este estudio es que se trata de una de las mayores cohortes prospectivas de pacientes con HI tras la comercialización de propranolol, y es probable que sea representativa de las características y terapias actuales de los HI en la práctica clínica. La principal limitación de nuestro estudio es la exclusión de aquellos pacientes que ya recibían tratamiento en el momento de la visita basal, lo cual podría haber originado un sesgo de selección. Sin embargo, como la principal variable de resultado del estudio será la comparación ciega del resultado estético entre las fotografías estandarizadas obtenidas en la visita basal, previamente al inicio del tratamiento (o la observación clínica) y las obtenidas al final del periodo de seguimiento de cinco años, la disponibilidad de una foto previa al inicio del tratamiento se consideró necesaria para la inclusión.
ConclusionesEn conclusión, hemos presentado las características basales de la cohorte española de pacientes con HI. Algunos datos, tales como la edad en el momento de la consulta, y el tamaño de los HI, reflejan un nuevo escenario para esta enfermedad, con médicos más formados y con más interés sobre los HI. Aproximadamente el 50% de los pacientes no recibieron tratamiento. El timolol tópico es el tratamiento más frecuente, siendo el compromiso estético el motivo principal para iniciar el tratamiento, aunque no existen ensayos clínicos que evalúen sus resultados, y se usa fuera de ficha técnica. El motivo más importante para iniciar tratamiento con propranolol es el compromiso estético, siendo otro motivo principal la presencia de complicaciones. En este grupo de edad, el resto de terapias tales como el uso de láser o corticosteroides, son actualmente anecdóticas. Dado que el compromiso estético es el motivo principal para iniciar el tratamiento, existe la necesidad de conocer mejor los resultados estéticos de las diferentes terapias. También existe la necesidad de incrementar la evidencia sobre el uso del timolol, el cual, incluso utilizándose fuera de ficha técnica, es actualmente la terapia más común para los HI. Algunas características de los pacientes y HI tratados con propranolol son similares a las del ensayo clínico pivotal, a pesar incluso de sus criterios de elegibilidad restrictivos. Sin embargo, esta afirmación no puede confirmarse de manera definitiva, ya que 1/3 de los HI observados en la práctica clínica rutinaria no alcanzó el diámetro mínimo para cumplir los criterios de inclusión del ensayo, y en el estudio original no se reportó información pronóstica importante, como el tamaño de los HI, el tipo del componente superficial, el tipo de borde, las localizaciones concretas, las complicaciones, o los motivos del inicio del tratamiento.
FinanciaciónEl estudio ha sido financiado por la Fundación Piel Sana AEDV.
Conflicto de interesesLa Dra. Baselga-Torres reporta la recepción de honorarios personales y otros recibidos de Pierre Fabre, y Venthera, durante la realización del estudio. Además, la Dra. Baselga-Torres está pendiente de patente para los inhibidores tópicos de PIK3CA para las malformaciones venosas. La Dra. Vicente reporta la recepción de honorarios de Pierre Fabre durante la realización del estudio; además de recibir honorarios de Pfizer, Lilly, Novartis, Cellgene, Amryt Pharma y Sanofi, ajenos al trabajo realizado. El resto de los autores declaran no tener ningún conflicto de intereses.
Quisiéramos agradecer a Miguel Ángel Descalzo-Gallego su valiosa contribución al desarrollo de esta investigación.