El penfigoide ampolloso (PA) es una enfermedad cutánea autoinmune que afecta generalmente a personas de edad avanzada. El tratamiento clásico con corticoides sistémicos e inmunosupresores se asocia a múltiples efectos adversos, lo que dificulta el cumplimiento terapéutico en este grupo de edad, donde las comorbilidades asociadas son frecuentes. Dupilumab se ha posicionado recientemente como un tratamiento eficaz para el PA refractario, con un perfil de seguridad superior a las alternativas tradicionales.
Se realizó un estudio observacional descriptivo retrospectivo, donde se incluyeron todos los casos de PA tratados con dupilumab en nuestro hospital desde octubre de 2019 hasta octubre de 2023.
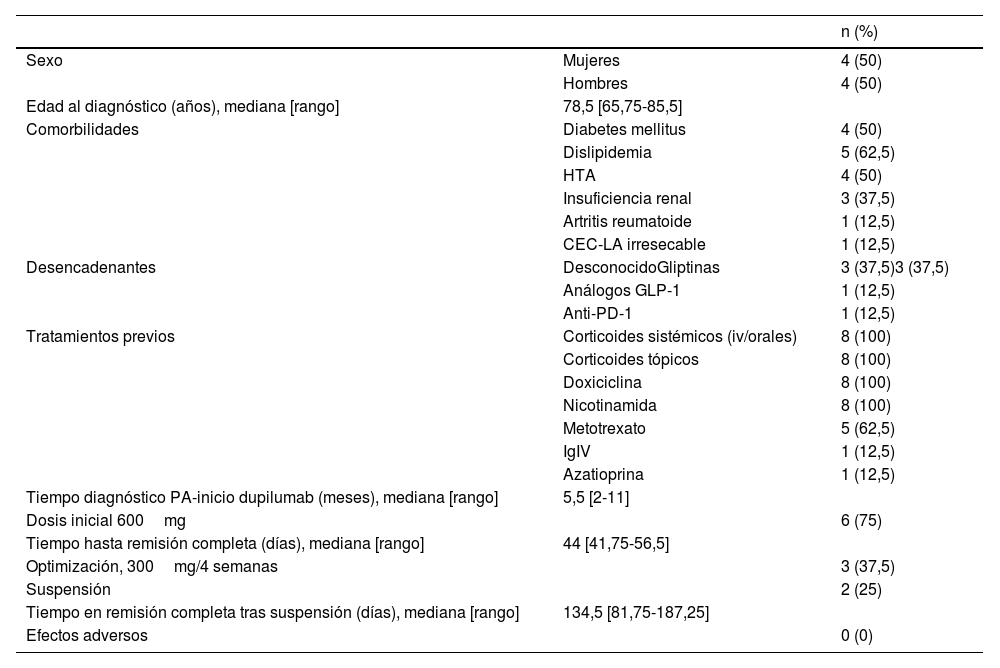
Se incluyó un total de 8 pacientes (tabla 1). La mediana de edad al diagnóstico fue de 78,5 años [65,75-85,5]. Entre los antecedentes personales destacaron diabetes mellitus (62,5%), hipertensión arterial (50%), dislipidemia (50%), insuficiencia renal (37,5%), artritis reumatoide (12,5%) y carcinoma epidermoide cutáneo localmente avanzado en la mano, no candidato a cirugía ni a radioterapia (12,5%). En 5 pacientes (62,5%) se identificó un fármaco desencadenante: gliptinas (37,5%), análogos del GLP-1 (12,5%) y anti-PD1 (12,5%). Respecto a los tratamientos previos, los más frecuentes fueron: corticoides sistémicos y tópicos (100%), doxiciclina (100%), nicotinamida (100%), metotrexato (62,5%), inmunoglobulinas intravenosas (12,5%) y azatioprina (12,5%). La posología habitual de dupilumab fue de 300mg cada 2 semanas. Todos los pacientes alcanzaron una remisión completa tras una mediana de 44 días [41,75-56,5] desde el inicio de dupilumab. En 3 (37,5%) pacientes se optimizó la pauta a 300mg cada 4 semanas por buen control clínico, manteniendo la respuesta. En 2 pacientes (25%) se suspendió el fármaco por ausencia de lesiones, sin recidiva tras una mediana de 134,5 [81,75-187,25] días de seguimiento. Ningún efecto adverso fue notificado en nuestro estudio.
Resultados de estudio monocéntrico con dupilumab en penfigoide ampolloso
| n (%) | ||
|---|---|---|
| Sexo | Mujeres | 4 (50) |
| Hombres | 4 (50) | |
| Edad al diagnóstico (años), mediana [rango] | 78,5 [65,75-85,5] | |
| Comorbilidades | Diabetes mellitus | 4 (50) |
| Dislipidemia | 5 (62,5) | |
| HTA | 4 (50) | |
| Insuficiencia renal | 3 (37,5) | |
| Artritis reumatoide | 1 (12,5) | |
| CEC-LA irresecable | 1 (12,5) | |
| Desencadenantes | DesconocidoGliptinas | 3 (37,5)3 (37,5) |
| Análogos GLP-1 | 1 (12,5) | |
| Anti-PD-1 | 1 (12,5) | |
| Tratamientos previos | Corticoides sistémicos (iv/orales) | 8 (100) |
| Corticoides tópicos | 8 (100) | |
| Doxiciclina | 8 (100) | |
| Nicotinamida | 8 (100) | |
| Metotrexato | 5 (62,5) | |
| IgIV | 1 (12,5) | |
| Azatioprina | 1 (12,5) | |
| Tiempo diagnóstico PA-inicio dupilumab (meses), mediana [rango] | 5,5 [2-11] | |
| Dosis inicial 600mg | 6 (75) | |
| Tiempo hasta remisión completa (días), mediana [rango] | 44 [41,75-56,5] | |
| Optimización, 300mg/4 semanas | 3 (37,5) | |
| Suspensión | 2 (25) | |
| Tiempo en remisión completa tras suspensión (días), mediana [rango] | 134,5 [81,75-187,25] | |
| Efectos adversos | 0 (0) |
CEC-LA: carcinoma epidermoide cutáneo localmente avanzado; GLP-1: péptido sumilar al glucagón tipo 1; HTA: hipertensión arterial; IgIV: inmunoglobulinas intravenosas; PA: penfigoide ampolloso.
El PA es una de las enfermedades ampollosas autoinmunes más frecuentes. Se caracteriza por la formación de ampollas subepidérmicas tras la unión de autoanticuerpos circulantes contra los antígenos BP180 o BP230 presentes en la membrana basal dermoepidérmica. El PA afecta típicamente a pacientes mayores de 70 años (la mediana de edad en nuestra serie fue de 78,5 años)1. Numerosos fármacos se han asociado al desarrollo de PA, siendo los más frecuentes antidiabéticos orales del grupo de las gliptinas, como en nuestro caso. Recientemente se ha descrito un aumento de PA asociado a inmunoterapia con inhibidores de PD-1 o PDL-1, utilizados en dermatología para el tratamiento de cáncer cutáneo avanzado2. En nuestra serie se notificó un caso desencadenado por cemiplimab (anti-PD-1), pautado por un carcinoma epidermoide cutáneo localmente avanzado en el dorso de la mano, no candidato a cirugía ni a radioterapia, con buen control tras el inicio de dupilumab, sin precisar la suspensión de la inmunoterapia. Actualmente las principales opciones de tratamiento se basan en la supresión inespecífica de la inflamación, siendo los corticoides tópicos y sistémicos la primera línea. Su empleo puede estar limitado por comorbilidades como la diabetes mellitus, muy prevalente en personas de edad avanzada (en nuestra serie, presente en el 50% de los pacientes)3. En casos refractarios se pautan inmunosupresores clásicos como metotrexato, cuyo uso debe ajustarse a la función renal, aumentando la incidencia de insuficiencia renal en este grupo de edad (se observó en el 37,5% de nuestros pacientes)4. Recientemente se ha notificado en la patogenia del PA un aumento de las citocinas proinflamatorias de fenotipo Th2 como IL-4, IL-5, IL-13 e IL-31, que pueden seleccionar eosinófilos, otras células inflamatorias y promover la secreción de IgE5. Además, citocinas como IL-4 e IL-31 pueden sensibilizar los nervios periféricos provocando prurito. Dupilumab es un anticuerpo monoclonal dirigido contra la subunidad del receptor alfa de la IL-4 que inhibe la señalización de IL-4 e IL-13, inhibiendo así la respuesta inflamatoria, reduciendo el prurito y previniendo la progresión de la enfermedad6. La pauta habitual de dupilumab es de 300mg cada 2 semanas, pudiendo administrar una dosis inicial de 600mg. En nuestro estudio, el 75% de los pacientes recibieron 600mg al inicio, seguidos de 300mg cada 2 semanas, pudiendo optimizar el tratamiento a 300mg cada 4 semanas en el 37,5% de los casos, manteniendo la respuesta clínica. Se suspendió en el 25% de los pacientes por ausencia de lesiones, persistiendo la remisión completa actualmente tras una mediana de 134,5 días de seguimiento. Actualmente, dupilumab no está aprobado para el tratamiento del PA, pero se muestra como una alternativa con un gran perfil de seguridad y eficacia7–9.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.