Los inhibidores del punto de control inmunitario (CI), utilizados para potenciar el sistema inmune, han mejorado sustancialmente el pronóstico de los pacientes con melanoma avanzado1,2. Sin embargo, están asociados a un único espectro de efectos secundarios: efectos adversos inmunomediados (IRAE), que son importantes de reconocer y tratar de inmediato3. A pesar de los ensayos clínicos relacionados con los IRAE, seguimos careciendo de comparación en la vida real entre los IRAE, cuando se utilizan los CI en la enfermedad metastásica (EM) o como terapia adyuvante (TA). Por tanto, realizamos un estudio de cohorte retrospectivo y observacional para evaluar la frecuencia, tipo y severidad de los IRAE en los pacientes con melanoma que recibieron TA, en comparación con aquellos que recibieron un régimen para EM (REM). Además, exploramos cualquier factor clínico relacionado con la aparición de IRAE o la correlación entre tratamiento y efectividad. Incluimos a todos los pacientes con melanoma tratados con un régimen estándar de CI en condiciones de la práctica diaria durante al menos 3 meses.
Nuestra cohorte incluyó 49 pacientes tratados con nivolumab (n=23), pembrolizumab (16), ipilimumab (n=8) o ipilimumab+nivolumab (n=2). Las características basales se incluyen en la tabla 1. De entre ellos, el 51,9% (n=27) siguieron TA y el 42,3% (n=22) REM. Encontramos que el 46,9% de los pacientes experimentó un IRAE. Normalmente estos tenían intensidad de leve a moderada, siendo severos (grado 3 de los criterios terminológicos comunes para efectos adversos3) en el 18,2% de los pacientes, resolviéndose la mayoría con corticosteroides tópicos/orales (tabla 1). Al comparar TA y REM, la frecuencia de los IRAE, el tipo o el manejo fueron similares en ambos grupos (tabla 1). La severidad de los IRAE difirió estadísticamente, con menor puntuación en el grupo TA. Estos datos podrían tener importancia a la hora de decidir la iniciación del tratamiento en un contexto diferente al del estadio III al que nos enfrentamos en la práctica clínica. Los IRAE causaron la discontinuación del tratamiento en 4 pacientes (n=1, TA; n=3, REM) no reportándose muertes relacionadas con los CI. En términos de progresión de la enfermedad, los pacientes con IRAE tuvieron menor probabilidad de progresar, y reflejaron una supervivencia libre de enfermedad más prolongada. Por último, la ulceración del melanoma guardó también relación con un número más elevado de IRAE (tablas 1 y 2 tabla 2). La ulceración es una entidad biológica, habiendo identificado los investigadores a lo largo de los años diversas características vinculadas al fenotipo ulcerado del melanoma tales como: incremento de la vascularidad tumoral, pérdida de adhesión celular, así como incremento de la densidad de diversas células inmunitarias y neutrófilos que se infiltran en el tumor, células dendríticas, macrófagos e incremento del número de células tumorales positivas PD-L1. Esto podría explicar la respuesta más fuerte al tratamiento con interferón alfa en este subconjunto de melanoma, pudiendo contribuir a una mayor tasa de IRAE4–6. Como se ha publicado previamente, este análisis reveló que la primera aparición de la mayoría de IRAE tuvo lugar al principio del tratamiento (tabla 2)4,5. De igual modo, los efectos más frecuentemente reportados fueron de tipo dermatológico, endocrino, gastrointestinal y hepático (tabla 1)3.
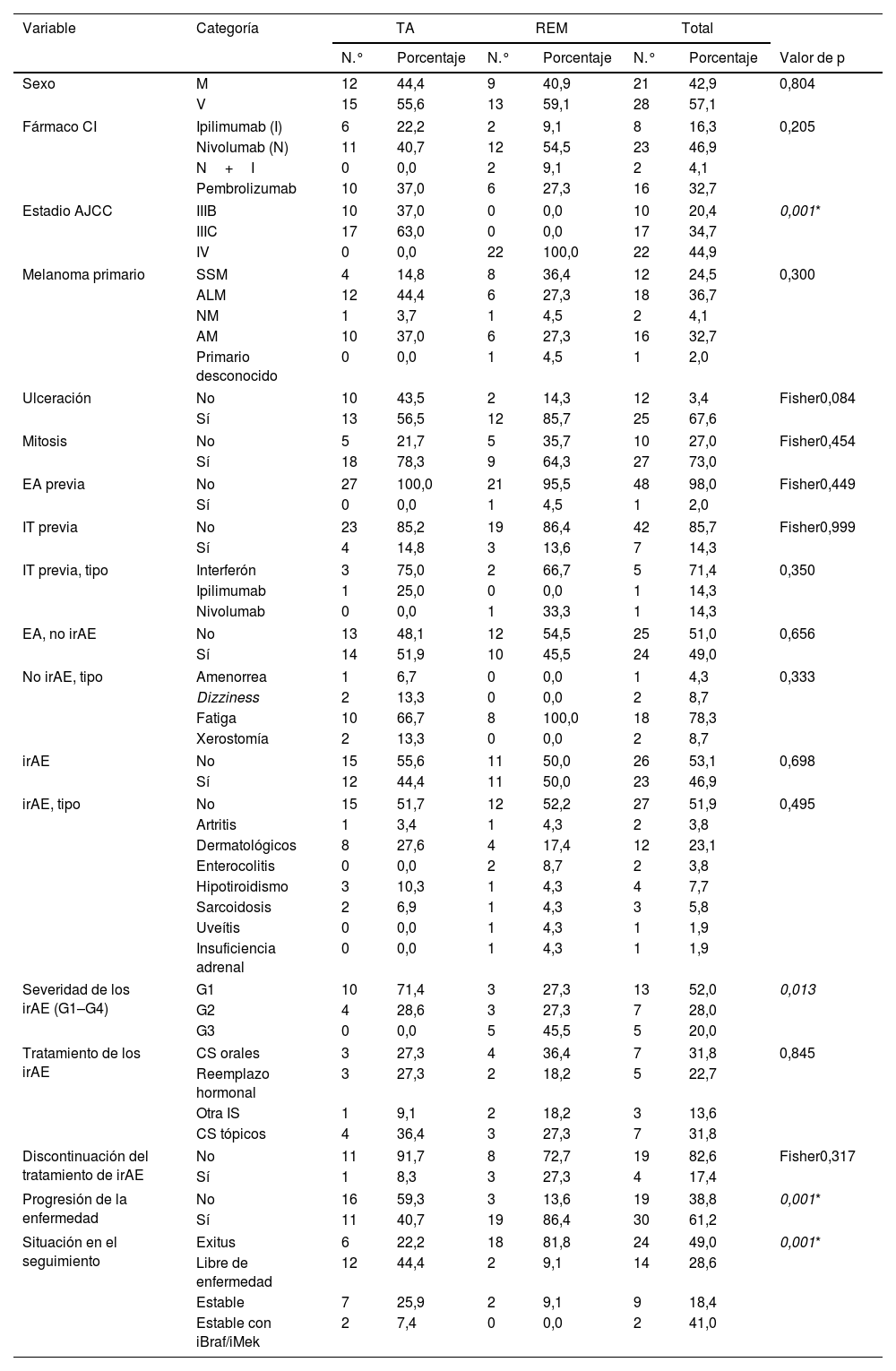
Características basales de los pacientes. Comparación entre grupos de pacientes en terapia adyuvante o regímenes de enfermedad metastásica
| Variable | Categoría | TA | REM | Total | ||||
|---|---|---|---|---|---|---|---|---|
| N.° | Porcentaje | N.° | Porcentaje | N.° | Porcentaje | Valor de p | ||
| Sexo | M | 12 | 44,4 | 9 | 40,9 | 21 | 42,9 | 0,804 |
| V | 15 | 55,6 | 13 | 59,1 | 28 | 57,1 | ||
| Fármaco CI | Ipilimumab (I) | 6 | 22,2 | 2 | 9,1 | 8 | 16,3 | 0,205 |
| Nivolumab (N) | 11 | 40,7 | 12 | 54,5 | 23 | 46,9 | ||
| N+I | 0 | 0,0 | 2 | 9,1 | 2 | 4,1 | ||
| Pembrolizumab | 10 | 37,0 | 6 | 27,3 | 16 | 32,7 | ||
| Estadio AJCC | IIIB | 10 | 37,0 | 0 | 0,0 | 10 | 20,4 | 0,001* |
| IIIC | 17 | 63,0 | 0 | 0,0 | 17 | 34,7 | ||
| IV | 0 | 0,0 | 22 | 100,0 | 22 | 44,9 | ||
| Melanoma primario | SSM | 4 | 14,8 | 8 | 36,4 | 12 | 24,5 | 0,300 |
| ALM | 12 | 44,4 | 6 | 27,3 | 18 | 36,7 | ||
| NM | 1 | 3,7 | 1 | 4,5 | 2 | 4,1 | ||
| AM | 10 | 37,0 | 6 | 27,3 | 16 | 32,7 | ||
| Primario desconocido | 0 | 0,0 | 1 | 4,5 | 1 | 2,0 | ||
| Ulceración | No | 10 | 43,5 | 2 | 14,3 | 12 | 3,4 | Fisher0,084 |
| Sí | 13 | 56,5 | 12 | 85,7 | 25 | 67,6 | ||
| Mitosis | No | 5 | 21,7 | 5 | 35,7 | 10 | 27,0 | Fisher0,454 |
| Sí | 18 | 78,3 | 9 | 64,3 | 27 | 73,0 | ||
| EA previa | No | 27 | 100,0 | 21 | 95,5 | 48 | 98,0 | Fisher0,449 |
| Sí | 0 | 0,0 | 1 | 4,5 | 1 | 2,0 | ||
| IT previa | No | 23 | 85,2 | 19 | 86,4 | 42 | 85,7 | Fisher0,999 |
| Sí | 4 | 14,8 | 3 | 13,6 | 7 | 14,3 | ||
| IT previa, tipo | Interferón | 3 | 75,0 | 2 | 66,7 | 5 | 71,4 | 0,350 |
| Ipilimumab | 1 | 25,0 | 0 | 0,0 | 1 | 14,3 | ||
| Nivolumab | 0 | 0,0 | 1 | 33,3 | 1 | 14,3 | ||
| EA, no irAE | No | 13 | 48,1 | 12 | 54,5 | 25 | 51,0 | 0,656 |
| Sí | 14 | 51,9 | 10 | 45,5 | 24 | 49,0 | ||
| No irAE, tipo | Amenorrea | 1 | 6,7 | 0 | 0,0 | 1 | 4,3 | 0,333 |
| Dizziness | 2 | 13,3 | 0 | 0,0 | 2 | 8,7 | ||
| Fatiga | 10 | 66,7 | 8 | 100,0 | 18 | 78,3 | ||
| Xerostomía | 2 | 13,3 | 0 | 0,0 | 2 | 8,7 | ||
| irAE | No | 15 | 55,6 | 11 | 50,0 | 26 | 53,1 | 0,698 |
| Sí | 12 | 44,4 | 11 | 50,0 | 23 | 46,9 | ||
| irAE, tipo | No | 15 | 51,7 | 12 | 52,2 | 27 | 51,9 | 0,495 |
| Artritis | 1 | 3,4 | 1 | 4,3 | 2 | 3,8 | ||
| Dermatológicos | 8 | 27,6 | 4 | 17,4 | 12 | 23,1 | ||
| Enterocolitis | 0 | 0,0 | 2 | 8,7 | 2 | 3,8 | ||
| Hipotiroidismo | 3 | 10,3 | 1 | 4,3 | 4 | 7,7 | ||
| Sarcoidosis | 2 | 6,9 | 1 | 4,3 | 3 | 5,8 | ||
| Uveítis | 0 | 0,0 | 1 | 4,3 | 1 | 1,9 | ||
| Insuficiencia adrenal | 0 | 0,0 | 1 | 4,3 | 1 | 1,9 | ||
| Severidad de los irAE (G1–G4) | G1 | 10 | 71,4 | 3 | 27,3 | 13 | 52,0 | 0,013 |
| G2 | 4 | 28,6 | 3 | 27,3 | 7 | 28,0 | ||
| G3 | 0 | 0,0 | 5 | 45,5 | 5 | 20,0 | ||
| Tratamiento de los irAE | CS orales | 3 | 27,3 | 4 | 36,4 | 7 | 31,8 | 0,845 |
| Reemplazo hormonal | 3 | 27,3 | 2 | 18,2 | 5 | 22,7 | ||
| Otra IS | 1 | 9,1 | 2 | 18,2 | 3 | 13,6 | ||
| CS tópicos | 4 | 36,4 | 3 | 27,3 | 7 | 31,8 | ||
| Discontinuación del tratamiento de irAE | No | 11 | 91,7 | 8 | 72,7 | 19 | 82,6 | Fisher0,317 |
| Sí | 1 | 8,3 | 3 | 27,3 | 4 | 17,4 | ||
| Progresión de la enfermedad | No | 16 | 59,3 | 3 | 13,6 | 19 | 38,8 | 0,001* |
| Sí | 11 | 40,7 | 19 | 86,4 | 30 | 61,2 | ||
| Situación en el seguimiento | Exitus | 6 | 22,2 | 18 | 81,8 | 24 | 49,0 | 0,001* |
| Libre de enfermedad | 12 | 44,4 | 2 | 9,1 | 14 | 28,6 | ||
| Estable | 7 | 25,9 | 2 | 9,1 | 9 | 18,4 | ||
| Estable con iBraf/iMek | 2 | 7,4 | 0 | 0,0 | 2 | 41,0 | ||
A menos que se exprese lo contrario, las pruebas Chi-cuadrado (χ2) de independencia se realizan para las variables cualitativas, y las pruebas t de Student para las cuantitativas.
AE: efectos adversos; ALM: melanoma lentiginoso acral; AM: melanoma amelanótico; CI: inhibidores del punto de control; CS: corticosteroides; EA: enfermedad autoinmune; G: grado; irAE: efecto adverso inmunomediado; IS: inmunosupresión; IT: inmunoterapia; M: mujer; MDR: regímenes de enfermedad metastásica; n: número de pacientes; NM: melanoma nodular; SSM: melanoma de extensión superficial; TA: terapia adyuvante; V: varón.
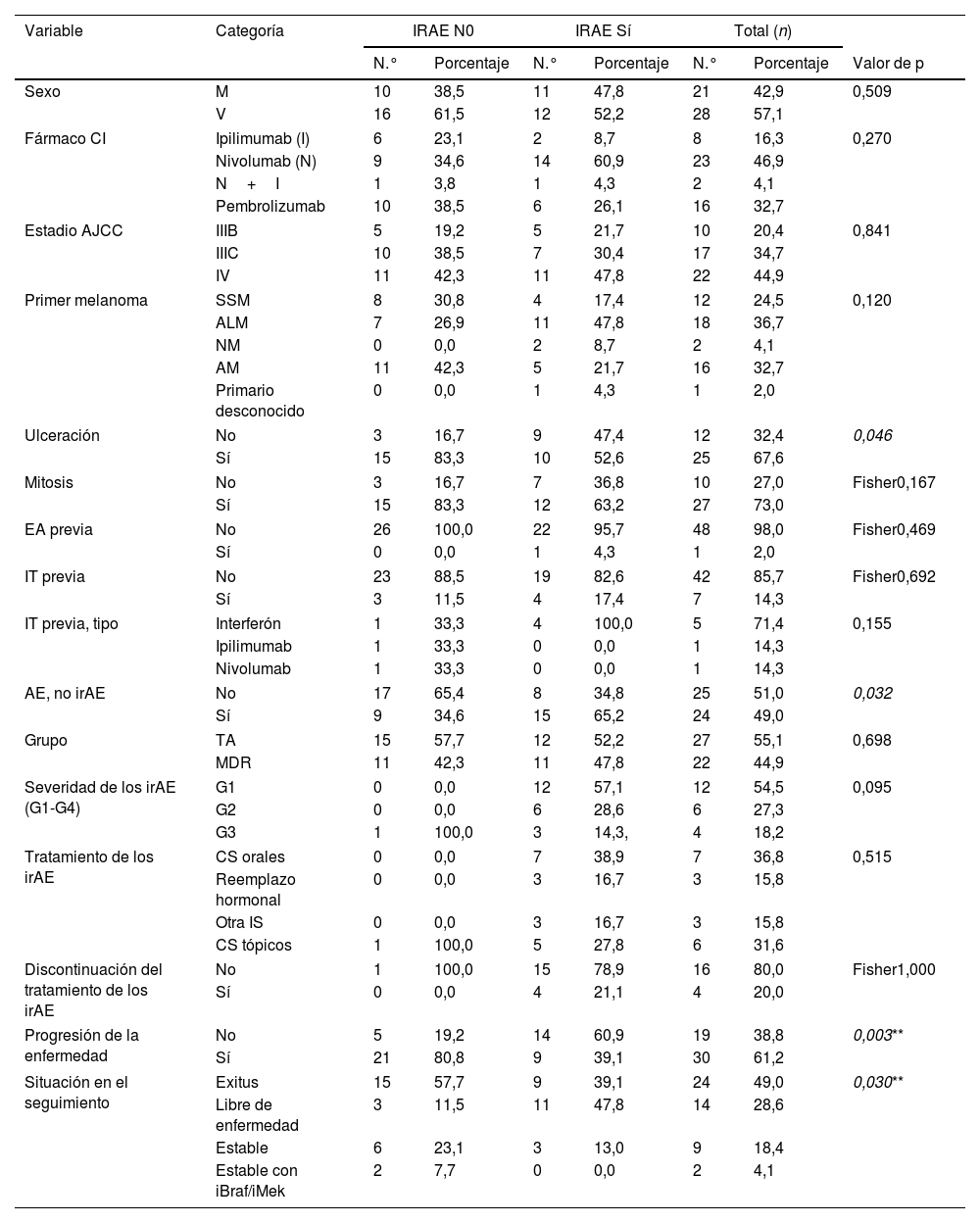
Comparación entre los grupos de pacientes que tuvieron/no tuvieron efectos adversos relacionados con la respuesta inmune
| Variable | Categoría | IRAE N0 | IRAE Sí | Total (n) | ||||
|---|---|---|---|---|---|---|---|---|
| N.° | Porcentaje | N.° | Porcentaje | N.° | Porcentaje | Valor de p | ||
| Sexo | M | 10 | 38,5 | 11 | 47,8 | 21 | 42,9 | 0,509 |
| V | 16 | 61,5 | 12 | 52,2 | 28 | 57,1 | ||
| Fármaco CI | Ipilimumab (I) | 6 | 23,1 | 2 | 8,7 | 8 | 16,3 | 0,270 |
| Nivolumab (N) | 9 | 34,6 | 14 | 60,9 | 23 | 46,9 | ||
| N+I | 1 | 3,8 | 1 | 4,3 | 2 | 4,1 | ||
| Pembrolizumab | 10 | 38,5 | 6 | 26,1 | 16 | 32,7 | ||
| Estadio AJCC | IIIB | 5 | 19,2 | 5 | 21,7 | 10 | 20,4 | 0,841 |
| IIIC | 10 | 38,5 | 7 | 30,4 | 17 | 34,7 | ||
| IV | 11 | 42,3 | 11 | 47,8 | 22 | 44,9 | ||
| Primer melanoma | SSM | 8 | 30,8 | 4 | 17,4 | 12 | 24,5 | 0,120 |
| ALM | 7 | 26,9 | 11 | 47,8 | 18 | 36,7 | ||
| NM | 0 | 0,0 | 2 | 8,7 | 2 | 4,1 | ||
| AM | 11 | 42,3 | 5 | 21,7 | 16 | 32,7 | ||
| Primario desconocido | 0 | 0,0 | 1 | 4,3 | 1 | 2,0 | ||
| Ulceración | No | 3 | 16,7 | 9 | 47,4 | 12 | 32,4 | 0,046 |
| Sí | 15 | 83,3 | 10 | 52,6 | 25 | 67,6 | ||
| Mitosis | No | 3 | 16,7 | 7 | 36,8 | 10 | 27,0 | Fisher0,167 |
| Sí | 15 | 83,3 | 12 | 63,2 | 27 | 73,0 | ||
| EA previa | No | 26 | 100,0 | 22 | 95,7 | 48 | 98,0 | Fisher0,469 |
| Sí | 0 | 0,0 | 1 | 4,3 | 1 | 2,0 | ||
| IT previa | No | 23 | 88,5 | 19 | 82,6 | 42 | 85,7 | Fisher0,692 |
| Sí | 3 | 11,5 | 4 | 17,4 | 7 | 14,3 | ||
| IT previa, tipo | Interferón | 1 | 33,3 | 4 | 100,0 | 5 | 71,4 | 0,155 |
| Ipilimumab | 1 | 33,3 | 0 | 0,0 | 1 | 14,3 | ||
| Nivolumab | 1 | 33,3 | 0 | 0,0 | 1 | 14,3 | ||
| AE, no irAE | No | 17 | 65,4 | 8 | 34,8 | 25 | 51,0 | 0,032 |
| Sí | 9 | 34,6 | 15 | 65,2 | 24 | 49,0 | ||
| Grupo | TA | 15 | 57,7 | 12 | 52,2 | 27 | 55,1 | 0,698 |
| MDR | 11 | 42,3 | 11 | 47,8 | 22 | 44,9 | ||
| Severidad de los irAE (G1-G4) | G1 | 0 | 0,0 | 12 | 57,1 | 12 | 54,5 | 0,095 |
| G2 | 0 | 0,0 | 6 | 28,6 | 6 | 27,3 | ||
| G3 | 1 | 100,0 | 3 | 14,3, | 4 | 18,2 | ||
| Tratamiento de los irAE | CS orales | 0 | 0,0 | 7 | 38,9 | 7 | 36,8 | 0,515 |
| Reemplazo hormonal | 0 | 0,0 | 3 | 16,7 | 3 | 15,8 | ||
| Otra IS | 0 | 0,0 | 3 | 16,7 | 3 | 15,8 | ||
| CS tópicos | 1 | 100,0 | 5 | 27,8 | 6 | 31,6 | ||
| Discontinuación del tratamiento de los irAE | No | 1 | 100,0 | 15 | 78,9 | 16 | 80,0 | Fisher1,000 |
| Sí | 0 | 0,0 | 4 | 21,1 | 4 | 20,0 | ||
| Progresión de la enfermedad | No | 5 | 19,2 | 14 | 60,9 | 19 | 38,8 | 0,003** |
| Sí | 21 | 80,8 | 9 | 39,1 | 30 | 61,2 | ||
| Situación en el seguimiento | Exitus | 15 | 57,7 | 9 | 39,1 | 24 | 49,0 | 0,030** |
| Libre de enfermedad | 3 | 11,5 | 11 | 47,8 | 14 | 28,6 | ||
| Estable | 6 | 23,1 | 3 | 13,0 | 9 | 18,4 | ||
| Estable con iBraf/iMek | 2 | 7,7 | 0 | 0,0 | 2 | 4,1 | ||
| Variables cuantitativas | N.° | Media (DE) | N.° | Media (DE) | N.° | Media (DE) | |
|---|---|---|---|---|---|---|---|
| Edad (a) | 26 | 60,7 (15,2) | 23 | 61,7 (10,2) | 49 | 61,1 (13) | 0,778 |
| Breslow | 18 | 6,5 (6,7) | 19 | 3,1 (2) | 37 | 4,7 (5,1) | 0,051 |
| Tiempo hasta el inicio del efecto inmunomediado (s) | 1 | 12 | 21 | 12,1 (5,3) | 22 | 12,0 (5,2) | 0,972 |
| Tiempo hasta la resolución del efecto inmunomediado (s) | 0 | NA | 5 | 3,0 (1,7) | 5 | 3,0 (1,7) | NA |
| Progresión del melanoma tras la iniciación de CI (s) | 25 | 27,6 (29,6) | 17 | 30,4 (24) | 42 | 28,7 (27,2) | 0,752 |
| Duración del tratamiento de CI (s) | 26 | 21,6 (25,2) | 23 | 19,0 (14,4) | 49 | 20,4 (20,7) | 0,653 |
| Tiempo de seguimiento hasta la última dosis de CI (s) | 26 | 17,7 (32,4) | 23 | 10,3 (12,5) | 49 | 61,1 (13) | 0,289 |
A menos que se exprese lo contrario, las pruebas Chi-cuadrado (χ2) de independencia se realizan para las variables cualitativas, y las pruebas t de Student para las cuantitativas.
a: años; AE: efectos adversos; ALM: melanoma lentiginoso acral; AM: melanoma amelanótico; CI: inhibidores del punto de control; CS: corticosteroides; DE: desviación estándar; EA: enfermedad autoinmune; G: grado; irAE: efecto adverso inmunomediado; IS: inmunosupresión; IT: inmunoterapia; M: mujer; MDR: regímenes de enfermedad metastásica; n: número de pacientes; NA: no aplicable; NM: melanoma nodular; s: semanas; SSM: melanoma de extensión superficial; TA: terapia adyuvante; V: varón.
*p<0,001 hallazgo de diferencias estadísticamente significativas.
Dada la disponibilidad actual de diversas opciones terapéuticas en el contexto del tratamiento del melanoma, es preciso comprender el ratio beneficio/riesgo en la práctica clínica para adoptar decisiones terapéuticas. Nuestro análisis de seguridad con nivolumab, pembrolizumab o/u ipilimumab fue consistente con los perfiles de seguridad establecidos publicados previamente para TA y REM2,4,7–10. Sin embargo, se observaron menores tasas de discontinuación en el análisis del conjunto de datos en nuestra cohorte (8,3%) en comparación con TA-ipilimumab (35-53%), que ya no es considerada como primera opción de TA)2, o con TA-pembrolizumab (13-14,8%),10 similar al compararse con TA-nivolumab (7,7%)7,8. Además, nuestros resultados confirmaron que los IRAE seleccionados en los contextos TA/REM son manejables utilizando guías de seguridad establecidas3. Como se observa con TA-pembrolizumab4, y no todavía con otros fármacos en TA5, los IRAE estuvieron asociados a un mejor pronóstico.
Las limitaciones incluyen la naturaleza retrospectiva y el pequeño tamaño muestral del estudio, lo cual nos empujó a analizar los datos en conjunto. Sin embargo, a nuestro saber, este informe constituye el mayor análisis comparativo hasta la fecha del perfil de seguridad de los CI en términos e TA y REM, en la práctica diaria.
En general, estos hallazgos se añaden a la comprensión del perfil beneficio/riesgo de la inmunoterapia en los pacientes con melanoma resecado de alto riesgo o avanzado, pudiendo servir de guía, en último caso, a los clínicos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.