La escabiosis es una parasitosis altamente prevalente que puede ocasionar un impacto significativo en la calidad de vida e incluso complicaciones graves como sobreinfección estreptocócica y daño renal asociado1. El tratamiento en niños pequeños está basado en la terapia tópica, aunque puede tolerarse mal y tener una mala adherencia terapéutica2. La ivermectina es un antiparasitario ampliamente utilizado y efectivo en la escabiosis1. Su uso está aprobado en adultos y niños > 15 kg, aunque estudios recientes sugieren que también sería segura para lactantes de menor peso2,3.
Describimos cuatro niños < 15 kg (n < 15 kg) con una escabiosis refractaria a terapia tópica tratados exitosamente con ivermectina oral (tabla 1).
Características clínico-epidemiológicas y respuesta terapéutica de los pacientes < 15 kg con escabiosis refractaria a tratamiento tópico tratados con ivermectina oral
| Caso | Sexo/edad (meses) | Peso (kg) | Comorbilidades | Cuadro clínico | Diagnóstico | Tratamientos previos | Dosis de ivermectina oral | Tratamiento tópico concomitante | Formulación* | Respuesta clínica | Efectos adversos |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | F / 16 | 8 | No | Escabiosis nodular (múltiples nódulos en la cara, tronco y extremidades) | Clínico y dermatoscópico (presencia de múltiples surcos con «signo del ala delta») | Permetrina 5% tópica (8 aplicaciones separadas por una semana) | 2 mg (0,25 mg/kg) el día 0 y día 7† | No | Suspensión formulada en la farmacia hospitalaria a partir de comprimidos de 3 mg | Resolución del cuadro clínico a las 3 semanas | No |
| 2 | M/13 | 13 | Dermatitis atópica en tratamiento con corticoides orales (indicados por su pediatra) | Sarna noruega | Clínico y confirmado con examen directo (Test de Muller) | Permetrina 5% tópica(2 aplicaciones separadas por una semana) | 3 mg (0,23 mg/kg) el día 0 y día 7† | Vaselina | Comprimido de 3 mg triturado | Resolución del cuadro clínico a las 3 semanas | No |
| 3 | M/10 | 11 | No | Escabiosis clásica (lesiones vesículo-pustulosas en palmas y plantas) | Clínico y dermatoscópico (presencia de múltiples surcos con «signo del ala delta») | Permetrina 5% tópica (3 ciclos de 2 aplicaciones separadas 1 semana cada uno) | 3 mg (0,27 mg/kg) el día 0 y día 7† | No | Comprimido de 3 mg triturado | Resolución del cuadro clínico a las 3 semanas | No |
| 4 | F/20 | 12 | No | Escabiosis clásica (lesiones vesículo-pustulosas en palmas y plantas) | Clínico y dermatoscópico (presencia de múltiples surcos con «signo del ala delta») | Permetrina 5% tópica (6 aplicaciones separadas por una semana) | 3 mg (0,25 mg/kg) el día 0 y día 7† | No | Comprimido de 3 mg triturado | Resolución del cuadro clínico a las 3 semanas | No |
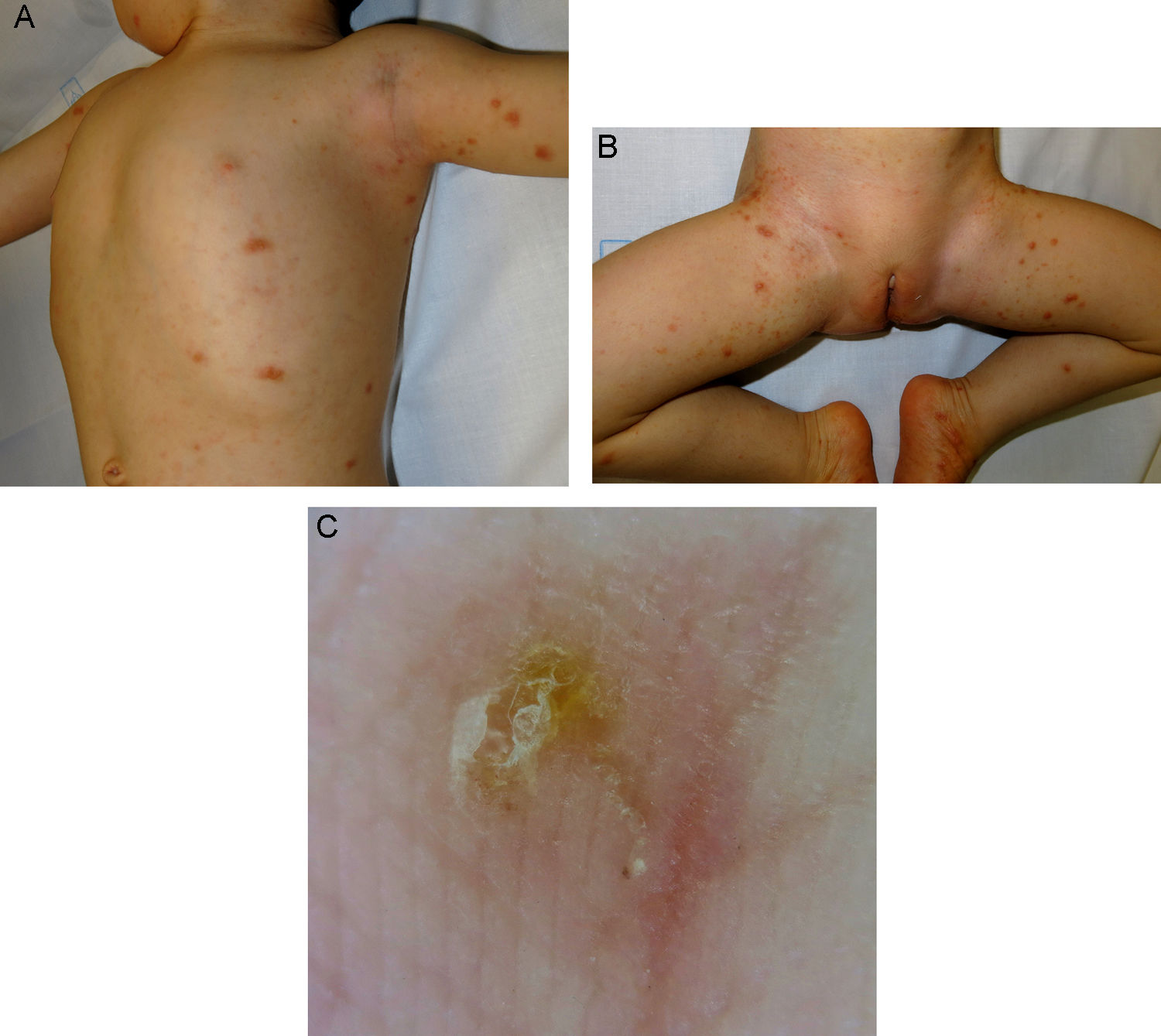
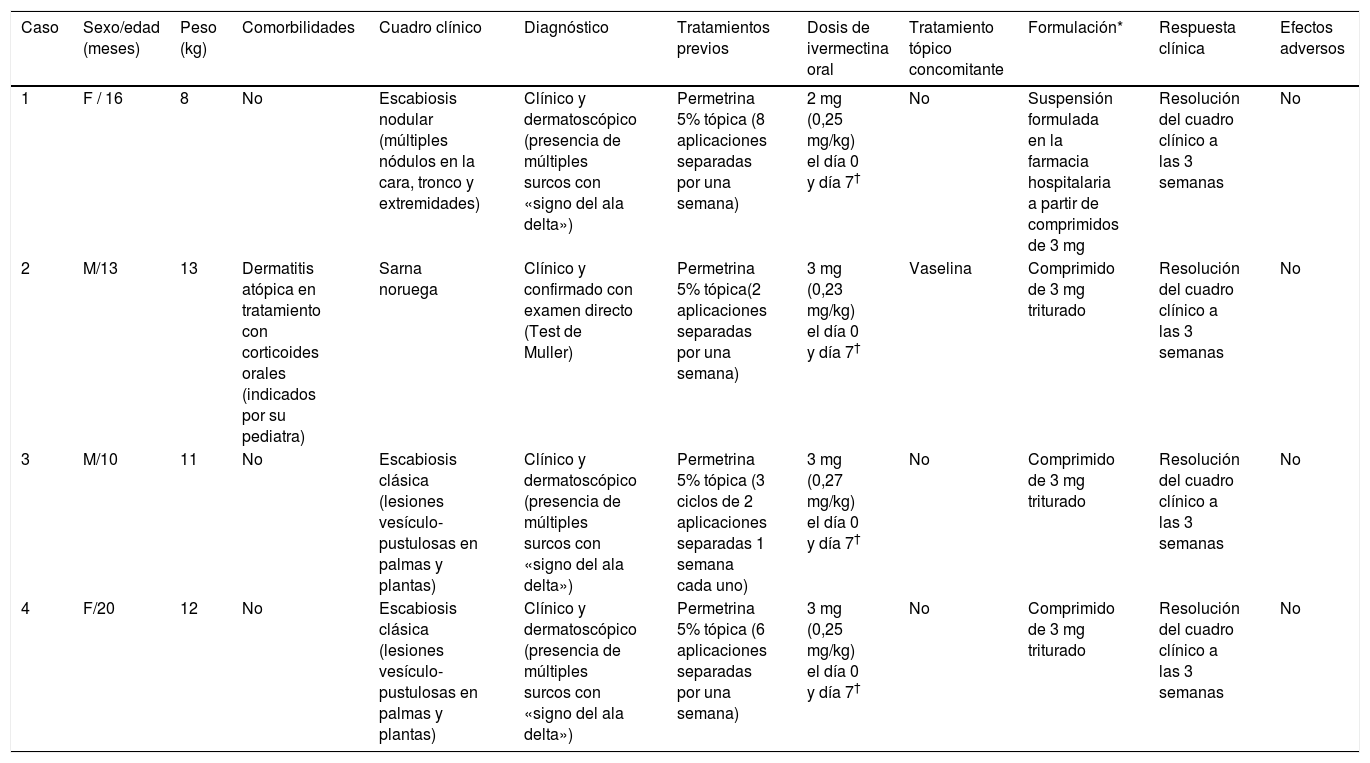
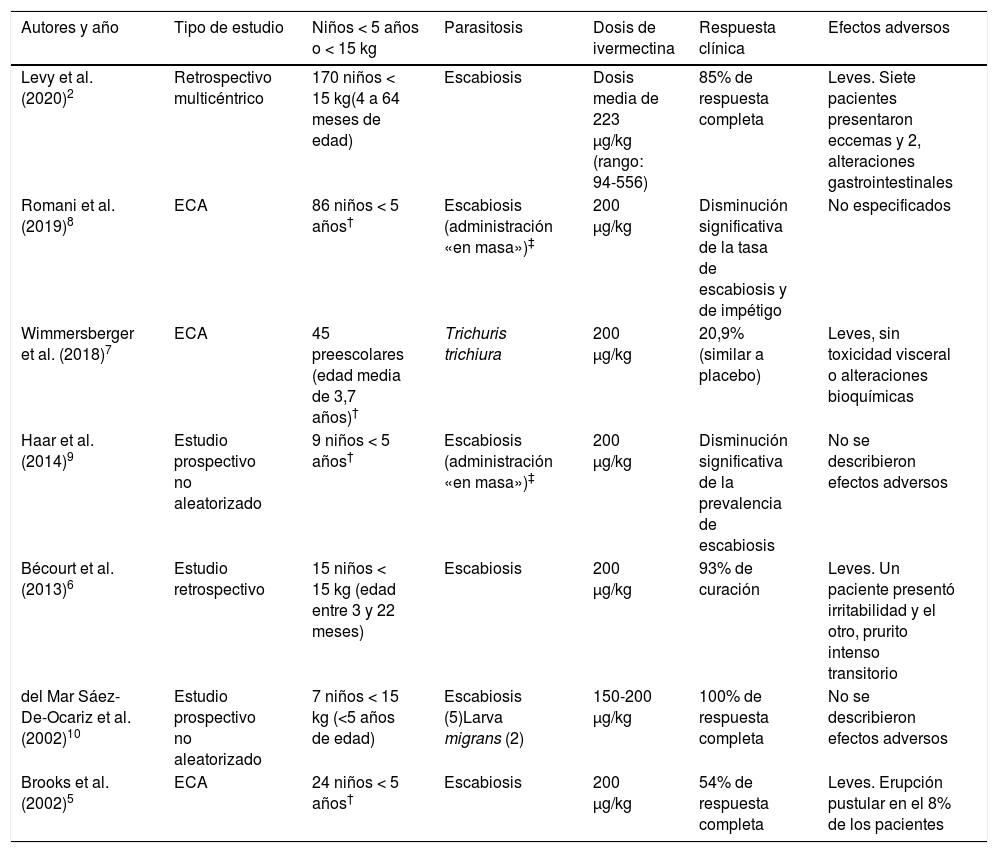
Un lactante de 16 meses y 8 kg fue referido por escabiosis nodular. Presentaba surcos acarinos en los pies y las muñecas, en los que se observaba el «signo del ala delta» en examen dermatoscópico (fig. 1 A-C). Recibió dos dosis de ivermectina de 2 mg (250 μg/kg) separadas por siete días. El segundo caso tenía 13 meses, pesaba 13 kg y tenía antecedentes de dermatitis atópica en tratamiento con corticoides orales desde hacía dos meses, pautados por su pediatra. Presentaba lesiones eritematodescamativas generalizadas desde hacía un mes y había sido diagnosticado de sarna noruega (posiblemente relacionada con la inmunosupresión secundaria a la corticoterapia sistémica), y tratado con permetrina tópica en múltiples ocasiones (tabla 1). El examen directo del raspado de escamas confirmó la presencia del Sarcoptes scabiei. Recibió dos dosis de ivermectina de 3 mg (230 μg/kg) separadas por siete días. El tercer y cuarto pacientes eran lactantes de 10 meses (11 kg) y 20 meses (12 kg), con un cuadro de escabiosis clásica. Presentaban surcos acarinos en los pliegues, el tronco y las muñecas, así como vesículas y pústulas pruriginosas en las palmas y las plantas. Recibieron dos dosis de ivermectina de 3 mg (270 μg/kg y 250 μg/kg, respectivamente) separadas por siete días. Los cuatro casos presentaron una respuesta completa al cabo de tres semanas, sin observarse efectos adversos.
El tratamiento de la escabiosis en n < 15 kg puede ser complejo, los tratamientos tópicos pueden ser difíciles de aplicar, ocasionar irritación cutánea y efectos adversos sistémicos. La ivermectina es un antiparasitario incluido en la lista de medicamentos esenciales de la Organización Mundial de la Salud y presenta una eficacia y una tolerancia similar a la permetrina tópica para el tratamiento de la escabiosis1. Los efectos adversos de la ivermectina son mayoritariamente leves e incluyen mareos, cefalea, síntomas gastrointestinales, parestesias y eccema4.
Recientemente, un estudio multicéntrico retrospectivo que incluyó a 170 niños de entre cuatro y 64 meses de edad, con un peso de 4 a 14 kg (31 de ellos < 7,5 kg), tratados con ivermectina oral (dosis media de 223 μg/kg [rango: 94-556 μg/kg]), mostró una respuesta terapéutica del 85% con unos efectos adversos mínimos. Siete pacientes presentaron eccema y dos, alteraciones gastrointestinales leves. Una dosis > 200 μg/kg y un intervalo entre dosis < 10 días se asociaron a una probabilidad mayor de remisión. Aunque la ivermectina sólo estaba disponible en comprimidos, no se describieron dificultades para administrar el fármaco2. Una revisión sistemática de la literatura publicada el año 2018 encontró nueve estudios con un total de 61 pacientes < 5 años tratados con ivermectina para diversas parasitosis, 24 de ellos < 15 kg (no se tenía información del peso de los demás individuos, pero probablemente muchos pesarán < 15 kg dada su edad), con una respuesta terapéutica buena en escabiosis, sin efectos adversos significativos3. Destaca el ensayo clínico aleatorizado de Brooks et al.5 que incluyó 45 niños entre uno y cinco años de edad con escabiosis y tratados con una dosis de 200 μg/kg. Si bien la tasa de respuesta (54%) fue menor que la descrita con dos dosis1,2, no se observaron efectos adversos moderado/graves. Bécourt et al.6 realizaron un estudio retrospectivo con 15 n < 15 kg (tres a 22 meses de edad) con escabiosis tratados con dos dosis de ivermectina oral, en los que observaron un 93% de respuesta completa y mínimos efectos adversos transitorios. Un ensayo clínico aleatorizado (no incluido en la revisión sistemática previa) que evaluó la efectividad de la ivermectina oral en el tratamiento del parásito Trichuris trichiura, incluyó 45 preescolares (edad media de 3,7 años) y una dosis de 200 μg/kg. El tratamiento no fue efectivo, aunque fue bien tolerado, describiéndose sólo efectos adversos leves (tabla 2). Se realizaron estudios de laboratorio basales y 72 horas después del tratamiento con ivermectina: en ningún caso se observó el desarrollo de anemia, plaquetopenia, neutropenia, insuficiencia renal o alteraciones de la función hepática7.
Estudios sobre el uso de ivermectina oral para el tratamiento de parasitosis en niños < 15 kg*
| Autores y año | Tipo de estudio | Niños < 5 años o < 15 kg | Parasitosis | Dosis de ivermectina | Respuesta clínica | Efectos adversos |
|---|---|---|---|---|---|---|
| Levy et al. (2020)2 | Retrospectivo multicéntrico | 170 niños < 15 kg(4 a 64 meses de edad) | Escabiosis | Dosis media de 223 μg/kg (rango: 94-556) | 85% de respuesta completa | Leves. Siete pacientes presentaron eccemas y 2, alteraciones gastrointestinales |
| Romani et al. (2019)8 | ECA | 86 niños < 5 años† | Escabiosis (administración «en masa»)‡ | 200 μg/kg | Disminución significativa de la tasa de escabiosis y de impétigo | No especificados |
| Wimmersberger et al. (2018)7 | ECA | 45 preescolares (edad media de 3,7 años)† | Trichuris trichiura | 200 μg/kg | 20,9% (similar a placebo) | Leves, sin toxicidad visceral o alteraciones bioquímicas |
| Haar et al. (2014)9 | Estudio prospectivo no aleatorizado | 9 niños < 5 años† | Escabiosis (administración «en masa»)‡ | 200 μg/kg | Disminución significativa de la prevalencia de escabiosis | No se describieron efectos adversos |
| Bécourt et al. (2013)6 | Estudio retrospectivo | 15 niños < 15 kg (edad entre 3 y 22 meses) | Escabiosis | 200 μg/kg | 93% de curación | Leves. Un paciente presentó irritabilidad y el otro, prurito intenso transitorio |
| del Mar Sáez-De-Ocariz et al. (2002)10 | Estudio prospectivo no aleatorizado | 7 niños < 15 kg (<5 años de edad) | Escabiosis (5)Larva migrans (2) | 150-200 μg/kg | 100% de respuesta completa | No se describieron efectos adversos |
| Brooks et al. (2002)5 | ECA | 24 niños < 5 años† | Escabiosis | 200 μg/kg | 54% de respuesta completa | Leves. Erupción pustular en el 8% de los pacientes |
Recientemente, diversos estudios han evaluado la administración terapéutica «en masa» (ATM) para diversas infecciones e infestaciones (tratamiento de todos los individuos de una comunidad independientemente de su estado, infestado o contacto) describiendo resultados esperanzadores. Un ensayo clínico evaluó tres brazos de tratamiento para la escabiosis: ATM de ivermectina oral (incluyendo 86 niños < 5 años), ATM de permetrina tópica o terapia estándar con permetrina tópica de los afectados por escabiosis y sus contactos. En la evaluación 24 meses después de 823 sujetos, la prevalencia de escabiosis y de impétigo fue significativamente menor en la comunidad que había recibido ATM con ivermectina oral. No se recogió la incidencia de efectos adversos8.
Desde mediados del 2021 está disponible comercialmente la ivermectina oral en España, con dosificación de 12 mg (3 comprimidos de 4 mg) (Ivergalen®, Galenicum Derma), lo que puede facilitar la prescripción de este fármaco.
La ivermectina oral parece ser bien tolerada en n < 15 kg con escabiosis. La realización de ensayos clínicos aleatorizados es prioritaria dada la alta prevalencia de diversas parasitosis en esta edad y los buenos resultados obtenidos con la ATM de este fármaco.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.