Los linfomas cutáneos de células B del centro folicular son tumores indolentes compuestos por células neoplásicas del centro folicular. Están constituidos por una mezcla de centrocitos con un número variable de centroblastos. Los tratamientos habitualmente utilizados son la cirugía y la radioterapia, aunque se utilizan otros como el interferón-α (IFN-α), la quimioterapia y tratamientos biológicos (rituximab). El rituximab es un anticuerpo monoclonal quimérico anti-CD20. Puede utilizarse por vía intravenosa o intralesional.
Presentamos el caso de un paciente varón de 41 años que consultó por lesiones nodulares violáceas en el área escapular izquierda y que, tras la realización de una biopsia, analítica, tomografía axial computarizada (TAC) toracoabdominopélvica, ecografía abdominal y biopsia de médula ósea fue diagnosticado de linfoma cutáneo de células B del centro folicular. Se decidió tratamiento con 30 mg de rituximab intralesional, tres veces a la semana, una vez al mes, durante 4 meses, con respuesta completa. Realizamos una revisión de los casos de linfoma cutáneo de células B tratados con rituximab intralesional.
Cutaneous follicular center B-cell lymphomas are indolent tumors characterized by the presence of neoplastic follicular center cells. They contain a mixture of centrocytes with a variable number of centroblasts. The tumor is usually treated by surgery or radiotherapy, although other treatments may be used such as interferon-α, chemotherapy, and biological agents (rituximab). Rituximab is a chimeric monoclonal anti-CD20 antibody that can be administered intravenously or intralesionally.
We report the case of a 41-year-old man who consulted for violaceous nodular lesions in the left scapular region and who was diagnosed with cutaneous follicular center B-cell lymphoma after biopsy, laboratory tests, thoracic-abdominal-pelvic computed tomography, abdominal ultrasound, and bone marrow biopsy. It was decided to treat him with 30 mg of intralesional rituximab administered for 1 week (3 times) every month for 4 months. Complete response was obtained. We also review the published cases of cutaneous B-cell lymphoma treated with intralesional rituximab.
Los linfomas cutáneos de células B (LCCB) son un grupo heterogéneo de procesos linfoproliferativos que se presentan en la piel. La clasificación de la WHO-EORTC los divide en linfoma de la zona marginal, linfoma del centro folicular, linfoma de células grandes de las piernas y linfoma de células grandes (otros tipos).
Los tratamientos utilizados en los LCCB son la cirugía y/o la radioterapia, menos frecuentemente el interferón alfa (IFN-α), la quimioterapia y, recientemente, el rituximab.
El rituximab es un anticuerpo monoclonal quimérico anti-CD20. El CD20 se expresa en el 95 % de los LCCB. Lleva empleándose en los linfomas de células B no Hodgkin sistémicos desde 1997 con buenos resultados. En los LCCB se utiliza por vía intravenosa e intralesional. La administración intralesional es muy bien tolerada, eficaz y con un coste mucho menor que la administración intravenosa.
Caso clínicoUn paciente varón, de 41 años de edad, sin antecedentes personales de interés, consultó por lesiones asintomáticas en el área escapular izquierda de 5 meses de evolución sin clínica acompañante.
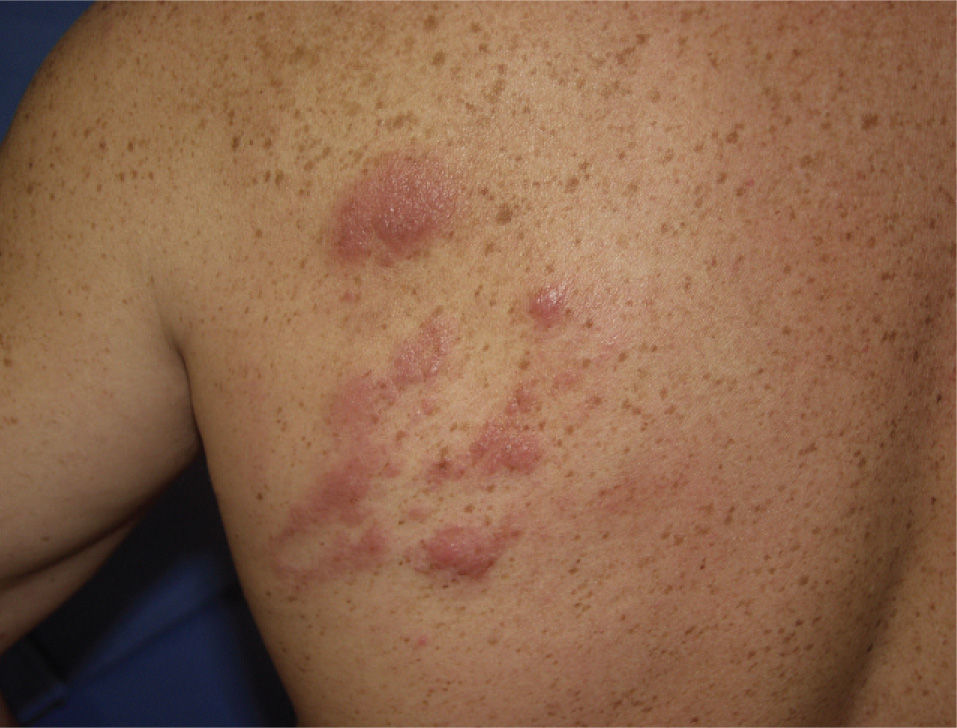
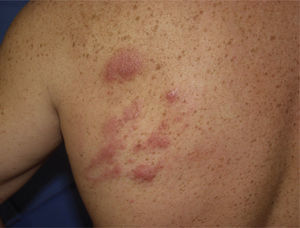
En la exploración física se apreciaban pápulas eritematovioláceas, infiltradas, de entre 1 y 3cm de diámetro agrupadas en un área de unos 9cm, localizadas en el área escapular izquierda (fig. 1). No presentaba adenopatías.
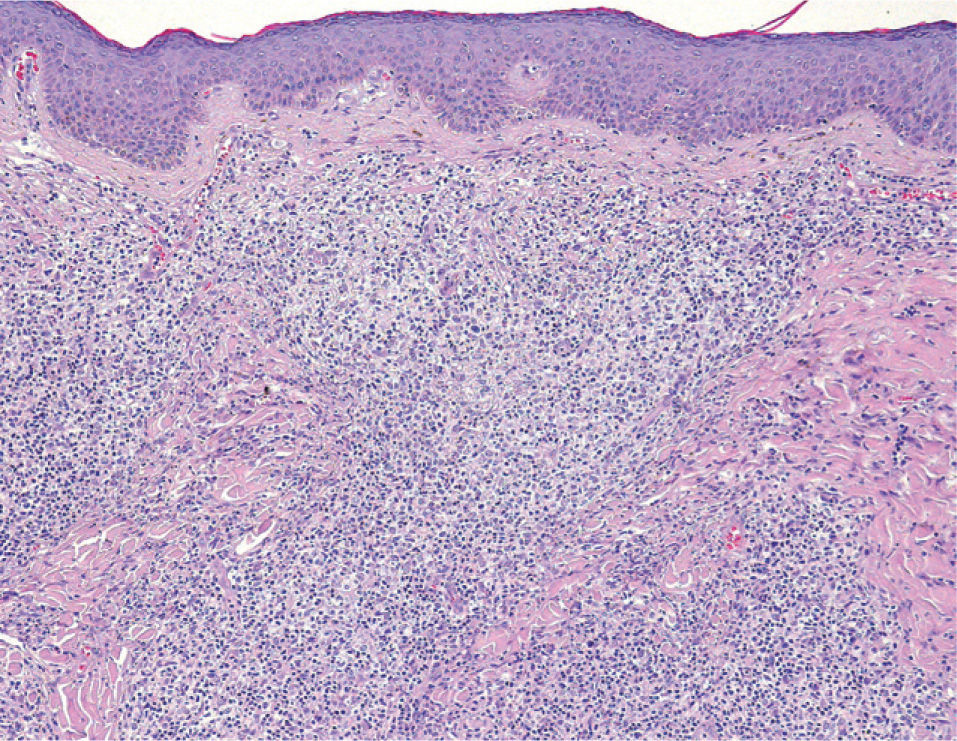
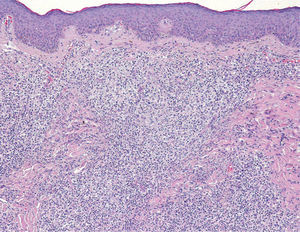
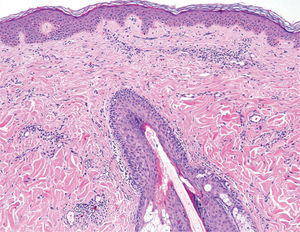
Se realizó una biopsia en la que se apreciaba infiltración de la dermis por un proceso linfoproliferativo con un patrón de crecimiento variable, con áreas discretamente nodulares que alternaban con otras de aspecto difuso, fundamentalmente en dermis superficial. La lesión estaba constituida por un infiltrado polimorfo, tanto en su tamaño, intermedio y grande, como en su forma, apreciándose muchas células de morfología hendida y otras grandes no hendidas. Las células se encontraban entremezcladas, con abundantes linfocitos de aspecto maduro, así como con células de hábito histiocitario. La epidermis suprayacente era normal (fig. 2).
El estudio inmunohistoquímico mostraba expresión en las células proliferantes de tamaño intermedio y grande de CD20, bcl-6 y puntualmente CD10, con ausencia de expresión para CD3, bcl-2, ciclina D-1 y cadenas ligeras kappa y lambda. Las células proliferantes grandes mostraban inmunoexpresión para Mib-1 y ocasionalmente para CD30. Los linfocitos pequeños, de aspecto maduro, eran reactivos para CD3, CD43 y ocasionalmente para bcl-2.
Se realizó un sistemático de sangre, orina, bioquímica y coagulación con parámetros dentro de la normalidad. Las serologías para virus de la hepatitis B, hepatitis C y virus de la inmunodeficiencia humana (VIH) fueron negativas. La ecografía abdominal y la tomografía axial computarizada (TAC) toracoabdominopélvica no mostraron alteraciones. La biopsia de médula ósea no evidenció infiltración neoplásica.
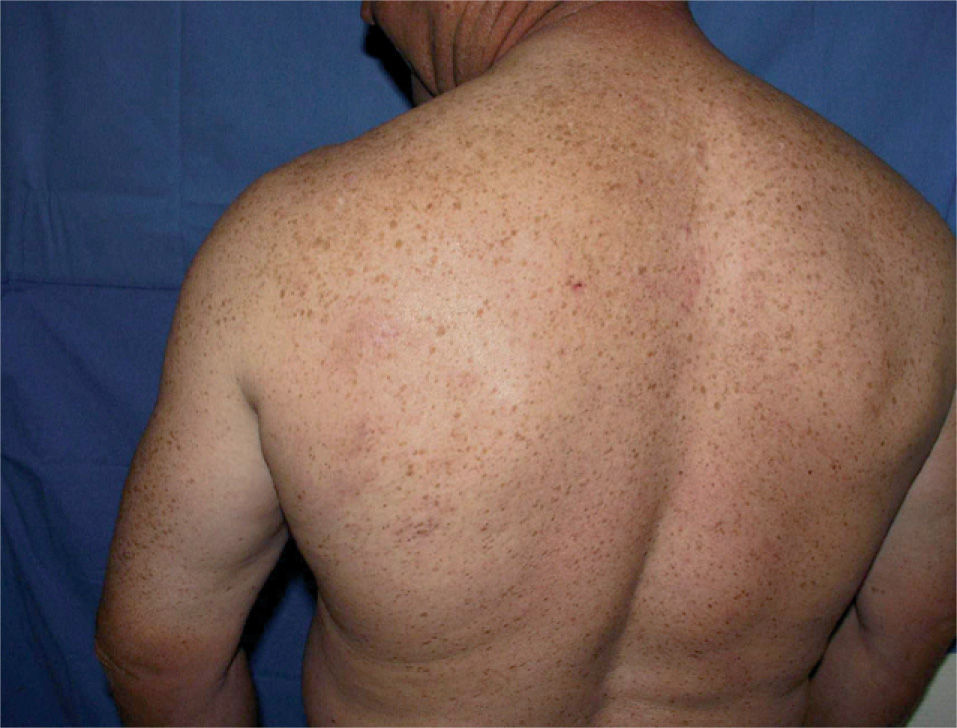
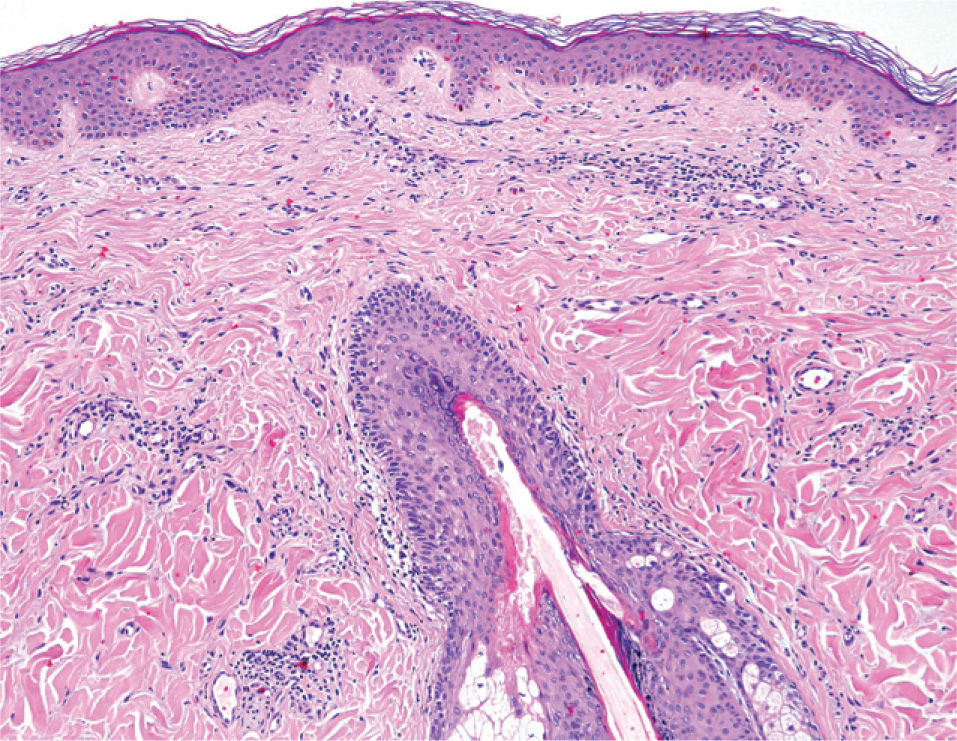
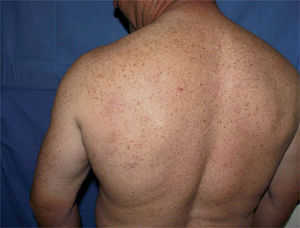
El paciente fue diagnosticado de LCCB del centro folicular. Tras solicitar su uso compasivo se inició terapia con rituximab intralesional 30mg (distribuidos entre las diferentes lesiones), tres días a la semana, una semana al mes durante 4 meses. Todas las lesiones fueron infiltradas. Tras el segundo ciclo la mayoría de las lesiones respondieron al tratamiento, exceptuando una lesión que tras dos ciclos más de tratamiento se resolvió. Se realizó una biopsia de esta última lesión un mes después de finalizar el tratamiento que no mostró infiltración neoplásica (figs. 3 y 4). La tolerancia del paciente al tratamiento fue buena, refiriendo dolor leve en las inyecciones, y en los controles analíticos realizados no se observaron alteraciones.
No ha presentado recidiva de las lesiones tras un período de 6 meses de seguimiento.
DiscusiónLos linfomas cutáneos primarios de células B son un grupo heterogéneo de procesos linfoproliferativos. Los LCCB se definen como la infiltración monoclonal cutánea de células B en ausencia de afectación extracutánea después del estadiaje completo. El estudio histológico mediante inmunotipificación con anticuerpos monoclonales en tejido congelado o incluido en parafina es necesario para el diagnóstico de un LCCB primario. Ante la sospecha clinicopatológica de LCCB es necesaria la realización de una TAC abdominopélvica para descartar afectación ganglionar, una ecografía abdominal que descarte afectación visceral, un aspirado y biopsia de médula ósea y llevar a cabo una citometría y análisis de lactatodeshidrogenasa (LDH)1. Los LCCB pueden clasificarse (según la clasificación de la WHO-EORTC) en linfoma de la zona marginal, linfoma del centro folicular, linfoma difuso de células grandes (tipo piernas) y linfoma B difuso de células grandes (otros tipos).
El linfoma cutáneo de células B del centro folicular es un tumor indolente compuesto por células neoplásicas del centro folicular: una mezcla de centrocitos (pequeños o grandes, hendidos) con un número variable de centroblastos (grandes, no hendidos y de nucleolo prominente). Pueden presentar un patrón de crecimiento difuso, folicular o mixto. Las localizaciones más frecuentes son la espalda y la cabeza, pero pueden presentarse en otras zonas y es posible la multifocalidad que no implica peor pronóstico.
Por inmunofenotipificación se observa restricción a una cadena ligera de inmunoglobulinas o pérdida de ambas, además de la positividad para CD20 y CD79a (panB). La expresión de bcl-6 suele ser positiva, la de CD10 variable y la expresión de bcl-2 negativa o débilmente positiva. La inmunogenotipificación muestra reordenamiento de la cadena pesada y ausencia de traslocación t (14,18).
Actualmente los tratamientos para los linfomas cutáneos de células B son la escisión quirúrgica y/o la radioterapia, el IFN-α intralesional o sistémico, la quimioterapia y el rituximab2.
La escisión quirúrgica es buena opción en caso de una lesión aislada o un pequeño número de lesiones agrupadas en una zona. Puede asociarse a radioterapia.
La radioterapia es efectiva en el tratamiento de lesiones de LCCB. Habitualmente se utilizan dosis que oscilan entre los 20 y los 30Gy. Es un tratamiento bien tolerado y muchos autores lo consideran de primera elección para lesiones localizadas.
El IFN-α actúa por sus propiedades inmunomoduladoras y antitumorales. Se emplea menos frecuentemente en linfomas cutáneos de células B que en linfomas cutáneos de células T. Las dosis que se utilizan habitualmente oscilan entre los 3 y los 9 millones de unidades subcutáneas administradas semanalmente. El IFN-α también puede ser administrado intralesionalmente. Los efectos secundarios más habituales son astenia, fiebre y naúseas.
La quimioterapia no es el tratamiento de elección en los linfomas cutáneos de células B. Se emplea sobre todo en las formas más agresivas de este tipo de linfomas, como el linfoma de células grandes de las piernas. La mayoría de las veces la quimioterapia más utilizada es el régimen CHOP (ciclofosfamida, doxorrubicina, vincristina y prednisona).
El rituximab es un anticuerpo monoclonal quimérico anti-CD20. El CD20 es una fosfoproteína de membrana que se expresa exclusivamente en los linfocitos B. Está presente en el 95 % de los linfomas de células B. Desde 1997 se emplea en el tratamiento de linfomas de células B no Hodgkin. Ha demostrado ser un tratamiento eficaz en linfomas cutáneos de células B. Se administra por vía intravenosa3 o intralesional.
La dosis intravenosa empleada habitualmente es de 375mg/m2 semanales entre 4 semanas y 8 semanas. La dosis total empleada es de entre 1.500 y 3.000mg/m2. Produce depleción transitoria de los linfocitos B que no se asocia a inmunodeficiencia y que se regenera en un período de 6 a 12 meses. Entre los efectos adversos descritos tras la administración sistémica de rituximab se encuentran la fiebre, la cefalea, la hipotensión arterial, la disnea, el broncoespamo, la urticaria, el angioedema, la trombocitopenia y la linfopenia. Pero las reacciones adversas a rituximab sistémico no son frecuentes y se observan sobre todo en la primera infusión, disminuyendo en las dosis posteriores. Suelen administrarse hidroxicina diclorhidrato y analgésicos por vía oral previa y posteriormente a las infusiones. El rituximab intravenoso no se asocia con riesgo significativo de toxicidad sistémica o infecciones oportunistas.
La administración intralesional de rituximab es muy bien tolerada refiriendo, la mayoría de pacientes, únicamente dolor en las inyecciones. Se suelen administrar dosis que oscilan entre los 10 y los 40mg tres veces a la semana una vez al mes, hasta obtener la respuesta completa de las lesiones.
Han sido publicados los casos de 21 pacientes con LCCB primario tratados con rituximab intralesional4-9. Incluyendo nuestro paciente en los datos que vamos a describir a continuación, la edad de los sujetos sometidos a estudio oscila entre los 34 y los 82 años edad, con una media de 54 años. Nueve pacientes son mujeres y 13 varones; 12 casos corresponden a un linfoma cutáneo de células B del centro folicular, 9 a linfoma de la zona marginal y un caso a un linfoma de células grandes (no de las piernas). Las dosis totales administradas intralesionalmente oscilan entre los 30 y los 720mg con una media aproximada de 187mg. La mayoría de los pacientes recibieron la terapia en dosis tres veces a la semana, una semana al mes. La dosis diaria oscila entre 1 y 4ml de solución de rituximab (10 y 40mg).
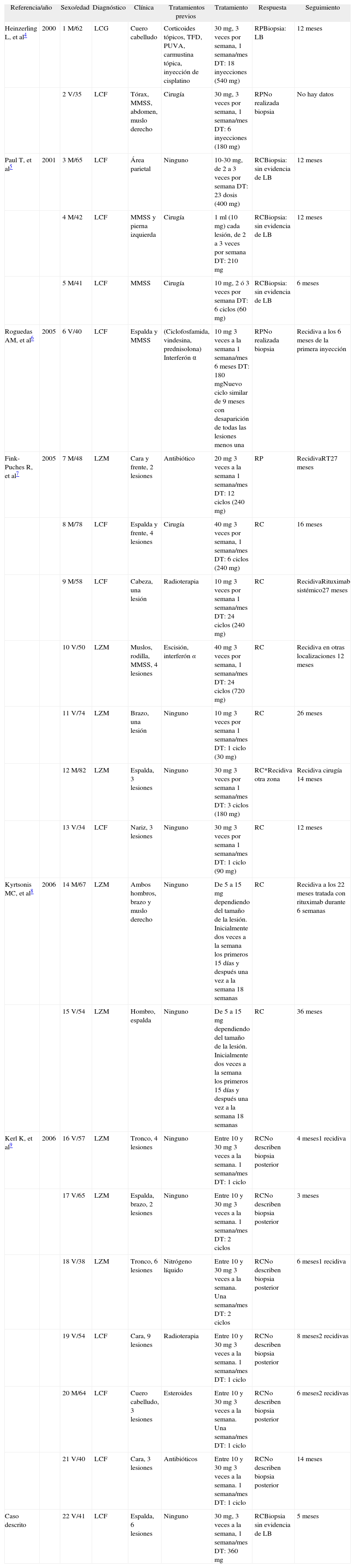
Algunos pacientes se habían sometido a tratamientos previos (cirugía, radioterapia, IFN, CHOP, PUVA, etc.) pero otros recibieron el rituximab intralesional como primer tratamiento (tabla 1).
Pacientes con linfoma cutáneo de células B tratados con rituximab intralesional
| Referencia/año | Sexo/edad | Diagnóstico | Clínica | Tratamientos previos | Tratamiento | Respuesta | Seguimiento | |
| Heinzerling L, et al4 | 2000 | 1M/62 | LCG | Cuero cabelludo | Corticoides tópicos, TFD, PUVA, carmustina tópica, inyección de cisplatino | 30 mg, 3 veces por semana, 1 semana/mes DT: 18 inyecciones (540 mg) | RPBiopsia: LB | 12 meses |
| 2V/35 | LCF | Tórax, MMSS, abdomen, muslo derecho | Cirugía | 30 mg, 3 veces por semana, 1 semana/mes DT: 6 inyecciones (180 mg) | RPNo realizada biopsia | No hay datos | ||
| Paul T, et al5 | 2001 | 3M/65 | LCF | Área parietal | Ninguno | 10-30 mg, de 2 a 3 veces por semana DT: 23 dosis (400 mg) | RCBiopsia: sin evidencia de LB | 12 meses |
| 4M/42 | LCF | MMSS y pierna izquierda | Cirugía | 1 ml (10 mg) cada lesión, de 2 a 3 veces por semana DT: 210 mg | RCBiopsia: sin evidencia de LB | 12 meses | ||
| 5M/41 | LCF | MMSS | Cirugía | 10 mg, 2 ó 3 veces por semana DT: 6 ciclos (60 mg) | RCBiopsia: sin evidencia de LB | 6 meses | ||
| Roguedas AM, et al6 | 2005 | 6V/40 | LCF | Espalda y MMSS | (Ciclofosfamida, vindesina, prednisolona) Interferón α | 10 mg 3 veces a la semana 1 semana/mes 6 meses DT: 180 mgNuevo ciclo similar de 9 meses con desaparición de todas las lesiones menos una | RPNo realizada biopsia | Recidiva a los 6 meses de la primera inyección |
| Fink-Puches R, et al7 | 2005 | 7M/48 | LZM | Cara y frente, 2 lesiones | Antibiótico | 20 mg 3 veces a la semana 1 semana/mes DT: 12 ciclos (240 mg) | RP | RecidivaRT27 meses |
| 8M/78 | LCF | Espalda y frente, 4 lesiones | Cirugía | 40 mg 3 veces por semana, 1 semana/mes DT: 6 ciclos (240 mg) | RC | 16 meses | ||
| 9M/58 | LCF | Cabeza, una lesión | Radioterapia | 10 mg 3 veces por semana 1 semana/mes DT: 24 ciclos (240 mg) | RC | RecidivaRituximab sistémico27 meses | ||
| 10V/50 | LZM | Muslos, rodilla, MMSS, 4 lesiones | Escisión, interferón α | 40 mg 3 veces por semana, 1 semana/mes DT: 24 ciclos (720 mg) | RC | Recidiva en otras localizaciones 12 meses | ||
| 11V/74 | LZM | Brazo, una lesión | Ninguno | 10 mg 3 veces por semana 1 semana/mes DT: 1 ciclo (30 mg) | RC | 26 meses | ||
| 12M/82 | LZM | Espalda, 3 lesiones | Ninguno | 30 mg 3 veces por semana 1 semana/mes DT: 3 ciclos (180 mg) | RC*Recidiva otra zona | Recidiva cirugía 14 meses | ||
| 13V/34 | LCF | Nariz, 3 lesiones | Ninguno | 30 mg 3 veces por semana 1 semana/mes DT: 1 ciclo (90 mg) | RC | 12 meses | ||
| Kyrtsonis MC, et al8 | 2006 | 14M/67 | LZM | Ambos hombros, brazo y muslo derecho | Ninguno | De 5 a 15 mg dependiendo del tamaño de la lesión. Inicialmente dos veces a la semana los primeros 15 días y después una vez a la semana 18 semanas | RC | Recidiva a los 22 meses tratada con rituximab durante 6 semanas |
| 15V/54 | LZM | Hombro, espalda | Ninguno | De 5 a 15 mg dependiendo del tamaño de la lesión. Inicialmente dos veces a la semana los primeros 15 días y después una vez a la semana 18 semanas | RC | 36 meses | ||
| Kerl K, et al9 | 2006 | 16V/57 | LZM | Tronco, 4 lesiones | Ninguno | Entre 10 y 30 mg 3 veces a la semana. 1 semana/mes DT: 1 ciclo | RCNo describen biopsia posterior | 4 meses1 recidiva |
| 17V/65 | LZM | Espalda, brazo, 2 lesiones | Ninguno | Entre 10 y 30 mg 3 veces a la semana. 1 semana/mes DT: 2 ciclos | RCNo describen biopsia posterior | 3 meses | ||
| 18V/38 | LZM | Tronco, 6 lesiones | Nitrógeno líquido | Entre 10 y 30 mg 3 veces a la semana. Una semana/mes DT: 2 ciclos | RCNo describen biopsia posterior | 6 meses1 recidiva | ||
| 19V/54 | LCF | Cara, 9 lesiones | Radioterapia | Entre 10 y 30 mg 3 veces a la semana. 1 semana/mes DT: 1 ciclo | RCNo describen biopsia posterior | 8 meses2 recidivas | ||
| 20M/64 | LCF | Cuero cabelludo, 3 lesiones | Esteroides | Entre 10 y 30 mg 3 veces a la semana. Una semana/mes DT: 1 ciclo | RCNo describen biopsia posterior | 6 meses2 recidivas | ||
| 21V/40 | LCF | Cara, 3 lesiones | Antibióticos | Entre 10 y 30 mg 3 veces a la semana. 1 semana/mes DT: 1 ciclo | RCNo describen biopsia posterior | 14 meses | ||
| Caso descrito | 22V/41 | LCF | Espalda, 6 lesiones | Ninguno | 30 mg, 3 veces a la semana, 1 semana/mes DT: 360 mg | RCBiopsia sin evidencia de LB | 5 meses | |
DT: dosis total; LCF: linfoma del centro folicular; LCG: linfoma de células grandes; LZM: linfoma de la zona marginal; M: mujer;
MMSS: miembros superiores; RC: respuesta completa; RP: respuesta parcial; TFD: terapia fotodinámica; V: varón.
Dieciocho de los 22 casos presentaron respuesta completa con confirmación histológica en algunos de los casos. De los 18 casos con respuesta completa, 10 son linfomas cutáneos del centro folicular y 8 linfomas B cutáneos de la zona marginal.
De los 18 pacientes en los que se observó respuesta completa de las lesiones, 10 no han presentado recidiva de lesiones de linfoma tras un seguimiento que oscila entre los 3 y los 36 meses, con una media de 14,2 meses. Las dosis totales acumuladas en los pacientes con respuesta completa sin recidiva fueron similares a las de aquellos con respuesta completa y recidiva.
El tratamiento con rituximab intralesional es muy bien tolerado por los pacientes, es eficaz y el coste es mucho menor que el tratamiento con rituximab intravenoso.
Se necesitan estudios comparativos entre el rituximab intralesional e intravenoso para comparar la respuesta, los efectos adversos y el porcentaje de recidivas con cada uno de ellos. Así mismo deberían estandarizarse las dosis de tratamiento y establecer qué dosis se asocian a menores tasas de recidiva.
Conflicto de interesesDeclaramos no tener ningún conflicto de intereses.