La naturaleza resistente y recalcitrante de la dermatitis de contacto alérgica (DCA) grave hace que su tratamiento sea desafiante. Con los avances en la comprensión de la patogénesis celular y molecular de esta dermatosis, están surgiendo nuevas opciones terapéuticas. En particular, el uso de fármacos biológicos como dupilumab e inhibidores de moléculas pequeñas (como los inhibidores de JAK) han cobrado impulso, dada la inhibición transversal de las acciones de múltiples citoquinas. Este artículo tiene como objetivo revisar los datos disponibles actuales sobre el uso de fármacos biológicos y fármacos inhibidores de moléculas pequeñas en la DCA. Los resultados sugieren que los iJAK, como abrocitinib, tofacitinib, upadacitinib y baricitinib; y los fármacos biológicos, como dupilumab, muestran promesas significativas en la DCA refractaria, aunque se necesitan más ensayos clínicos a largo plazo para confirmar su eficacia y seguridad.
The resistant and recalcitrant nature of severe allergic contact dermatitis (ACD) makes treatment challenging. With advances in the understanding of the cellular and molecular pathogenesis of this dermatosis, new therapeutic options are emerging. In particular, the use of biologic drugs such as dupilumab and small molecule inhibitors, such as JAK inhibitors have gained momentum given the cross-cutting inhibition of multiple cytokine actions. This article aims to review the current available data on the use of biologic drugs and small molecule inhibitor drugs in the management of ACD. Results suggest that iJAKs, such as abrocitinib, tofacitinib, upadacitinib, and baricitinib; although biologic drugs, such as dupilumab show significant promise in refractory ACD, more long-term clinical trials are needed to confirm their safety and efficacy profile.
Se ha estimado que entre el 4 y 7% de las consultas dermatológicas son por dermatitis de contacto1. La prevalencia de la dermatitis de contacto alérgica (DCA) es desconocida, aunque algunos estudios la han estimado entre un 1,7 y 9,8%2, siendo especialmente importante en aquellas de origen ocupacional3. Hay diferentes patrones clínicos en la DCA según el área afectada. El conocimiento de estos patrones no solo ayudará al médico a llegar al diagnóstico, sino que también sugerirá posibles alérgenos y formas de contacto4. El gold estándar para el estudio de los pacientes continúa siendo las pruebas epicutáneas, con una tasa de positividad relevante entre el 15 y 20,1% de los pacientes parcheados5. Todos los pacientes deberían ser estudiados con la serie estándar nacional6, los productos propios del paciente7, y en función de las características del caso y las fuentes de exposición, añadir las series específicas comercializadas. La identificación de los alérgenos responsables y su evitación en ocasiones no es suficiente para resolver el problema, lo cual plantea la necesidad de prescribir un tratamiento tópico y/o sistémico inmunosupresor en estos casos refractarios. La falta de respuesta a la evitación del alérgeno y la limitación de los tratamientos tradicionales destacan la necesidad de nuevas terapias8. La reciente investigación en inhibidores de moléculas pequeñas y fármacos biológicos ofrece nuevas esperanzas, especialmente para aquellos que no responden a los enfoques convencionales.
En la práctica clínica puede no ser posible realizar el estudio de pruebas epicutáneas suspendiendo el fármaco inmunosupresor, lo cual aumenta el riesgo de falsos negativos9. Los pacientes con polisensibilización (3 o más alérgenos) en pruebas epicutáneas son un grupo de pacientes de difícil control, que aumenta el riesgo de refractariedad tras el intento de evitación10.
En los últimos años se ha avanzado en el conocimiento de la fisiopatología de la DCA y de los diferentes grupos de alérgenos11. Esta información brinda la oportunidad de plantearse tratamientos dirigidos avanzados, fuera de ficha técnica, para el control de la DCA refractaria a la evitación de los alérgenos identificados. Durante la fase inicial del proceso de hipersensibilidad de tipo IV, el sistema inmune innato participa de forma activa tras la formación del complejo antigénico, induciendo la liberación de citoquinas como la IL-1α, IL-1β, TNF-α, IL-8, IL-18 y el factor estimulante de colonias de granulocitos y macrófagos12. Previamente a la fase de sensibilización la célula presentadora de antígenos captará el hapteno para presentarlo a los linfocitos T naíf del ganglio linfático regional, que pueden reconocerlo y activar la vía Th1 si se libera IL-12, Th2 si se libera IL4, Th17 si se libera IL-17 o IL-23, o bien Th22 si se libera IL-2213,14. También es posible la activación de linfocitos T reguladores. En la última década se ha definido de forma más precisa la especificidad inflamatoria de algunos alérgenos, como el sulfato de níquel y las citoquinas de tipo Th1 y Th17, las fragancias y la inflamación predominantemente de tipo Th2, y el caucho (goma) relacionado con la inflamación de tipo Th2 y Th2214. En la tabla 1 se recogen los principales alérgenos estudiados desde un punto de vista molecular y las vías inflamatorias que activan.
Entendiendo que la asignación de perfiles inmunogénicos específicos a cada alérgeno (o grupo de ellos) puede ser compleja, y que probablemente hablamos de predominancias inflamatorias, no deja de ser interesante el uso de fármacos con dianas terapéuticas concretas en estos pacientes. Actualmente, y a grosso modo, podemos clasificar las opciones terapéuticas en dos grupos: inhibidores de moléculas pequeñas como los inhibidores de la Janus cinasa (iJAK), y las terapias biológicas (anticuerpos monoclonales dirigidos frente a la IL-4, 13, 17, 12, 23, inmunoglobulina E [IgE], y TNF-α). Ninguno de estos tratamientos comercializados está aprobado para el tratamiento de la DCA, por lo tanto, su solicitud será fuera de ficha técnica u off label8.
En esta revisión se excluyó el estudio de los inmunosupresores clásicos, tales como los corticoides, la ciclosporina, el metotrexato, el micofenolato o la azatioprina, en el tratamiento de la DCA15. Esta decisión se tomó debido a que estos no representan tratamientos novedosos.
Material y métodosSe realizó una revisión narrativa de la literatura en PubMed hasta el 28 de julio de 2024, utilizando términos específicos relacionados con la DCA y las nuevas terapias: «dermatitis de contacto alérgica», «alérgenos», «reacción de hipersensibilidad retardada», «prueba del parche», «inhibidores de Jak», «iJak», «biológicos», «terapia biológica», «anticuerpos monoclonales», «abrocitinib», «tofacitinib», «upadacitinib», «baricitinib», «ruxolitinib», «delgocitinib», «apremilast», «roflumilast», «crisaborol», «difamilast», «dupilumab», «tralokinumab», «nemolizumab», «lebrikizumab», «secukinumab», «ustekinumab», «omalizumab», «anti-TNF», «infliximab», «adalimumab», «etanercept», «certolizumab» y «certolizumab pegol». Se incluyeron estudios en inglés y español que evaluaban la eficacia y seguridad de los inhibidores de moléculas pequeñas y fármacos biológicos en DCA. Se excluyeron estudios centrados en tratamientos tradicionales, como corticosteroides e inmunosupresores clásicos, dada su naturaleza no novedosa. Los artículos fueron seleccionados basándose en la relevancia de sus resúmenes y se evaluaron detalladamente tras la lectura completa de los mismos.
Inhibidores de moléculas pequeñasInhibidores de JAK (iJAK): abrocitinib, tofacitinib, upadacitinib, baricitinib, ruxolitinib y delgocitinibLa vía de señalización intracelular Janus kinase/signal transducer and activator of transcription (JAK/STAT) se inicia cuando un ligando extracelular se une a receptores transmembrana, lo que conduce a la fosforilación de moléculas intracelulares. Esto desencadena una cascada de señalización intracelular y regula la transcripción de numerosos genes. Las JAK forman parte de esta familia de tirosincinasas que funcionan como transductores de señal intracelular e incluyen JAK1, JAK2, JAK3 y TYK2. Las JAK forman dímeros en la porción intracitoplasmática de los receptores de citoquinas, lo que les permite asociarse con múltiples receptores y activarse por diferentes citoquinas. A su vez, activan diversas proteínas STAT, como STAT1, STAT2, STAT3, STAT4, STAT5a, STAT5b y STAT6, participando así en funciones biológicas específicas. Cuando estas proteínas STAT se activan, se asocian formando dímeros y pueden translocarse al núcleo de la célula. Allí, actúan como factores de transcripción, regulando al alza la expresión de genes responsables de la producción de citoquinas proinflamatorias y factores de crecimiento, así como regulando el comportamiento de otras proteínas intracelulares16. Los iJAK han emergido como una clase terapéutica con múltiples aplicaciones en dermatología (vitíligo, alopecia areata, psoriasis y dermatitis atópica)17,18. Se postula que los iJAK podrían ser una opción terapéutica prometedora en casos resistentes a las terapias convencionales de la DCA19. Estos fármacos han demostrado influir en múltiples vías inflamatorias, incluidas las vías TH1, TH2 y TH17 que están implicadas en la fisiopatología de la DCA20. La eficacia de los iJAK puede variar según el alérgeno específico involucrado, lo que destaca la importancia de una evaluación individualizada. Aunque la investigación clínica en este campo aún es limitada, se han documentado casos donde el tratamiento con iJAK mostró resultados alentadores. Por ejemplo, el uso de abrocitinib a una dosis de 100mg cada 24h en un varón de 37 años con DCA aerotransportada causada por partículas de plantas de la familia Compositae (Asteraceae), con exposición ocupacional en un entorno laboral donde la evitación del alérgeno era inviable, resultó en una resolución completa de los síntomas tras 8 meses de tratamiento sin presentar efectos adversos21. Este paciente había presentado una falta de respuesta previa al tratamiento con dupilumab 300mg cada 2 semanas durante 11 meses, lo que sugiere que el alérgeno en cuestión activa otras vías inflamatorias no relacionadas con la vía Th2.
Otro caso clínico publicó el éxito terapéutico de tofacitinib 5mg cada 12h tras 4 semanas de tratamiento sin presentar efectos secundarios en una paciente india de 57 años con DCA de patrón aerotransportado a Parthenium, un género de plantas de la familia Compositae (Asteraceae)22. Esta paciente había realizado tratamiento previo con corticoides tópicos y orales, tacrolimus 0,1% tópico y azatioprina sin respuesta. Estos hallazgos respaldan la viabilidad de los iJAK como una opción terapéutica en casos seleccionados de DCA.
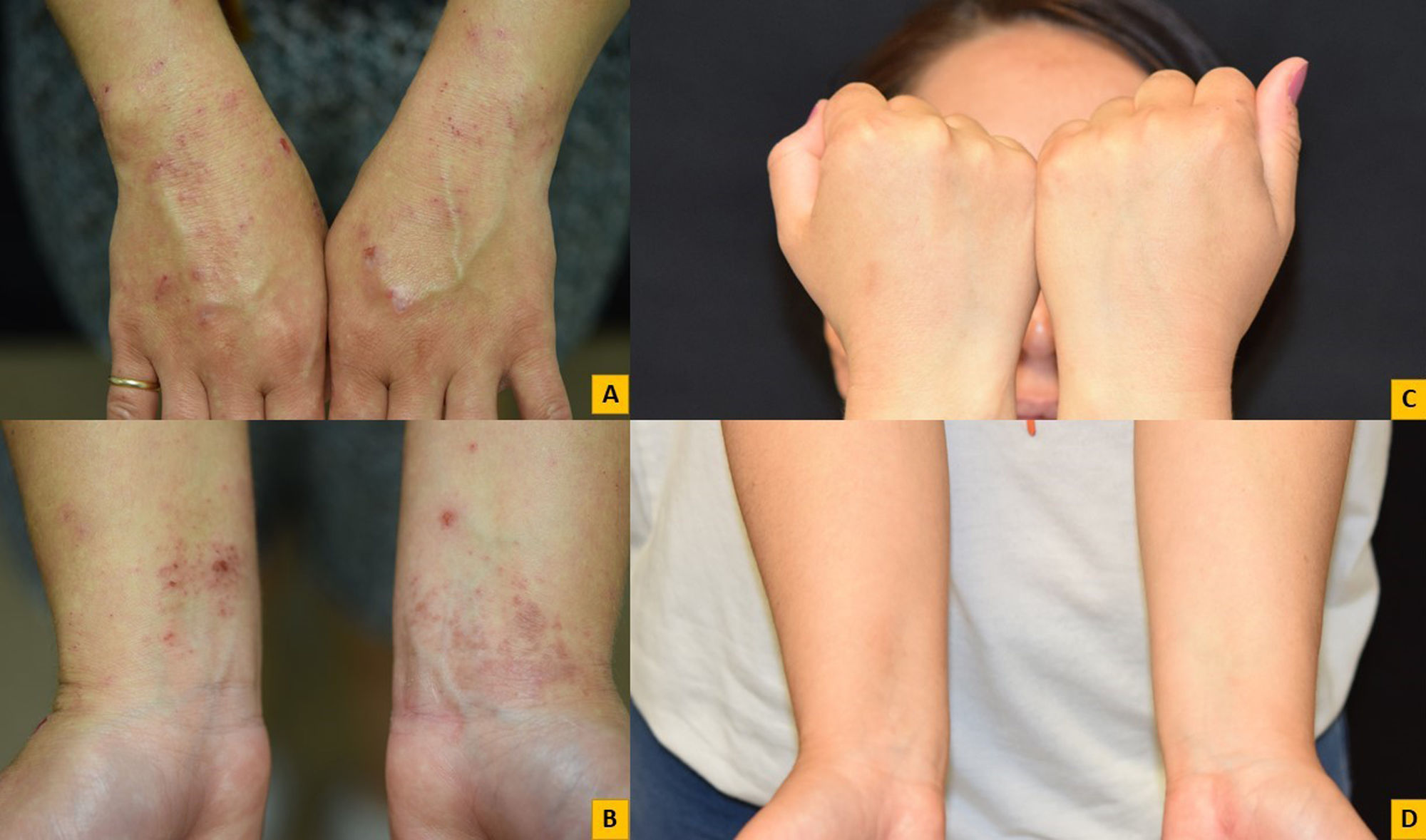
Recientemente se han publicado 2 casos de pacientes con psoriasis y DCA a la mezcla de fragancias I y bálsamo de Perú, con buena respuesta a upadacitinib 15mg al día23. El uso de upadacitinib 30mg también mostró silenciar la reacción alérgica de múltiples alérgenos (corticosteroides, lanolina, thiuram mix, resina de 4-terc-butilfenolformaldehído) al repetir las pruebas epicutáneas en la misma paciente después de estar 4 meses en tratamiento con upadacitinib 30mg24. Esto es importante no solo por el hecho de plantear que pueda ser una herramienta terapéutica interesante, sino también para no realizar las pruebas epicutáneas en pacientes que reciben este tipo de fármacos, por el elevado riesgo de falsos negativos. Nosotros tenemos experiencia con el tratamiento de DCA a aceleradores de la goma (mezcla thiuram, mezcla carba y mercaptobenzotiazol) en una paciente refractaria a ciclosporina, que respondió completamente a las 4 semanas de tratamiento con baricitinib 2mg/24h (fig. 1). No hemos encontrado ningún caso publicado de DCA tratado con ruxolitinib ni delgocitinib tópicos, pero sospechamos que tras su comercialización sí se publiquen nuevos casos de DCA tratados con estos fármacos tópicos. En la tabla 2 se resumen los hallazgos encontrados acerca de los iJAK en el tratamiento de la DCA.
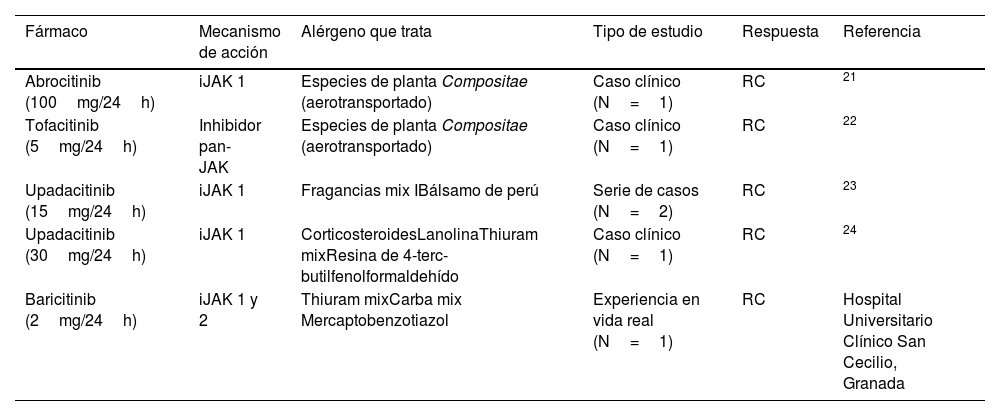
iJAK: fármaco, mecanismo de acción, DCA con sensibilización a alérgeno con relevancia presente que es capaz de tratar o silenciar en pruebas epicutáneas, tipo de estudio, respuesta y referencia
| Fármaco | Mecanismo de acción | Alérgeno que trata | Tipo de estudio | Respuesta | Referencia |
|---|---|---|---|---|---|
| Abrocitinib (100mg/24h) | iJAK 1 | Especies de planta Compositae (aerotransportado) | Caso clínico (N=1) | RC | 21 |
| Tofacitinib (5mg/24h) | Inhibidor pan-JAK | Especies de planta Compositae (aerotransportado) | Caso clínico (N=1) | RC | 22 |
| Upadacitinib (15mg/24h) | iJAK 1 | Fragancias mix IBálsamo de perú | Serie de casos (N=2) | RC | 23 |
| Upadacitinib (30mg/24h) | iJAK 1 | CorticosteroidesLanolinaThiuram mixResina de 4-terc-butilfenolformaldehído | Caso clínico (N=1) | RC | 24 |
| Baricitinib (2mg/24h) | iJAK 1 y 2 | Thiuram mixCarba mix Mercaptobenzotiazol | Experiencia en vida real (N=1) | RC | Hospital Universitario Clínico San Cecilio, Granada |
DCA: dermatitis de contacto alérgica; RC: respuesta completa.
No hemos encontrado datos para delgocitinib, ruxolitinib, roflumilast ni difamilast. Crisaborol tópico puede producir DCA29,30.
La fosfodiesterasa 4 (PDE4) es una enzima encargada de la degradación del monofosfato de adenosina cíclico (AMPc), lo que promueve la producción de mediadores inflamatorios (citoquinas: TNF-α, IL-1β, e IL-6) y la activación de células inmunitarias (linfocitos T, macrófagos y mastocitos) a nivel sistémico y epidérmico. El uso de iPDE4 en la DCA ayudaría a limitar la respuesta inflamatoria y a conservar la función barrera cutánea frente a los alérgenos e irritantes. Apenas existen publicaciones acerca de su uso en DCA. Apremilast se empleó en un ensayo abierto en fase 2 para DCA recalcitrante y/o DA, en el que participaron 10 pacientes a dosis de 20mg 2 veces al día por un período de 12 semanas, de los cuales 4 pacientes presentaban DCA y en un paciente coexistían DCA y DA25. El principal objetivo se fijó en una mejoría de 2 puntos del IGA (Investigator Global Assessment), alcanzándose en el 20% de los sujetos. Solo el 10% alcanzó el EASI-75 (Eczema Assessment Severity Index-75), por lo que se concluyó su escaso efecto para estos pacientes en comparación con los resultados obtenidos en psoriasis25. Sin embargo, en este ensayo se observó un hallazgo interesante: los sujetos con diagnóstico de DCA respondieron mejor al tratamiento con apremilast en comparación con los pacientes con DA. Los pacientes con DCA mostraron una mejoría promedio del 40% en la puntuación del EASI, mientras que los pacientes con DA experimentaron un empeoramiento del 20% (p=0,026). Además, los sujetos con DCA presentaron una disminución del prurito del 30%, en contraste con una reducción del 10% en los pacientes con DA. Sin embargo, esta diferencia en el prurito no fue estadísticamente significativa, probablemente debido al pequeño tamaño muestral. Este hallazgo sugiere que apremilast podría ser más eficaz en el tratamiento de la DCA que en la DA, aunque cabe destacar que los pacientes con DCA presentaban puntuaciones iniciales más bajas en el índice EASI, con una media de 12,5, en comparación con los pacientes con DA, quienes tenían una media de 34,1; por lo que se necesita un mayor número de pacientes para confirmar estos resultados25.
Roflumilast es un fármaco indicado para la enfermedad pulmonar obstructiva crónica (EPOC) que ha demostrado resultados prometedores en el tratamiento de aftosis oral recurrente, liquen plano, psoriasis y DA, entre otros26. Un ensayo clínico en fase IIa (NCT04773587) con roflumilast en crema al 0,15% y al 0,015% versus placebo ha demostrado un buen perfil de seguridad con disminución del EASI de 6,4 puntos en el grupo de roflumilast al 0,15%, de 6 puntos en el grupo de roflumilast al 0,05% y de 4,8 puntos en el grupo control, sin resultar estadísticamente significativo, en adultos y niños por encima de 6 años con DA leve-moderada27. Sin embargo, en otro ensayo clínico en fase IIa (NCT01856764) con roflumilast tópico al 0,5% versus placebo en DA no se alcanzaron resultados superiores a placebo en el grupo con roflumilast28. A pesar de la ausencia de evidencia de eficacia de roflumilast en la DCA, su perfil de seguridad y potencial antiinflamatorio pueden motivar su uso en casos seleccionados.
Respecto a otros fármacos tópicos, crisaborol es el primer iPDE4 aprobado para la DA desde 2020 para mayores de 3 meses de edad como tratamiento ahorrador de corticoides. No se han encontrado publicaciones sobre su uso en DCA; de hecho, hay 2 artículos recientes que lo postulan como potencial alérgeno29,30. Difamilast es otro iPDE4 tópico actualmente en estudio en fase 3 para el tratamiento de la DA, aprobado en Japón desde el 2021 para mayores de 2 años. Ha demostrado efecto antiinflamatorio y antipruriginoso de rápida actuación desde la primera semana de tratamiento31. Tampoco hemos encontrado datos sobre su uso en DCA.
Terapia biológicaDupilumabDupilumab, un inhibidor del receptor alfa de la interleucina 4 (IL-4Rα), está aprobado para tratar la DA moderada a grave. Posiblemente, de todas las moléculas revisadas, dupilumab es la que más evidencia científica tiene publicada. Como se ha planteado en varios artículos, algunos alérgenos están inmunomediados por la inflamación de tipo Th2, motivo por el cual se plantea el uso de dupilumab en DCA32. Actualmente, se encuentra en fase de reclutamiento un ensayo clínico para evaluar el tratamiento de la DCA (NCT03935971)33. Por otro lado, en el ensayo clínico que evalúa la eficacia y seguridad de dupilumab frente a placebo en pacientes con eczema crónico grave de manos con respuesta inadecuada o intolerancia a alitretinoína, el 90% de los pacientes tratados con dupilumab mostraban hipersensibilidad alérgica a al menos una sustancia con una mejoría del 75% en la puntuación del Hand Eczema Severity Index (HECSI-75) en la semana 16 del 95% de los pacientes tratados con dupilumab frente al 33% de los pacientes tratados con placebo34. El éxito terapéutico publicado de dupilumab en DCA aumentó el interés por el uso de esta terapia en pacientes con pruebas epicutáneas positivas relevantes y refractarios a la evitación del alérgeno35–37. Casos aislados y series de casos de DCA parcheados con pruebas positivas han sido analizados antes y después de dupilumab38. Alérgenos como las gomas39, la mezcla de lactonas sesquiterpénicas40,41, dicromato potásico42, isobornil acrilato (IBOA)43, e incluso el síndrome de alergia sistémica por sulfato de níquel y bálsamo de Perú fueron tratados con éxito con dupilumab44. Un estudio multicéntrico nacional mostró que más de la mitad de los pacientes parcheados antes y después de estar bajo tratamiento con dupilumab mostraban falsos negativos45. En este aspecto debe considerarse suspender el tratamiento con dupilumab 2 semanas antes de la realización de las pruebas epicutáneas, sobre todo en aquellos con brotes frecuentes de eczema y/o que presenten dermatitis persistente localizada (como por ejemplo el área facial). Por el impacto que supone sufrir una DCA ocupacional, y en ocasiones la dificultad que ofrece el caso para una resolución de la dermatitis, dupilumab también ha sido utilizado con éxito en 6 pacientes46 o en casos de polisensibilización en una peluquera47. Aunque posiblemente controvertido, dupilumab es una opción interesante en pacientes sensibilizados a alérgenos cuya predisposición inmunogénica es de tipo Th2. Aunque probablemente sean tratamientos válidos para el tratamiento de la DCA, no hay publicaciones de tralokinumab, nemolizumab ni lebrikizumab hasta la fecha. En la tabla 3 se resumen los principales estudios relacionados con dupilumab y el tratamiento de la DCA.
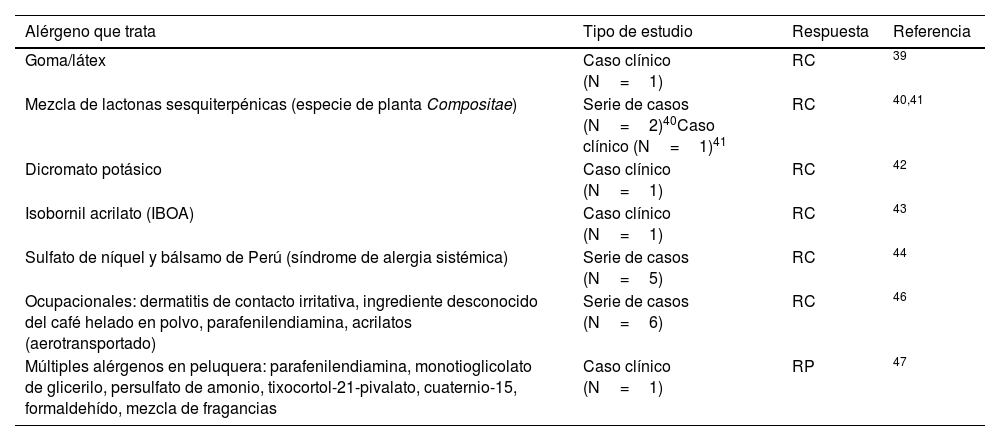
Dupilumab. DCA con sensibilización a alérgeno con relevancia presente que es capaz de tratar, tipo de estudio, respuesta y referencia
| Alérgeno que trata | Tipo de estudio | Respuesta | Referencia |
|---|---|---|---|
| Goma/látex | Caso clínico (N=1) | RC | 39 |
| Mezcla de lactonas sesquiterpénicas (especie de planta Compositae) | Serie de casos (N=2)40Caso clínico (N=1)41 | RC | 40,41 |
| Dicromato potásico | Caso clínico (N=1) | RC | 42 |
| Isobornil acrilato (IBOA) | Caso clínico (N=1) | RC | 43 |
| Sulfato de níquel y bálsamo de Perú (síndrome de alergia sistémica) | Serie de casos (N=5) | RC | 44 |
| Ocupacionales: dermatitis de contacto irritativa, ingrediente desconocido del café helado en polvo, parafenilendiamina, acrilatos (aerotransportado) | Serie de casos (N=6) | RC | 46 |
| Múltiples alérgenos en peluquera: parafenilendiamina, monotioglicolato de glicerilo, persulfato de amonio, tixocortol-21-pivalato, cuaternio-15, formaldehído, mezcla de fragancias | Caso clínico (N=1) | RP | 47 |
DCA: dermatitis de contacto alérgica; RC: respuesta complete; RP: respuesta parcial.
El secukinumab es un anticuerpo monoclonal IgG1 kappa completamente humano dirigido contra la IL-1748. Los niveles de IL-17 fueron elevados en ratones y sujetos humanos que presentaron una reacción positiva en la prueba de parche al níquel. Estos niveles más altos de IL-17 en estos sujetos indican la participación de la IL-17 en la manifestación de la DCA14,49. Basándose en este hallazgo, se probó el secukinumab en la DCA. Sin embargo, en la práctica clínica, la terapia con secukinumab no mostró ninguna mejora clínica sustancial50.
UstekinumabEl ustekinumab es un anticuerpo monoclonal humano IgG1k que bloquea la actividad biológica de la IL-12 e IL-23 al inhibir los receptores de estas citoquinas en células T, células NK y células presentadoras de antígenos, citoquinas relevantes para la diferenciación Th151. Recientemente se ha destacado el probable papel de la IL-23 en la DCA52. Cuando se administró ustekinumab a 5 pacientes con DCA recalcitrante, solo un paciente mostró mejoría clínica53. En nuestra opinión, la futura comercialización de ustekinumab biosimilar podrá suponer una interesante opción terapéutica en pacientes sensibilizados a alérgenos cuya vía inmunogénica predominante sea Th1, donde la IL-12 juega un papel crucial en la diferenciación de los linfocitos T naíf a Th1.
OmalizumabOmalizumab es un anticuerpo monoclonal dirigido frente a la IgE, aprobado para el tratamiento de la urticaria crónica y asma alérgica grave. Respecto a su uso fuera de ficha técnica, se han publicado casos de DA, penfigoide ampolloso, enfermedad de Kimura y síndrome hiper-IgE con buena respuesta54. Por su mecanismo de acción, no interfiere en el resultado de las pruebas epicutáneas. Aquellos pacientes que sufran una dermatitis de contacto por proteínas mediada por IgE (hipersensibilidad tipo I), omalizumab podría ser una opción terapéutica interesante, sobre todo en aquellos casos de origen ocupacional. Existe una publicación de un caso de dermatitis ocupacional recalcitrante asociada a asma alérgica secundaria a la exposición al trigo. Omalizumab 225mg cada 2 semanas resultó eficaz en el control de la DCA sin evitación del alérgeno55. La respuesta favorable al tratamiento puede deberse al mecanismo de hipersensibilidad combinado tipo I y IV, lo que abre una ventana de oportunidad terapéutica para las DCA por proteínas. Tenemos experiencia en el tratamiento de pacientes con intolerancia innata a fragancias en general, sin mostrar sensibilización positiva durante las pruebas epicutáneas, con mejoría de los síntomas de forma significativa y mejorando la calidad de vida de estos pacientes.
Inhibidores del factor de necrosis tumoral α (anti-TNFα): infliximab, adalimumab, etanercept y certolizumab-pegolEl TNF-α por diferentes mecanismos contribuye al desarrollo de la DCA. Durante la sensibilización, promueve la activación y migración de células presentadoras de antígenos, facilitando la presentación del alérgeno a las células T. En la fase de elicitación estimula la liberación de citoquinas proinflamatorias y quimiocinas, lo que resulta en una mayor infiltración de células inflamatorias y amplificación de la respuesta inflamatoria15. No obstante, el uso de anti-TNFα ha demostrado ser insuficiente en el bloqueo de la DCA, lo que sugiere que hay otras vías implicadas que actuarían en compensación. La mayoría de los estudios en pacientes en tratamiento biológico con estos fármacos no demuestran negativización de las pruebas epicutáneas56,57. Por otra parte, la inyección subcutánea del fármaco puede inducir cambios histopatológicos similares a una reacción de hipersensibilidad de contacto, tales como proliferación local de fibroblastos y capilares en la dermis, reacción hiperplásica de queratinocitos o necrosis masiva en la epidermis58.
Solo hay disponible un caso de un varón de 30 años con antecedente personal de atopia y sensibilización a sulfato de níquel y bicromato de potasio con buena respuesta a infliximab59, demostrando ser eficaz en disminuir la extensión de las lesiones y el prurito asociado con buena tolerancia al tratamiento; sin embargo, este artículo fue publicado el 2006, previo a la comercialización de las nuevas terapias en DA59.
DiscusiónLa DCA es una patología compleja cuya fisiopatología involucra la activación del sistema inmunológico mediada por células T en respuesta a alérgenos específicos12. La evitación de los alérgenos que muchas veces no es posible y los tratamientos tradicionales, como los corticosteroides y los inhibidores de calcineurina tópicos o los inmunosupresores clásicos, han demostrado eficacia en muchos casos, pero presentan limitaciones en términos de efectos secundarios y respuesta incompleta en algunos pacientes15.
Los iJAK representan una terapia emergente prometedora debido a su capacidad para modular múltiples vías inflamatorias simultáneamente. Este mecanismo es especialmente relevante en pacientes polisensibilizados a múltiples alérgenos, donde pueden estar involucradas tanto las vías TH1, TH2 como TH17. Los casos revisados muestran una reducción significativa en los síntomas de DCA, con un perfil de seguridad favorable a corto plazo21–23. Además, los iJAK que se han utilizado en estos pacientes han sido administrados a la menor dosis comercializada, incluyendo nuestra experiencia con un paciente tratado con baricitinib 2mg al día, lo que es interesante desde el punto de vista de la relación coste-eficacia21,22. A pesar de esto, el poco número de pacientes y el seguimiento realizado a corto plazo limitan la generalización de estos hallazgos.
Apremilast podría ser una opción terapéutica prometedora, sin embargo, solo hay un ensayo clínico que demuestra eficacia en un número limitado de pacientes25.
Comparativamente, las terapias biológicas, como los inhibidores de IL-4/IL-13, también muestran resultados alentadores en el manejo de la DCA refractaria39–44,46,47. Sin embargo, en la práctica clínica real, hay menos informes de casos exitosos con fármacos biológicos anti-IL-17 y anti-IL-23, a pesar de su potencial utilidad en la DCA50,53. El conocimiento de las firmas moleculares de los alérgenos es fundamental para la elección del tratamiento según la vía inflamatoria que active13,14; por esta razón, la respuesta de los pacientes con DCA a estos tratamientos varía.
El mecanismo de inhibición de la vía OX40/OX40L podría ser particularmente interesante en la prevención del desarrollo de la DCA debido a su papel crucial en la regulación de la respuesta inmunitaria adaptativa, específicamente en la activación y proliferación de las células T60. Esta diana terapéutica se está investigando actualmente para el tratamiento de la DA61. Será interesante conocer el papel preventivo que tienen estas moléculas en el desarrollo de la DCA en estos pacientes.
La personalización del tratamiento basada en el perfil inmunológico del paciente podría optimizar los resultados terapéuticos. En pacientes con comorbilidades como atopia, alopecia areata, psoriasis o hidradenitis, o en aquellos polisensibilizados donde no es posible evitar el alérgeno, los iJAK podrían ofrecer una opción terapéutica valiosa21–23.
LimitacionesEste artículo presenta algunas limitaciones que deben ser reconocidas. La presente revisión tiene la limitación de ser narrativa y no una revisión sistemática o metaanálisis. La mayoría de estudios incluidos son casos o series de casos relativamente recientes y carecen de datos a largo plazo sobre seguridad y eficacia y, por otro lado, en algunos pacientes coexiste DA y DCA.
Además, la variabilidad en la respuesta de los pacientes a los tratamientos puede complicar la generalización de los hallazgos. La falta de estudios comparativos directos entre las diferentes opciones terapéuticas emergentes y los tratamientos convencionales es una limitación significativa. Por último, se requiere más investigación para identificar biomarcadores que puedan predecir la respuesta al tratamiento y guiar la personalización del manejo de la DCA.
ConclusionesLas terapias emergentes para la DCA, como los iJAK y las terapias biológicas, muestran un gran potencial para mejorar el manejo de esta condición refractaria. No obstante, se necesitan más datos para establecer su lugar en la práctica clínica rutinaria. Los iJAK, al actuar de forma más transversal inhibiendo múltiples citoquinas, serían los fármacos más prometedores en cuanto a eficacia; por otro lado, dupilumab sería una opción terapéutica en aquellos pacientes en los que coexiste dermatitis atópica y sensibilización a alérgenos con polarización de la respuesta inflamatoria predominantemente Th2. La personalización del tratamiento, basada en el perfil inmunológico y la identificación de biomarcadores predictivos, es un área de investigación prometedora que podría optimizar los resultados clínicos y mejorar la calidad de vida de los pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.