Un paciente de 9 años fue remitido a las consultas de Dermatología por la aparición de lesiones puntiformes y rugosas al tacto, en cejas, mejillas y ambos brazos. Entre los antecedentes personales destacaba la presencia de dermatitis atópica, rinitis, asma y un ganglioglioma temporo-mesial izquierdo. El paciente recibió tratamiento para la neoplasia cerebral con cirugía y radioterapia local. Posteriormente, dada la presencia de la mutación BRAF V600E en las células tumorales del ganglioglioma, se decidió iniciar dabrafenib, inhibidor de BRAF, a dosis de 150mg cada 12 h. Tres meses después de iniciar el tratamiento comenzó con las manifestaciones cutáneas, para las cuales el paciente no había realizado ningún tratamiento previo.
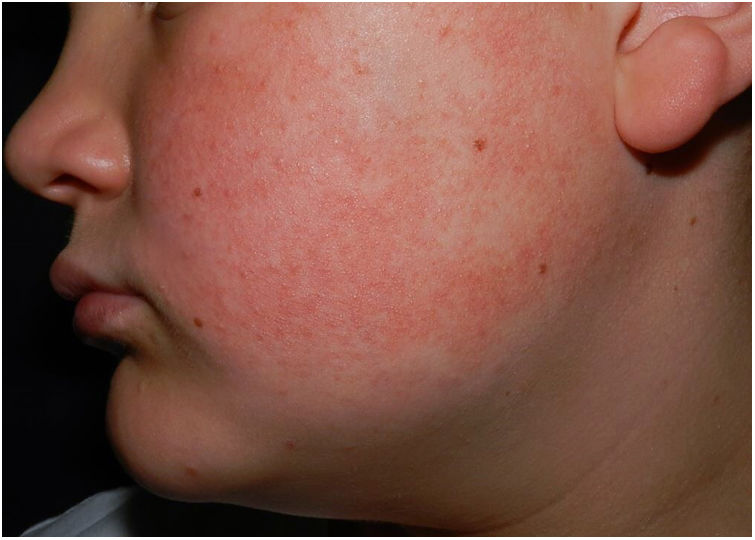
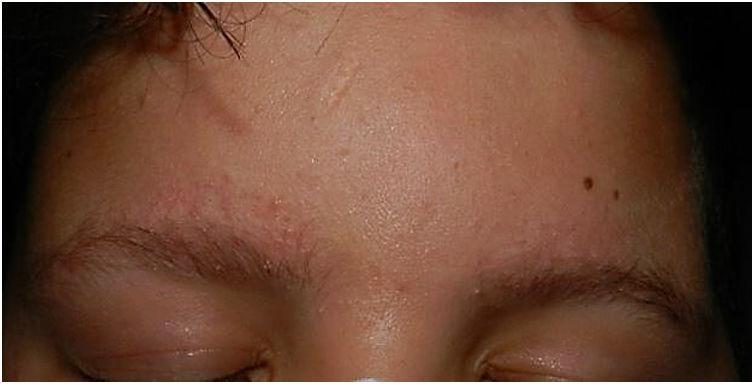
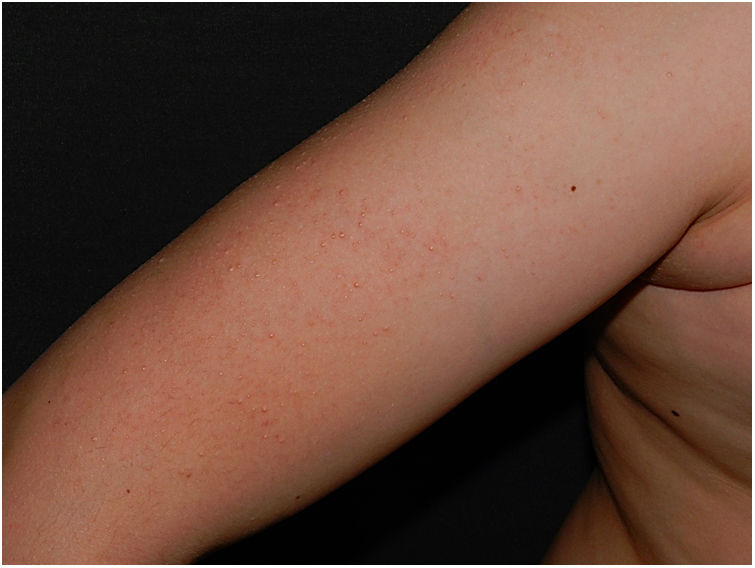
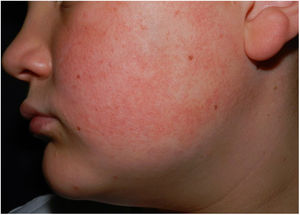
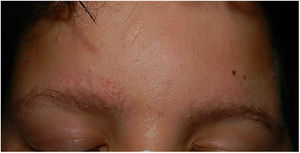
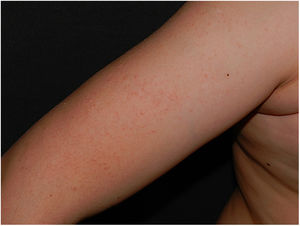
En el examen físico se observaron pápulas hiperqueratósicas milimétricas sobre fondo eritematoso en ambas mejillas (fig. 1) y cejas (fig. 2), con pérdida de pelo en la zona medial de las mismas. Así como, múltiples pápulas hiperqueratósicas en la cara externa de ambos brazos (fig. 3). No presentaba lesiones en otras zonas del cuerpo ni en las mucosas.
Por la historia clínica y las manifestaciones cutáneas. se llegó al diagnóstico de reacción cutánea tipo uleritema ofriógenes, también denominado «queratosis folicular atrófica de la cara»; una dermatosis poco frecuente caracterizada por pápulas foliculares eritematosas que afectan predominantemente a las cejas, la frente y las mejillas, con evolución ocasional hacia la atrofia y la alopecia. Puede aparecer durante la infancia o en la edad adulta1,2.
El diagnóstico diferencial se realiza con un grupo de trastornos estrechamente interrelacionados conocidos como queratosis pilar atrófica, del que forman parte la atrofodermia vermiculada y la queratosis espinulosa decalvante1,2.
El uleritema ofriógenes es considerado un marcador cutáneo de varios síndromes congénitos, entre los que se encuentran: el síndrome de Noonan, el síndrome de Cornelia de Lange, el síndrome de Rubinstein-Taybi, la monosomía parcial del brazo corto del cromosoma 18, anomalías nerviosas, enfermedades oculares y retardos mentales. Es considerada una genodermatosis autosómica dominante con penetrancia incompleta1-3.
Las mutaciones en BRAF V600E son comunes en los gangliogliomas cerebrales y se dan en aproximadamente el 50% de los pacientes, resultando en una peor supervivencia libre de progresión en comparación con los gangliogliomas que no la presentan. Estas mutaciones han generado un gran interés y se han convertido en dianas terapéuticas susceptibles de ser tratados con los inhibidores de BRAF, como el dabrafenib4.
En cuanto a los inhibidores de BRAF, pioneros en el tratamiento dirigido para el melanoma metastásico, y posteriormente con otras indicaciones terapéuticas, son tratamientos con un perfil de seguridad complejo, relacionándose con un amplio espectro de reacciones adversas cutáneas; mayoritariamente leves (grado 1 y 2)5-7. Entre las manifestaciones cutáneas más frecuentes destacan los exantemas cutáneos, la alopecia, el carcinoma epidermoide cutáneo, el queratoacantoma, la hiperqueratosis palmo-plantar, las reacciones tipo queratosis pilar y el prurito6,7. En lo que respecta al carcinoma epidermoide, se debe destacar que no se han observado casos con dabrafenib reportados en población pediátrica a diferencia de los adultos4.
La reacción tipo queratosis pilar suele afectar predominantemente a las superficies extensoras de los brazos y a la cara anterior de los muslos, pudiendo extenderse al tronco. La región facial se encuentra generalmente respetada6. La aparición de este efecto adverso se ha descrito en los primeros meses de inicio de tratamiento con dabrafenib, en cualquiera de sus indicaciones terapéuticas, notificándose según las últimas publicaciones en el 10 al 14% de los pacientes4,8. La reacción cutánea tipo queratosis pilar es más frecuente en pacientes que reciben tratamiento con vemurafenib (inhibidor BRAF) y, por el contrario, se ha descrito una menor incidencia en aquellos pacientes que reciben tratamientos combinados con los inhibidores BRAF/MEK7.
Khetarpal et al. reportaron, en el año 2016, el primer caso de queratosis pilar atrófica con relación al tratamiento con nilotinib, un inhibidor de la tirosina cinasa de segunda generación, en un paciente con leucemia mieloide crónica9.
Revisando en la literatura no se ha encontrado ningún caso de reacciones tipo queratosis folicular atrófica facial secundaria al tratamiento con dabrafenib. Presentamos, en este artículo, el primer caso reportado de una reacción adversa tipo uleritema ofriógenes en un niño de 9 años tras recibir tratamiento con dabrafenib dirigido a un ganglioglioma temporo-mesial. A pesar de que el uleritema ofriogenes se considere un marcador cutáneo de varios síndromes congénitos1,2, y no suela presentarse como un efecto secundario farmacológico, no fue el caso de este paciente y la relación temporal desde el inicio del fármaco apoyó el diagnóstico.
Este tipo de manifestaciones cutáneas suelen ser leves y de manejo sintomático, por lo que es importante distinguirlas de reacciones de hipersensibilidad a fármacos, más graves, que puedan requerir la interrupción de la medicación7,10. En cuanto al tratamiento, si bien hay casos de resolución espontánea hacia la adolescencia, se suelen emplear agentes queratolíticos, corticoides y medidas de fotoprotección, con una respuesta variable10. Recientemente, algunas publicaciones logran buenos resultados con el láser de colorante pulsado3.
FinanciaciónNo existe entidad financiadora.