Las queratosis actínicas (QA) son lesiones cutáneas frecuentes que surgen en la piel crónicamente expuesta a los rayos ultravioleta y que potencialmente pueden progresar a un carcinoma epidermoide cutáneo (CEC) infiltrante. Debido a que no se puede predecir qué lesiones progresarán a CEC ni cuándo, generalmente se recomienda el tratamiento de todas las QA. Existe un amplio abanico de tratamientos disponibles para la QA a los que se les han unido nuevas aprobaciones en los últimos años. Estos cambios en los tratamientos disponibles para la QA hacen necesaria la revisión de la evidencia científica y del estado actual del diagnóstico y manejo de la QA en España.
Actinic keratoses (AK) are common cutaneous lesions located in skin areas chronically exposed to UV radiation, with the potential of progressing into invasive squamous cell carcinoma (SCC). Since it is not possible to predict which AK lesions will become SCC or when will that happen, treating all AK is generally recommended. There is a wide range of therapies available for AK and new drug approvals have joined the therapeutic armamentarium in recent years. These changes in the available treatments for AK require a review of the scientific evidence available and the current status of AK diagnosis and management in Spain.
La queratosis actínica (QA) es una causa común de consulta dermatológica en España, llegando a representar un 6% de las consultas1. La mayoría de autores están de acuerdo en considerar la QA como una forma de carcinoma escamoso in situ de la piel2.
La prevalencia global de las QA es del 14%, según un metaanálisis de 60 estudios observacionales, y se estima una incidencia de 1,9 por 100.000 personas-año3. En España, la prevalencia de QA en pacientes de 45 años o más que acuden a consultas dermatológicas es del 28,6%, la cual aumenta con la edad (45,2%, 71-80 años)4.
La principal causa de las QA es la exposición crónica a la radiación ultravioleta (UV), especialmente la UV-B5. Este tipo de radiación induce mutaciones en el gen supresor de tumores p53, crucial para inducir la apoptosis de células dañadas, lo que lleva a una proliferación incontrolada de estas células y conduce a la aparición de QA2. Además, la radiación UV induce mutaciones en otros genes, como H-Ras (regulador de la proliferación celular), o el supresor de tumores p16, contribuyendo al desarrollo de la QA2,6,7. Por otro lado, infecciones por el virus del papiloma humano también podrían estar relacionadas con la QA2,8.
Aunque pocas QA evolucionan a carcinoma epidermoide cutáneo (CEC) invasivoinvasivo (0,07%-0,6% en el primer año y del 2,6% en 4años)9,10, es importante señalar que aproximadamente el 60-65% de los CEC infiltrantes surgen sobre QA9,10. Por ello, las QA se consideran un marcador de riesgo de CEC y el factor de riesgo independiente más importante para su desarrollo9,10. Aunque no todas las QA progresan a CEC, no existen marcadores fiables que permitan identificar las que lo harán. Cabe destacar, además, que algunas QA pueden regresar espontáneamente o persistir como QA sin progresar hacia la infiltración de la dermis11. La tasa de regresión espontánea varía entre el 15 y el 63% al año para lesiones individuales10,11. Sin embargo, las QA que involucionan pueden reaparecer, con una tasa de recurrencia estimada del 15-53% al año11.
Las últimas recomendaciones para la evaluación y tratamiento de los pacientes con QA en España fueron publicadas en 201712. Desde entonces, ha habido cambios relevantes tanto en su diagnóstico y estadificación como en su manejo, por lo que el objetivo de esta publicación es ofrecer una actualización del estado actual de la QA en nuestro país.
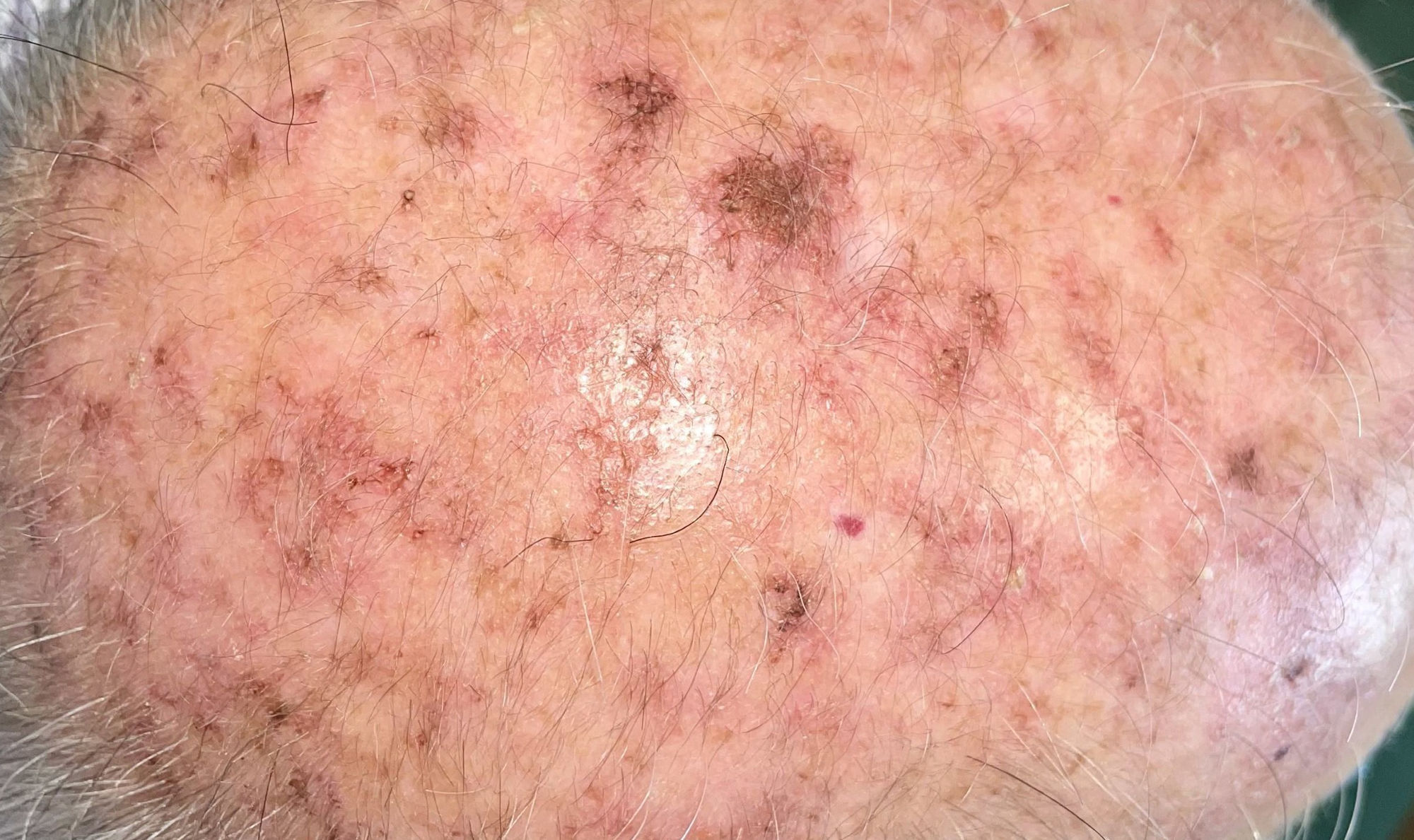
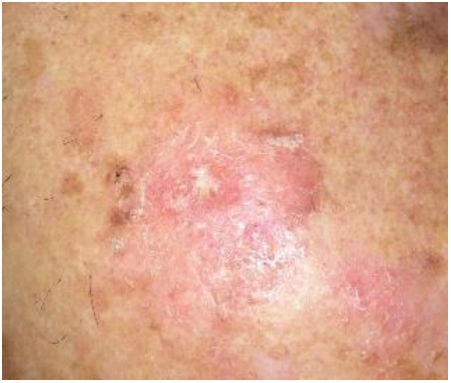
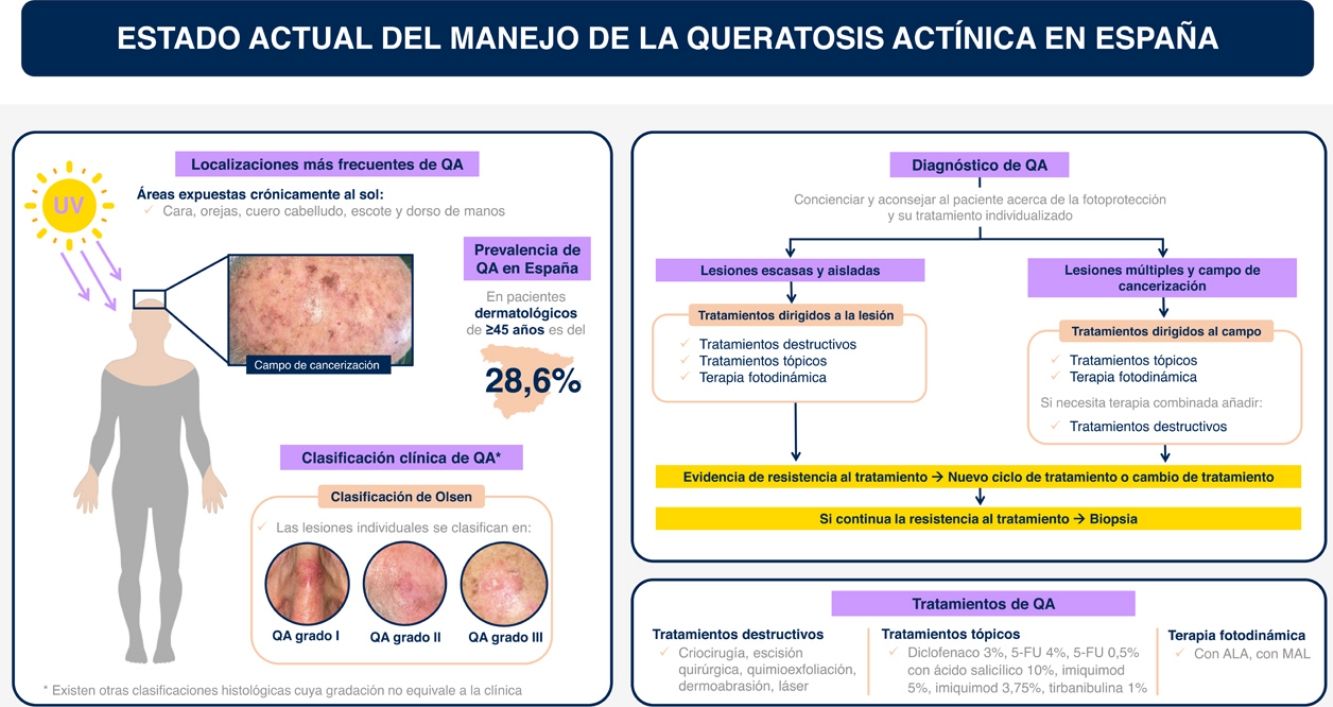
DiagnósticoDiagnóstico clínicoLas QA suelen presentarse cómo máculas, pápulas o placas no infiltradas, eritematosas o del color de la piel, con tacto rasposo y un tamaño de pocos mm a 2-3cm de diámetro12. Las localizaciones más frecuentes son las áreas expuestas crónicamente al sol: cara, orejas, cuero cabelludo (en personas con alopecia), escote y dorso de manos. Dependiendo de la intensidad o el predominio de ciertos signos, se pueden diferenciar algunas variantes clínicas como la forma hipertrófica o la pigmentada13,14.
La evaluación clínica presenta una sensibilidad del 98% y una especificidad del 62% para detectar QA15.
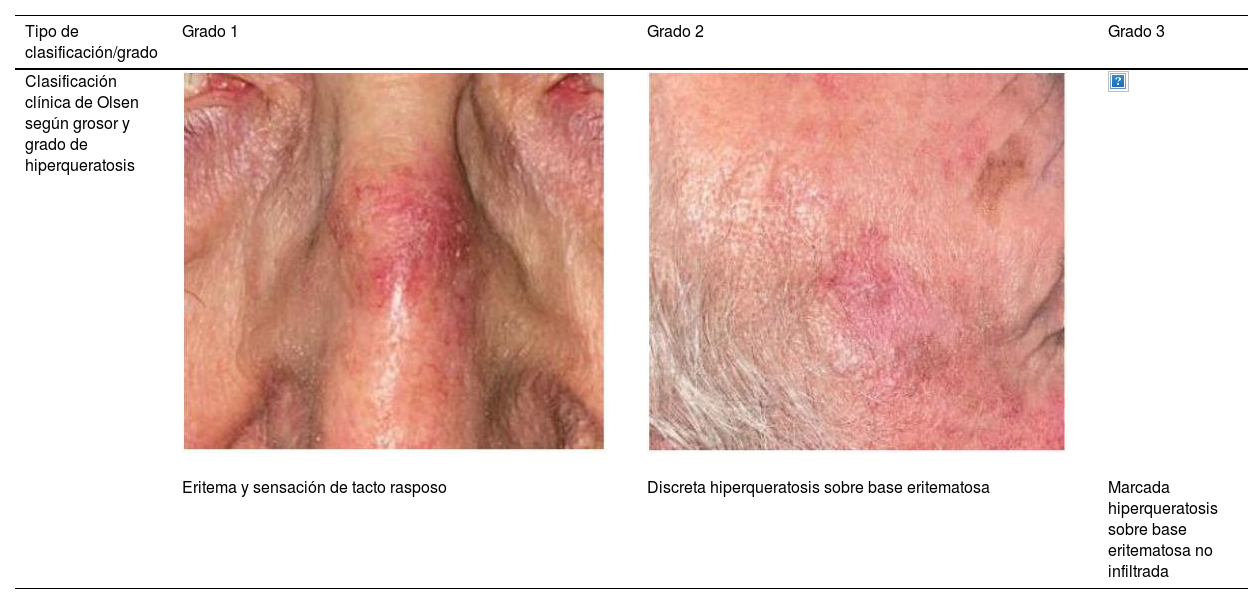
Las lesiones individuales de QA se pueden clasificar clínicamente según la escala de Olsen en grado 1 a 3 según el grosor y la hiperqueratosis (tabla 1)16. Un estudio de 2022 observó que el riesgo de progresión a CEC infiltrante en un área tratada fue de 3,7% a los 5 años, siendo superior en las QA hiperqueratósicas (grado 3 de Olsen) que en las QA grado 1/2 (20,9% vs. 2,4%)17.
Clasificaciones clínicas e histológicas de la QA
| Tipo de clasificación/grado | Grado 1 | Grado 2 | Grado 3 |
|---|---|---|---|
| Clasificación clínica de Olsen según grosor y grado de hiperqueratosis | |||
| Eritema y sensación de tacto rasposo | Discreta hiperqueratosis sobre base eritematosa | Marcada hiperqueratosis sobre base eritematosa no infiltrada |
| AKI | Budding (PROII) | Papillary sprouting (PROIII) | |
|---|---|---|---|
| Clasificación histológica según la extensión intraepidérmica de los queratinocitos atípicos (Röwer-Huber) | |||
| Queratinocitos atípicos limitados al tercio inferior de la epidermis | Queratinocitos atípicos en los 2 tercios inferiores de la epidermis | Queratinocitos atípicos en toda la epidermis |
| Crowding (PROI) | Budding (PROII) | Papillary sprouting (PROIII) | |
|---|---|---|---|
| Clasificación histológica según el patrón de crecimiento basal de los queratinocitos atípicos (PRO) | |||
| Los queratinocitos atípicos se concentran en la capa basal de la epidermis | Pequeños brotes de queratinocitos atípicos de la epidermis basal protruyen ligeramente hacia la dermis papilar | Hay un patrón de crecimiento basal pronunciado con grupos de queratinocitos atípicos formando papilas elongadas que protruyen en la dermis |
QA: queratosis actínica.
* La gradación de las tres clasificaciones no se correlacionan entre ellas.
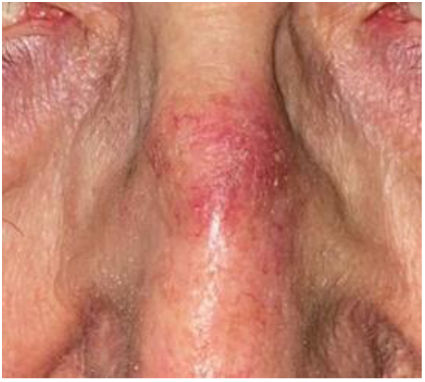
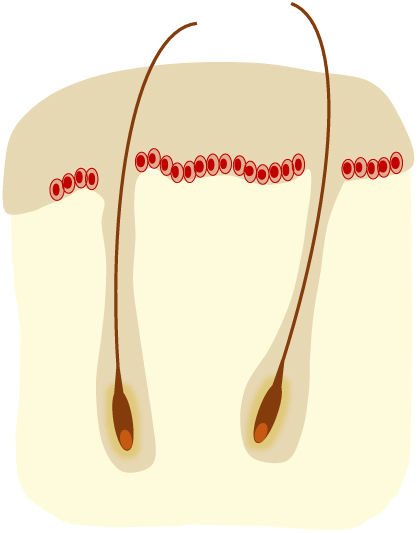
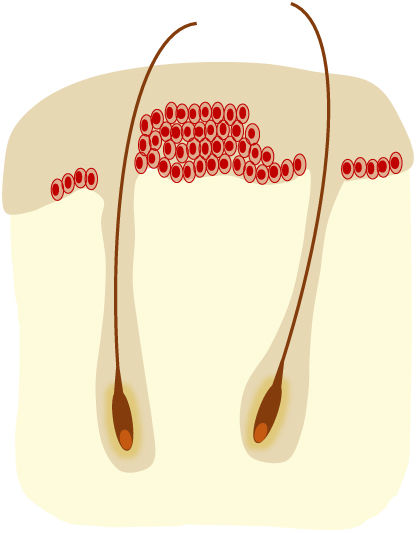
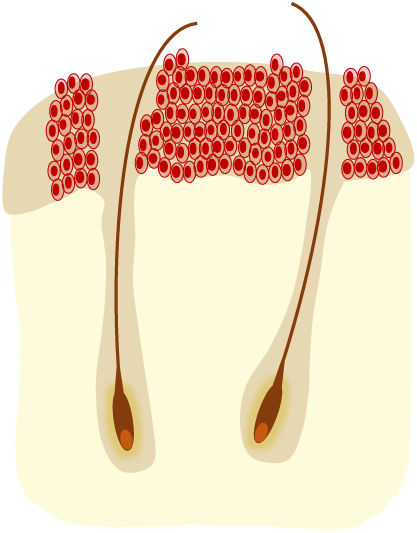
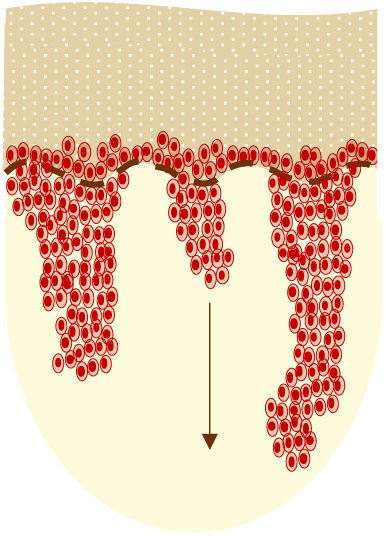
Las QA suelen ser, sin embargo, múltiples. En este sentido, el concepto de «campo de cancerización» hace referencia al área de piel dañada crónicamente por el sol, caracterizada por al menos 2de los siguientes signos: telangiectasias, atrofia, cambios pigmentarios y aspecto de papel de lija18. En esta área, se pueden encontrar QA visibles clínicamente (aunque no hay acuerdo sobre si su presencia es imprescindible o no), QA subclínicas (diagnosticables microscópicamente), grupos de queratinocitos con alteraciones genéticas (detectables por estudios moleculares) y áreas de piel normal (fig. 1). Hay que destacar que en la piel aparentemente normal se han descrito cambios histológicos y moleculares comunes a la QA y al carcinoma epidermoide18, lo que sugiere un probable beneficio de tratar no solo las QA individuales, sino también el campo de cancerización.
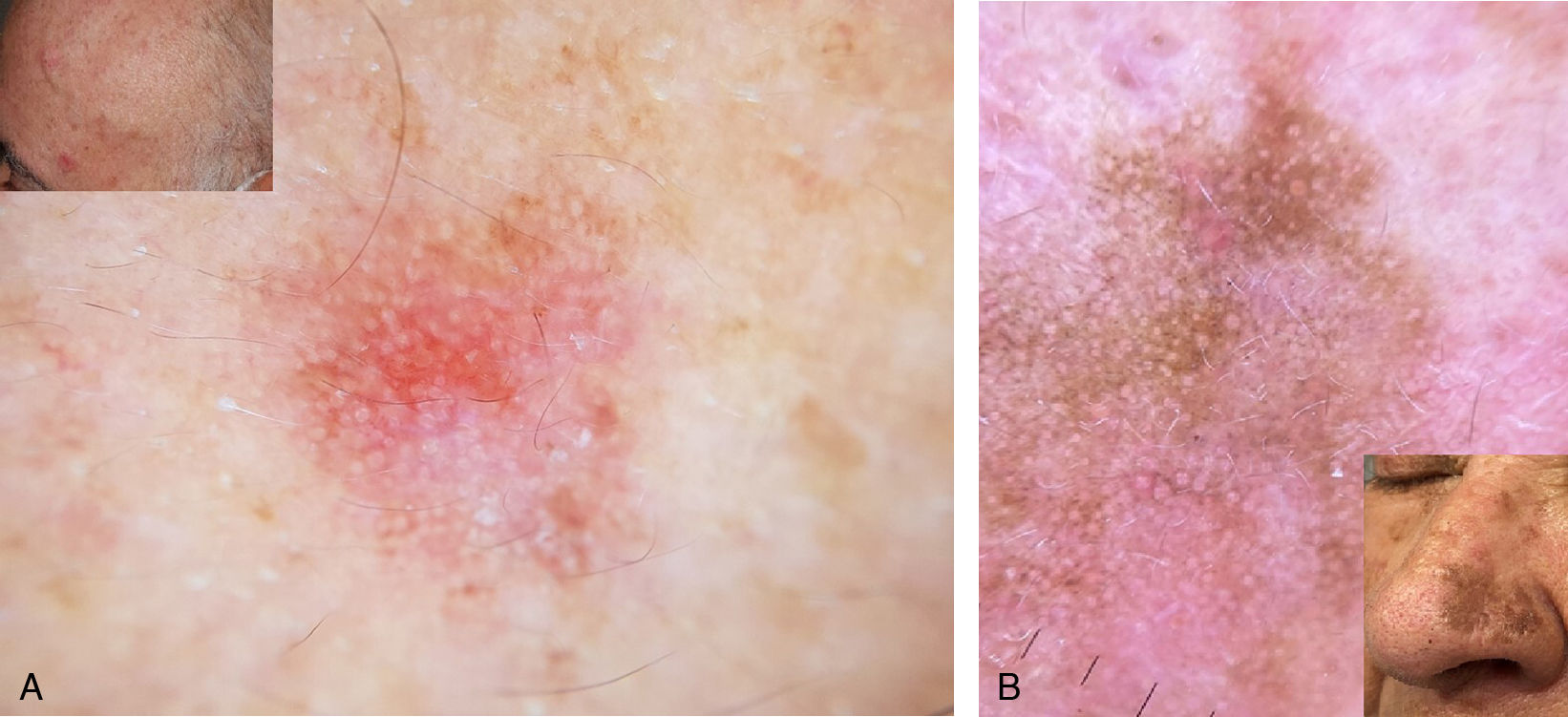
Técnicas de imagenDermatoscopiaLa dermatoscopia se utiliza ampliamente para diagnosticar QA19,20, con una sensibilidad y especificidad del 98% y 95%, respectivamente (fig. 2)21–23. Las características dermatoscópicas comunes de las QA no pigmentadas incluyen rosetas, eritema, seudoretículo rosa, aperturas foliculares amarillentas, escamas y vasos finos. En el 95% de los casos la combinación de estas características produce un patrón característico en fresa21.
Microscopia de reflectancia confocalLa microscopia de reflectancia confocal (MRC) tiene una sensibilidad y especificidad en el diagnóstico de QA del 80 y el 96%, respectivamente12,24. Su poca penetración, de 200-300 μs, particularmente en lesiones hiperqueratósicas, es una limitación24. Las principales características observables son la presencia de alteración superficial con escamas y paraqueratosis y el desorden estructural y pleomorfismo celular del estrato espinoso y granuloso con una disrupción del patrón en panal de abejas característico de estos estratos24,25.
Tomografía de coherencia ópticaLa tomografía de coherencia óptica (TCO) es útil para identificar las QA, ya que puede penetrar hasta la unión dermoepidérmica, con una sensibilidad del 86% y una especificidad del 83%26,27. Algunas de las características descritas incluyen: adelgazamiento de la epidermis con destrucción de la capa dermo-epidérmica, estrías blancas, puntos y áreas grises que corresponden a hiperqueratosis, y una banda oscura en el estrato córneo28,29.
Diagnóstico histopatológicoLa confirmación histológica es necesaria si la clínica es atípica, para descartar un CEC infiltrante, o en QA que no responden al tratamiento2. Microscópicamente las QA son proliferaciones intraepidérmicas de queratinocitos atípicos (con núcleos aumentados de tamaño, pleomórficos, hipercromáticos e incremento de la actividad mitótica), indistinguibles de los queratinocitos de los CEC infiltrantes, lo que implica que las QA sean consideradas como carcinomas escamosos in situ.
Según la clasificación histológica de Röwert-Huber et al.30,31 se pueden distinguir 3 grados (QA I-III) en función de la extensión intraepidérmica de los queratinocitos atípicos (tabla 1). La clasificación de Olsen no se correlaciona bien con la clasificación de Röwert-Huber, por lo que no se pueden extraer conclusiones sobre el grado histológico a partir de la apariencia clínica de las QA32. Un estudio histológico33 observó que la QA I era la lesión más frecuentemente encontrada en la base o en el borde de un CEC infiltrante, describiendo una vía de progresión donde una QA I puede evolucionar directamente a CEC.
Otra clasificación histológica para las QA incluye la evaluación del patrón de crecimiento basal de los queratinocitos atípicos (tabla 1)34 que se ha relacionado con el riesgo de progresión a CEC. Un estudio35 observó que cerca de los CEC infiltrantes aparecían con más frecuencia QA con un patrón de crecimiento basal pronunciado (PRO III).
Dado que tampoco existe correlación entre la clasificación histológica QA I-III y el patrón de crecimiento basal de PRO I-III, la clasificación histológica debe considerar patrones de crecimiento tanto ascendentes como descendentes34.
EscalasAKASI y AK-FASEn los últimos años se han descrito una serie de escalas que permiten evaluar toda el área afectada por QA y no solo las lesiones individuales. El índice del área y severidad de la queratosis actínica (Actinic Keratosis Area and Severity Index [AKASI])36 fue desarrollado para evaluar la severidad de las QA en la cabeza. Para su cálculo, se divide la cabeza en 4áreas asignando una ponderación según su tamaño relativo. En cada zona, se puntúa el porcentaje del área afectada, la distribución de las QA, el eritema y el grosor. La puntuación AKASI oscila entre 0 (sin QA) y 18 (grado más severo).
La escala Actinic Keratosis Field Assessment Scale (AK-FAS)37 evalúa la gravedad del campo de cancerización. Considera la extensión del área afectada por QA, el grado de hiperqueratosis y el daño solar y distingue 4grados de severidad.
AKQoLLas QA afectan a la calidad de vida de los pacientes por estar en zonas visibles, por el miedo de progresión38,39 y por los efectos locales de los tratamientos40.
El cuestionario Actinic Keratosis Quality of Life (AKQoL)41 evalúa la calidad de vida en pacientes con QA y está validado en España42. Incluye 3 dominios: «Función», «Emociones» y «Control sobre la vida en general», con una puntuación entre 0 y 27, donde una mayor puntuación indica un mayor deterioro en la calidad de vida.
Aunque las escalas AKASI y AK-FAS y el cuestionario AKQoL se utilizan en diversos estudios o ensayos clínicos, su aplicación en la práctica clínica todavía es limitada.
PrevenciónFotoprotecciónEl tratamiento de las QA debe complementarse con medidas de protección solar12. La fotoprotección ayuda a reducir la incidencia de nuevas lesiones y a frenar la progresión de las existentes43,44. En el mercado disponemos de filtros físicos (sustancias minerales como el óxido de cinc, que reflejan la radiación solar), químicos (moléculas que absorben la radiación UV) o biológicos: endonucleasas y fotoliasas (útiles en la prevención y reversión del fotodaño)45. Es importante señalar que la evidencia sobre el uso de fotoliasas para la prevención de QA es limitada y proviene de estudios realizados mayoritariamente en combinación con protectores solares. Estos estudios incluyen generalmente muestras pequeñas y periodos de seguimiento variables, lo que dificulta extraer conclusiones definitivas sobre su eficacia como tratamiento único. De ese modo, mientras que las fotoliasas pueden tener un rol complementario en la protección frente al fotodaño, su efecto óptimo parece depender de su uso junto con otros agentes fotoprotectores tradicionales45-49.
Quimioprofilaxis oralEn inmunodeprimidos principalmente, la quimioprofilaxis con retinoides orales (acitretina 10-25mg/día según tolerancia) se ha considerado una estrategia eficaz para prevenir QA y CEC44,45. No obstante, la evidencia que respalda la eficacia de los retinoides orales es limitada y la mayoría de los estudios disponibles se basan en muestras pequeñas. Cabe destacar que el efecto preventivo desaparece al suspender el tratamiento. Además, la tolerancia no es buena, por lo que se recomiendan como tratamientos intermitentes50–52.
La nicotinamida oral (500mg/12 h) ha demostrado disminuir los carcinomas queratinocíticos un 23% comparado con placebo, pero las QA únicamente un 13% a 12 meses de seguimiento. En pacientes receptores de un trasplante renal (RTOS) demostró ser eficaz y segura, aunque las diferencias no fueron estadísticamente significativas53,54.
TratamientoCuándo tratarEl tratamiento de los pacientes con QA es recomendable para lograr un aclaramiento completo y reducir el riesgo de progresión a CEC14,55. Sin embargo, dado que la regresión espontánea de las QA puede ocurrir en hasta un 23% de las lesiones de manera individual56, es importante considerar que la indicación del tratamiento debe evaluarse individualmente para cada paciente. En ocasiones, puede ser apropiado no tratar al paciente de inmediato y optar por un seguimiento cercano de su evolución.
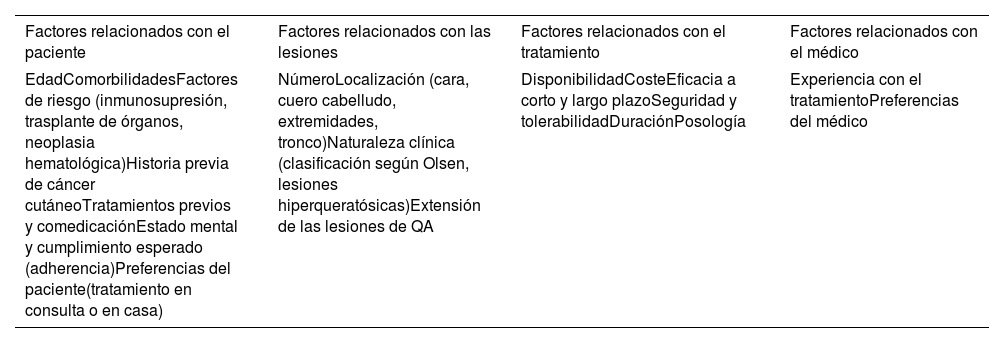
Aspectos a considerar a la hora de seleccionar el tratamientoLa elección de un tratamiento dirigido a la lesión o al campo de cancerización, debe tener en cuenta factores relacionados con el paciente, con las lesiones, con el propio tratamiento y con el médico (tabla 2)2,12,57,58.
Factores a considerar en la toma de decisiones sobre el tratamiento de la QA
| Factores relacionados con el paciente | Factores relacionados con las lesiones | Factores relacionados con el tratamiento | Factores relacionados con el médico |
|---|---|---|---|
| EdadComorbilidadesFactores de riesgo (inmunosupresión, trasplante de órganos, neoplasia hematológica)Historia previa de cáncer cutáneoTratamientos previos y comedicaciónEstado mental y cumplimiento esperado (adherencia)Preferencias del paciente(tratamiento en consulta o en casa) | NúmeroLocalización (cara, cuero cabelludo, extremidades, tronco)Naturaleza clínica (clasificación según Olsen, lesiones hiperqueratósicas)Extensión de las lesiones de QA | DisponibilidadCosteEficacia a corto y largo plazoSeguridad y tolerabilidadDuraciónPosología | Experiencia con el tratamientoPreferencias del médico |
QA: queratosis actínica.
La criocirugía debe ofrecerse en QA únicas o múltiples en número limitado2. Su aplicación es rápida y sencilla, pero el método de aplicación no está estandarizado. Demuestra tasas de curación completa de aproximadamente el 68%59-61, siendo eficaz también fuera de cabeza y cuello62. Los efectos secundarios esperables son la hipopigmentación y las cicatrices y el dolor durante la aplicación. En caso de hiperqueratosis se recomienda retirarla primero para favorecer la eficacia del tratamiento.
Escisión quirúrgicaIndicado para QA únicas si son hiperqueratósicas o hipertróficas, si no responden a otros tratamientos o si existe duda diagnóstica. La principal ventaja es el examen histológico posterior para excluir CEC infiltrante. Las desventajas incluyen la necesidad de anestesia local, el sangrado, o la cicatrización no estética2.
Tratamientos destructivosLos peelings químicos (ácido tricloroacético, solución de Jessner, fenol) presentan una tasa de eliminación de lesiones del 31,9%63. Sirven para tratamiento del campo de cancerización y tiene efecto fotorrejuvenecedor. Con la dermoabrasión, cuando se hace correctamente, se han observado tasas de respuesta completa altas y sostenidas del 83-96% a los 2 años64. Sin embargo, no está bien estandarizada, es operador dependiente y puede provocar cicatrices inestéticas. Los láseres ablativos (CO2) se han empleado para lesiones concretas o en el contexto de rejuvenecimiento asociado a tratamiento de campo, pero comparado con la crioterapia es un tratamiento más caro, menos disponible y con menor aclaramiento sostenido6.
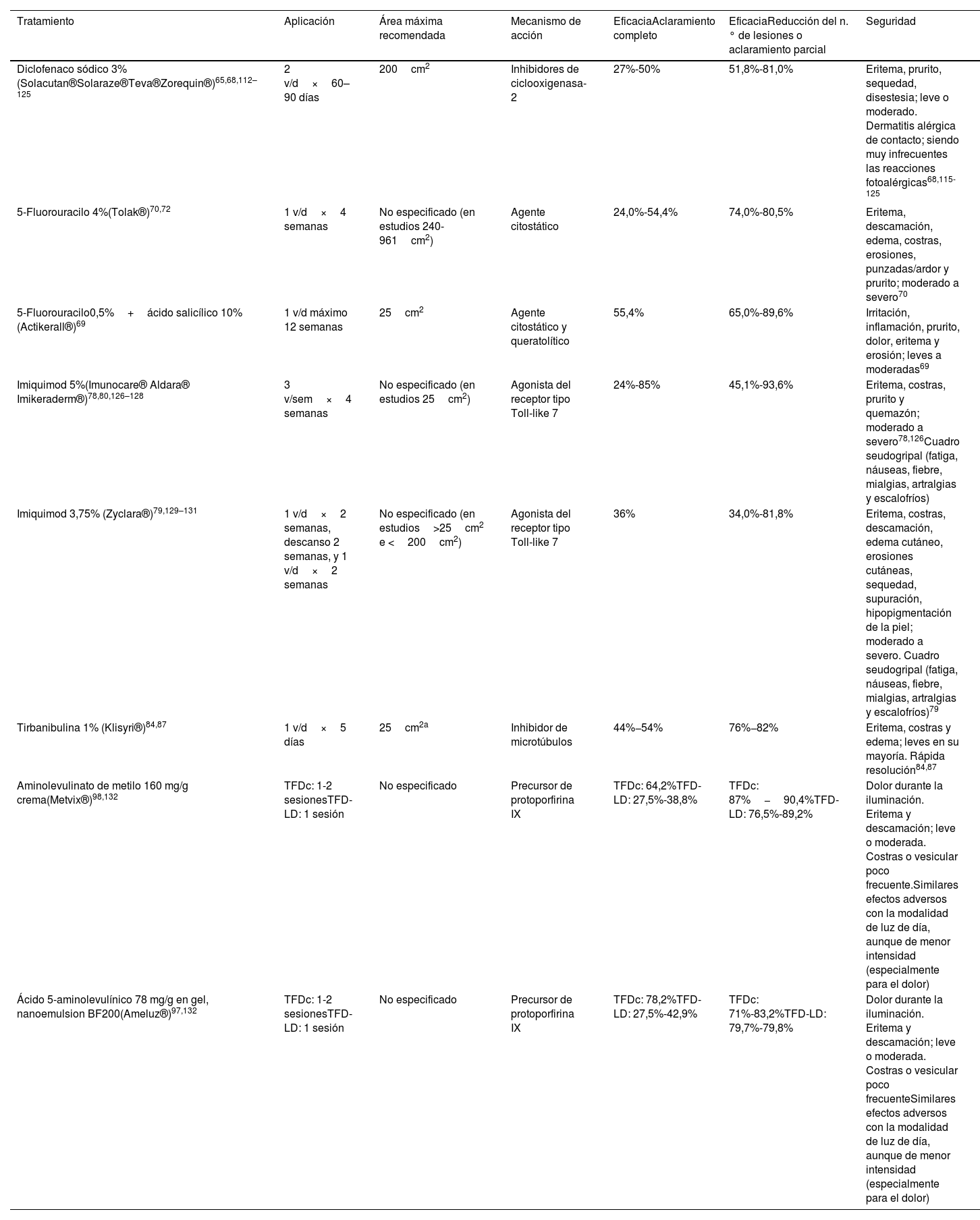
Tratamientos tópicosLas principales características de los tratamientos tópicos se muestran en la tabla 3.
Principales características de los tratamientos tópicos disponibles en España actualmente
| Tratamiento | Aplicación | Área máxima recomendada | Mecanismo de acción | EficaciaAclaramiento completo | EficaciaReducción del n.° de lesiones o aclaramiento parcial | Seguridad |
|---|---|---|---|---|---|---|
| Diclofenaco sódico 3%(Solacutan®Solaraze®Teva®Zorequin®)65,68,112–125 | 2 v/d×60–90 días | 200cm2 | Inhibidores de ciclooxigenasa-2 | 27%-50% | 51,8%-81,0% | Eritema, prurito, sequedad, disestesia; leve o moderado. Dermatitis alérgica de contacto; siendo muy infrecuentes las reacciones fotoalérgicas68,115-125 |
| 5-Fluorouracilo 4%(Tolak®)70,72 | 1 v/d×4 semanas | No especificado (en estudios 240-961cm2) | Agente citostático | 24,0%-54,4% | 74,0%-80,5% | Eritema, descamación, edema, costras, erosiones, punzadas/ardor y prurito; moderado a severo70 |
| 5-Fluorouracilo0,5%+ácido salicílico 10%(Actikerall®)69 | 1 v/d máximo 12 semanas | 25cm2 | Agente citostático y queratolítico | 55,4% | 65,0%-89,6% | Irritación, inflamación, prurito, dolor, eritema y erosión; leves a moderadas69 |
| Imiquimod 5%(Imunocare® Aldara® Imikeraderm®)78,80,126–128 | 3 v/sem×4 semanas | No especificado (en estudios 25cm2) | Agonista del receptor tipo Toll-like 7 | 24%-85% | 45,1%-93,6% | Eritema, costras, prurito y quemazón; moderado a severo78,126Cuadro seudogripal (fatiga, náuseas, fiebre, mialgias, artralgias y escalofríos) |
| Imiquimod 3,75% (Zyclara®)79,129–131 | 1 v/d×2 semanas, descanso 2 semanas, y 1 v/d×2 semanas | No especificado (en estudios>25cm2 e <200cm2) | Agonista del receptor tipo Toll-like 7 | 36% | 34,0%-81,8% | Eritema, costras, descamación, edema cutáneo, erosiones cutáneas, sequedad, supuración, hipopigmentación de la piel; moderado a severo. Cuadro seudogripal (fatiga, náuseas, fiebre, mialgias, artralgias y escalofríos)79 |
| Tirbanibulina 1% (Klisyri®)84,87 | 1 v/d×5 días | 25cm2a | Inhibidor de microtúbulos | 44%−54% | 76%−82% | Eritema, costras y edema; leves en su mayoría. Rápida resolución84,87 |
| Aminolevulinato de metilo 160 mg/g crema(Metvix®)98,132 | TFDc: 1-2 sesionesTFD-LD: 1 sesión | No especificado | Precursor de protoporfirina IX | TFDc: 64,2%TFD-LD: 27,5%-38,8% | TFDc: 87%−90,4%TFD-LD: 76,5%-89,2% | Dolor durante la iluminación. Eritema y descamación; leve o moderada. Costras o vesicular poco frecuente.Similares efectos adversos con la modalidad de luz de día, aunque de menor intensidad (especialmente para el dolor) |
| Ácido 5-aminolevulínico 78 mg/g en gel, nanoemulsion BF200(Ameluz®)97,132 | TFDc: 1-2 sesionesTFD-LD: 1 sesión | No especificado | Precursor de protoporfirina IX | TFDc: 78,2%TFD-LD: 27,5%-42,9% | TFDc: 71%-83,2%TFD-LD: 79,7%-79,8% | Dolor durante la iluminación. Eritema y descamación; leve o moderada. Costras o vesicular poco frecuenteSimilares efectos adversos con la modalidad de luz de día, aunque de menor intensidad (especialmente para el dolor) |
TFDc: terapia fotodinámica convencional; TFD-LD: terapia fotodinámica de luz de día.
Actualmente está en estudio su uso en un área máxima de 100cm2, se han publicado los datos del estudio MUST (fase 1) con resultados favorables91.
El diclofenaco tiene acción antiinflamatoria y antineoplásica. La presentación al 3% en gel de ácido hialurónico está aprobada desde 201165 para tratar QA únicas o múltiples y el campo de cancerización (incluyendo campos grandes). Debido a su larga posología (60-90 días) la adherencia al tratamiento puede no ser la esperada66. Las tasas de respuesta completa se encuentran en torno al 41%67. La tolerancia es en general buena, aunque se asocia a prurito en un tercio de los pacientes y existe riesgo de fotosensibilidad y dermatitis de contacto68.
5-fluorouraciloLas formulaciones comercializadas en España son 5-fluorouracilo (5-FU) al 0,5% con ácido salicílico al 10% en solución cutánea (desde 2013)69 y 5-FU al 4% en crema (desde 2020)70. Ambas aprobadas para tratar QA únicas o múltiples y el campo de cancerización.
La formulación clásica de 5-FU al 5% en crema se administraba 2 veces al día, 21 días. En un ensayo clínico aleatorizado con 624 pacientes donde se comparaban 4 tipos de tratamientos para las QA (5-FU 5%, imiquimod 5%, mebutato de ingenol [IMB] y terapia fotodinámica [TFD]), se concluyó que el 5-FU 5% era el tratamiento más efectivo con una probabilidad de mantenerse libre de enfermedad del 74,7% al año del tratamiento71. No obstante, se asocia a tasas elevadas de reacciones cutáneas locales (40% erosiones y 57% costras71), lo que obliga a suspender el tratamiento hasta un tercio de los pacientes, con un impacto en la eficacia. Fuera de ficha técnica, se emplea en pautas más cortas de administración (10-15 días una vez al día) con tasas de respuesta razonables y mejor tolerancia, aunque dichas pautas no han sido evaluadas en ensayos clínicos ni existen estudios con datos de vida real. La crema comercializada de 5-FU al 4% muestra eficacia similar y mejor tolerabilidad que al 5% aplicándose una vez al día durante 4 semanas72.
El 5-FU al 0,5% con ácido salicílico al 10% tiene un efecto queratolítico que potencia el efecto citostático del 5-FU. Se aplica una vez al día, pero el tratamiento puede alargarse hasta 12 semanas, lo que puede comprometer la adherencia. Está especialmente indicado para QA hiperqueratósicas.
La aplicación de 5-FU al 5% combinado con calcipotriol 0,005% 2 veces al día durante 4 días, es más eficaz que el 5-FU en monoterapia según un ensayo clínico aleatorizado, aunque solo se alcanzó un aclaramiento completo en el 27% de los participantes en la semana 873. La combinación de calcipotriol y 5-FU redujo el riesgo de CEC en la cara y el cuero cabelludo durante un período de 3 años73-76.
La utilización de tratamiento oclusivo con 5-FU (aplicación de 5-FU y oxido de cinc y vendaje elástico, con recambio 1 vez a la semana) se ha utilizado para el tratamiento de grandes campos de miembros superiores e inferiores con buenos resultados77.
ImiquimodImiquimod tiene actividad antivírica y antineoplásica además de estimular la respuesta inmune innata y adquirida. Es un agonista de receptores TLR7 y produce una elevación local de los niveles de IFN-alfa entre otras citocinas. En España se comercializa imiquimod al 5% (desde 1999)78 y al 3,75% (desde 2012)79. Ambas formulaciones están aprobadas para tratar QA únicas o múltiples y el campo de cancerización. Las principales diferencias entre ambas son la extensión del campo a tratar y la posología (tabla 3). Imiquimod al 5% en crema alcanza tasas de respuesta completa del 45-57% de los pacientes80,81. Al año, el 53,9% de los pacientes se mantienen libres de enfermedad71. Un 15% suspende el tratamiento debido a reacciones cutáneas locales, casi la mitad desarrollan erosiones o úlceras y el 70%, costras71. Imiquimod se ha asociado a síntomas sistémicos en forma de cuadro seudogripal y al desarrollo de una reacción cutánea local más allá de las zonas tratadas. También se ha utilizado imiquimod al 5% crema en tratamientos de 12 días consecutivos con unas tasas de respuesta completa del 52,3% y parcial del 75,4%82.
Mebutato de ingenolEn 2020, la European Medicines Agency (EMA) suspendió la aprobación de IMB para QA debido a la observación de una mayor incidencia de CEC en los pacientes tratados con IMB respecto a los tratados con imiquimod en un estudio de seguridad de 3 años en 484 pacientes (3,3% vs. 0,4%)83. Los pacientes previamente tratados con IMB deben ser monitorizados para detectar la aparición de tumores de piel en campos de tratamiento anteriores.
TirbanibulinaDesde 2021 tirbanibulina está aprobada para tratar QA únicas o múltiples no hipertróficas y el campo de cancerización en cara o cuero cabelludo en un área de hasta 25cm284. Utiliza un mecanismo de acción nuevo que inhibe la polimerización de las tubulinas durante la división celular y hace que la célula entre en apoptosis y no necrosis, lo que se ha asociado a una alta eficacia con reacciones locales en su mayoría leves a moderadas85-88. Se administra una vez al día durante 5 días consecutivos, con reacciones cutáneas locales leves, muy alta adherencia y satisfacción de médicos y pacientes89. Alcanza tasas de remisión completa del 49% y de respuesta parcial superiores al 70%87,90. La eficacia y la seguridad de tirbanibulina en áreas mayores (hasta 100cm2) está siendo evaluada, obteniéndose resultados favorables en un estudio fase 1, resultados que han sido confirmados recientemente en un estudio fase 391,92. El eritema es la única reacción cutánea local frecuente, con un pico máximo a los 8 días y una resolución completa a los 30 días sin necesidad de intervención. El dolor, el picor y la sensación de ardor se observan en menos del 10%, al igual que las erosiones que se califican en moderadas o graves en el 3% de los pacientes87.
Terapia fotodinámicaLa TFD se basa en la aplicación de un agente tópico fotosensibilizante junto a una fuente de luz para destruir selectivamente los queratinocitos atípicos. Se han establecido múltiples regímenes de TFD lo que la convierte en un procedimiento heterogéneo93-96. Todos los tipos de TFD se ofrecen para tratar QA únicas o múltiples y el campo de cancerización.
Los fotosensibilizantes e indicaciones aprobadas en España son el metil-aminolevulinato en crema (MAL) desde 200298 para QA no hipertróficas; y el ácido 5-aminolevulínico en nanoemulsión en gel (ALA-BF200) desde 201297 para QA leves y moderadas y campo de cancerización. Ambos se pueden emplear tanto en TFD con luz roja como con luz de día.
La TFD puede requerir pretratamiento de la QA94 con vaselina salicílica al 10% durante una semana previa al tratamiento, urea al 20%, peeling químico, láser ablativo o micropunciones.
El protocolo convencional consiste en la aplicación del fotosensibilizador, con incubación en oclusión durante 2-3 h antes de la activación con luz roja (37,5J/cm2) durante 10-20 min. Las tasas de aclaramiento completo varían entre el 31,4 y el 91,0% (tasa de reducción de lesiones 58,0-94,3%)2,6,55. El 37,7% de los pacientes que responden se mantienen libres de enfermedad al año de tratamiento71. La TFD asocia dolor en el 80% de los pacientes y ardor moderado/intenso en el 86%. La aplicación de frío local, la toma de antiinflamatorios no esteroideos 30 min antes de la irradiación, la irradiación fraccionada con pausas de 3 min, la aplicación de clobetasol tópico, la «talkestesia» o la infiltración de anestesia local o troncular sin vasoconstrictor ayudan a mejorar la tolerancia94.
Los protocolos de TFD con luz de día utilizan la luz solar natural como fuente de energía mediante la aplicación del fotosensibilizantes y la exposición a la luz solar en los siguientes 30 min durante 2 h99. Las tasas de aclaramiento completo varían entre el 27,5 y el 42,9% al utilizar ALA (tasa de reducción de lesiones 79,7-79,8%) y del 27,5-38,8% para MAL (tasa de reducción de lesiones 76,5-89,2%)2,6,55. Las ventajas incluyen un dolor menor, la posibilidad de tratar campos grandes, mayor cumplimiento y la falta de necesidad de fuentes de luz artificial, lo que abarata los costes100. Esta modalidad se puede realizar en España durante todo el año debido a nuestra latitud, excepto en los días lluviosos o si la temperatura es menor a 10°C.
La realización de TFD combinada mediante la realización de TFD con luz de día durante 2 h y aplicación posterior de luz roja a dosis habitual ha demostrado mejor eficacia respecto a la luz de día (respuesta completa 31,6% vs. 15,8% y respuesta parcial 63,2% vs. 25,3%) con un aumento leve/moderado de los efectos secundarios locales y dolor101.
Terapia combinadaLa combinación de una modalidad para tratar la lesión con otra para tratar el campo de cancerización en un mismo paciente es frecuente en la práctica clínica habitual con el objetivo de maximizar la respuesta, mejorar eficacia y tolerancia6,55. Combinaciones utilizadas incluyen la combinación del láser ablativo como tratamiento previo a la TFD102, la criocirugía en combinación con un tratamiento tópico103 y la TFD en combinación con un tratamiento tópico, incluyendo calciprotriol 15 días antes, 5-FU al 5% 2 veces al día 6-7 días antes, imiquimod previo o posterior a TFD, o tazaroteno previo a TFD104,105.
Otros tratamientosExisten otros tratamientos descritos para el manejo de las QA en pacientes de especial severidad, como la radioterapia volumétrica (VMAT) y la capecitabina oral, aunque su uso no está extendido en la práctica clínica en España.
Algunos estudios han evaluado el uso de VMAT para tratar el campo de cancerización en pacientes con múltiples QA e incluso carcinoma de células escamosas. La decisión de emplear esta terapia más agresiva, por ejemplo, para tratar múltiples lesiones en el cuero cabelludo, debe ser evaluada por un equipo multidisciplinario de dermatología y oncología radioterápica106,107.
Capecitabina puede utilizarse en un contexto de prevención de CEC. Sin embargo, debido a sus efectos secundarios es un tratamiento poco utilizado en nuestro entorno y se reserva para casos de alto riesgo, como los pacientes trasplantados de órgano sólido con antecedentes de múltiples carcinomas de células escamosas108.
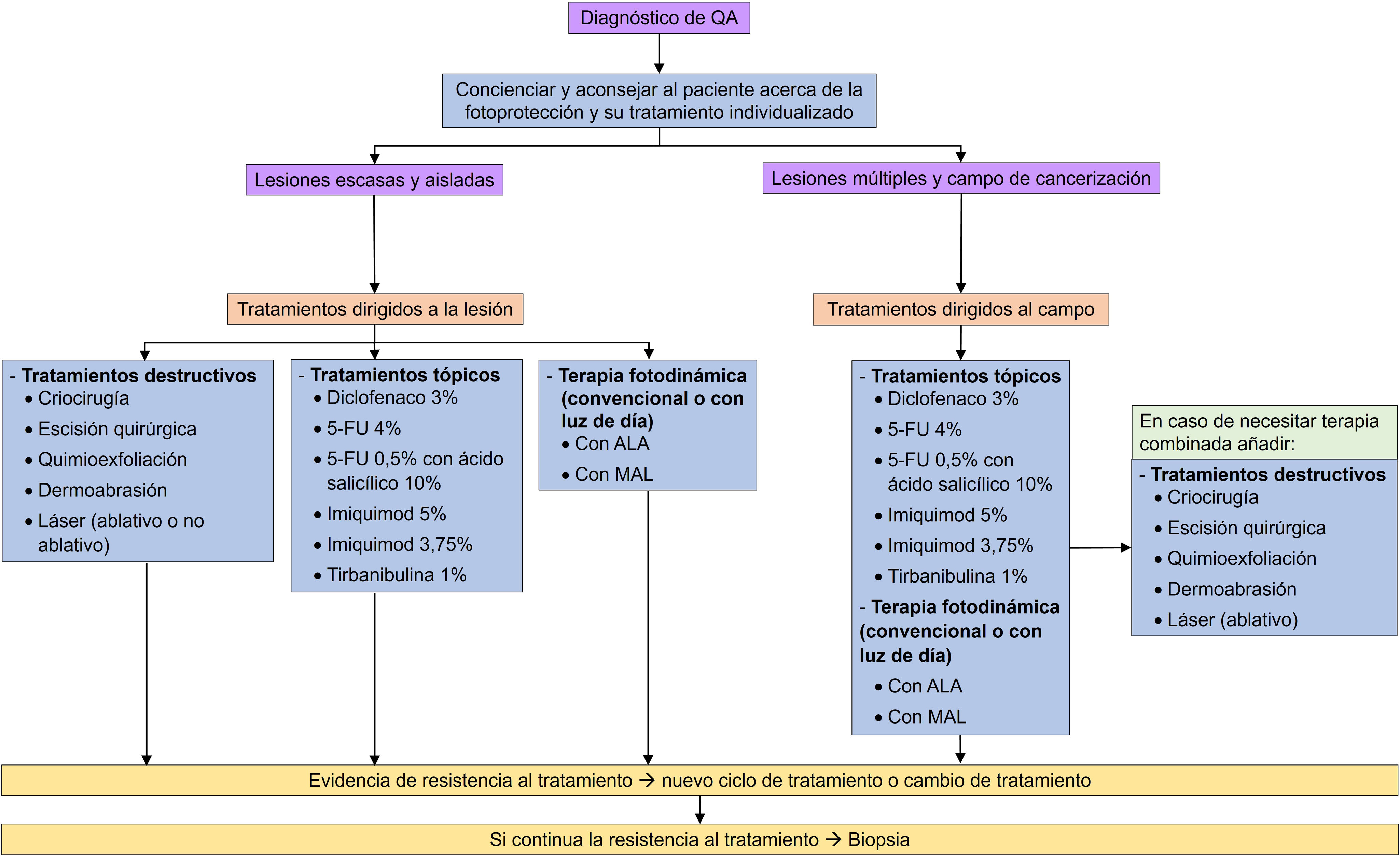
Resumen de manejo de las QA en el momento actualEn los últimos años se han aprobado nuevos fármacos y nuevas formulaciones para el tratamiento de la QA. La figura 3 muestra la actualización del cuadro de tratamiento de la QA propuesto en 2014 por Ferrandiz et al.14 de acuerdo con los tratamientos disponibles actualmente en España.
Pacientes especiales: inmunosupresión y trasplante de órganosLa quimioprofilaxis con retinoides orales es eficaz para la prevención de QA y CEC en esta población de riesgo51.
Una revisión sistemática de tratamientos locales para QA en 242 RTOS encontró que la TFD tuvo las tasas más altas de aclaramiento de lesiones (46-100%), seguida por 5-FU (79%), imiquimod (61-73,7%) y diclofenaco (53%); pero no existen estudios comparativos y esta revisión incluía únicamente un estudio con 5-FU109. En general, la eficacia de los tratamientos en RTOS parece ser menor que en pacientes inmunocompetentes y los expertos en el tratamiento de pacientes trasplantados no han alcanzado un consenso sobre qué tratamiento de las QA sería de primera elección en esta población110.
Debido al curso más agresivo de la enfermedad y a una mayor proporción de lesiones resistentes al tratamiento, a menudo es necesario repetir el tratamiento55.
SeguimientoSe deben programar visitas de seguimiento periódicas ya que el paciente con QA debe ser considerado un paciente crónico. El seguimiento después del tratamiento inicial implica evaluar el éxito del tratamiento, la recurrencia de las lesiones y el desarrollo de nuevas QA. Debe insistirse en la autoexploración y en las medidas de fotoprotección. El intervalo de seguimiento debe adaptarse al perfil de cada paciente y al riesgo específico de desarrollar un carcinoma6,14,55. No existen estudios que hayan demostrado un protocolo de seguimiento más adecuado. Sí que se ha demostrado que el efecto preventivo de los tratamientos del campo de cancerización aparece durante el primer año, pero se pierde a largo plazo. De ese modo, dado que la QA se considera una enfermedad crónica, se recomienda realizar tratamientos periódicos para eliminar las lesiones de nueva aparición y reducir el riesgo de CEC111.
- 1.
El diagnóstico de las QA es fundamentalmente clínico, aunque técnicas como la dermatoscopia, la MRC o la TCO pueden ayudarnos a confirmar el diagnóstico. La biopsia cutánea se reserva para casos dudosos.
- 2.
Actualmente disponemos de varios sistemas de clasificación clínica, microscópica y de área de afectación, sin una clara correlación entre ellos, pero fundamentales para una más adecuada valoración del riesgo del paciente.
- 3.
No se puede predecir qué QA progresará a CEC ni cuándo, por lo que se recomienda el tratamiento de todas las QA.
- 4.
Existe un amplio abanico de tratamientos disponibles para las QA a los que se les han unido nuevas aprobaciones en los últimos años como la administración con luz de día de la TFD, la formulación de 5-fluorouracilo al 4% o la tirbanibulina al 1%, entre otros.