El tratamiento de la leishmaniasis cutánea (LC) es complejo, depende de la especie de Leishmania, el área de adquisición de la infección, forma clínica y edad del paciente. Los fármacos administrados parenteralmente se reservan en general para formas complejas o pacientes inmunocomprometidos, y consisten principalmente en antimoniales pentavalentes administrados vía intravenosa o intramuscular. Los tratamientos locales son los más utilizados e incluyen a los antimoniales pentavalentes intralesionales, la termoterapia y crioterapia, entre otros. Estas terapias pueden ser muy dolorosas, presentar efectos adversos potenciales graves y tener menor efectividad en niños1. La miltefosina, agente oral con eficacia reconocida para leishmania, puede ser una buena opción en estos casos.
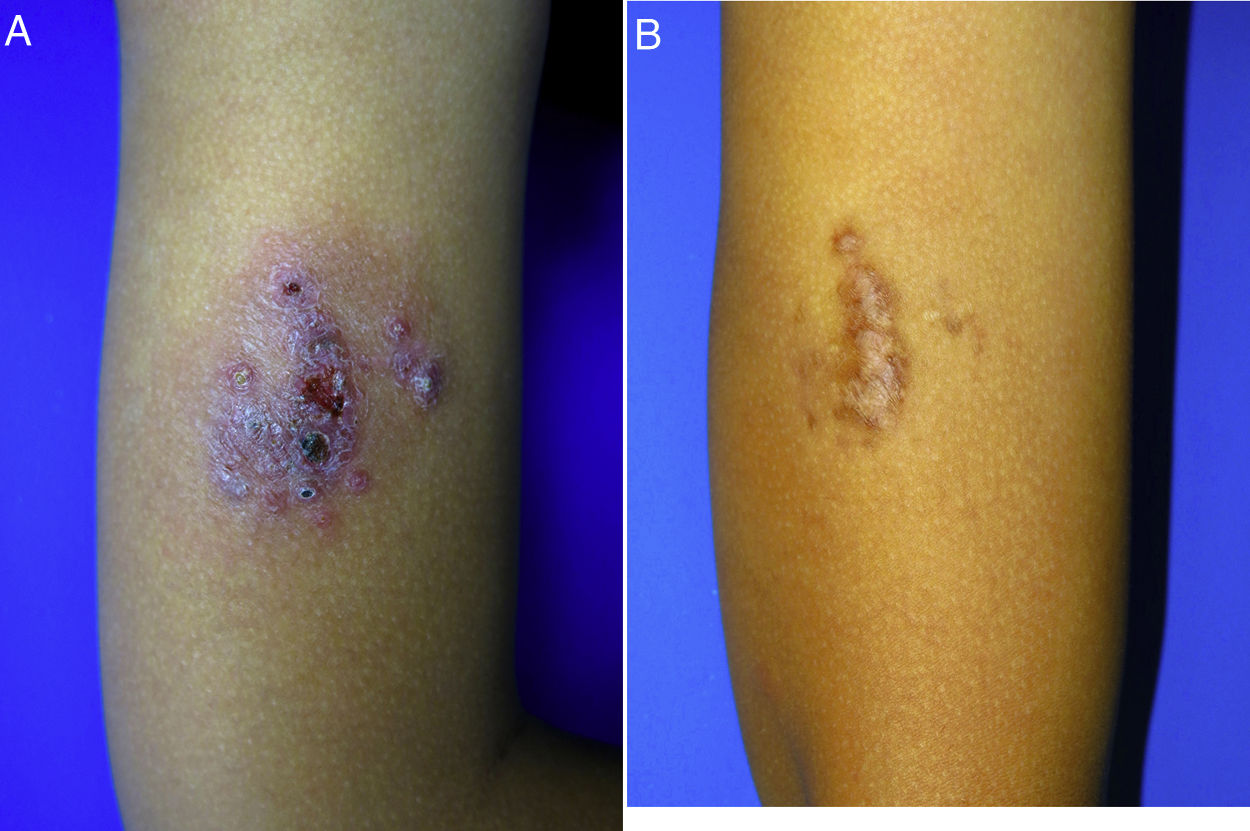
Un niño de 10 años (35 kg) de origen marroquí, sin antecedentes patológicos relevantes, consultó por una lesión cutánea dolorosa en el brazo de seis meses de evolución que apareció una semana después de viajar a Marruecos. En el examen físico presentaba una placa eritematoviolacea exudativo-costrosa de 8 x 6 cm (fig. 1A). La biopsia mostró un infiltrado linfohistiocitario con amastigotes intracelulares (cuerpos de Leishman-Donovan) en dermis, diagnosticándose de LC. Debido a la edad del niño, su escasa tolerancia a procedimientos médicos y a los potenciales efectos adversos de los antimoniales pentavalentes intralesionales, junto con su menor efectividad en población infantil menor de 12 años2, se decidió iniciar tratamiento con miltefosina (75 mg/día) por 28 días. Las analíticas previas y durante el tratamiento, incluyendo hemograma, perfil renal y hepático fueron normales. A las dos semanas de tratamiento el paciente ya no presentaba dolor, y a las cuatro semanas se observaba notable mejoría clínica, con presencia de hiperpigmentación residual. En el seguimiento seis meses después el paciente se mantenía asintomático, con una placa de aspecto residual en el brazo (fig. 1B).
Leishmaniasis cutánea infantil. A) Placa eritematoviolácea exudativo-costrosa muy dolorosa de 8 x 6 cm en el brazo de un niño de 10 años. B) Control seis meses después del tratamiento con miltefosina oral. Placa marronácea de aspecto residual en el brazo. El paciente se mantenía asintomático.
El tratamiento de la leishmaniasis en niños puede ser difícil: presentan mayor porcentaje de lesiones faciales, una tasa de respuesta significativamente menor a los antimoniales que los adultos, y dificultades como menor adherencia a tratamientos inyectables y la potencial toxicidad sistémica derivada del tratamiento estándar1 (tabla 1).
Tratamientos disponibles para leishmaniasis cutánea en niños
| Tratamiento | Vía de administración – dosis | Efectos adversos | Indicación |
|---|---|---|---|
| Crioterapia | Nitrógeno líquido aplicado durante 15–20 segundos hasta 1–2 mm por fuera de la lesión. Repetir 3 veces por sesión.El tratamiento se repite cada 3 semanas hasta la curación. | Eritema, edema, ampolla,hipo o hiperpigmentación residual, cicatriz | Lesiones recientes, pequeñas (< 3 cm de diámetro), < 5 placas, no utilizar en áreas cosmética ni funcionalmente importantes (cara, articulaciones) |
| Termoterapia | Calor superficial a 50°C durante 30 segundos hasta 1–2 mm alrededor de la lesión. Requiere anestesia local | Eritema, edema, quemaduras, hipo o hiperpigmentación residual | Pocas lesiones < 5, pequeñas < 3 cm de diámetro, no áreas cosméticamente importantes(cara), y no áreas funcionalmente importantes.Especies termosensibles: L.L. major, L.L. tropica, L.V. panamensis y L.V. braziliensis |
| Imiquimod | Tópica. Crema al 5%, 3 veces a la semana por 8 semanas | Eritema, prurito, edema, ulceración. Cefalea, síndrome seudogripal, mialgias (poco frecuentes) | Pocas lesiones, pequeñas, especies no asociadas con afectación mucosa o linfocutánea.En combinación con fármacos antimoniales pentavalentes, puede reducir el tiempo de administración de éstos.En monoterapia presenta una eficacia variable12 |
| Paromomicina | Tópica. Cremas o pomadasDiferentes formulaciones | Eritema, prurito, dolor | Ulceras debido a L. major, pequeñas (≤ 5 cm), escasas en número, sin afectación linfocutánea |
| Terapia fotodinámica/ terapia fotodinámica activada con luz de día | Aplicación semanal hasta curación de las lesiones* | Eritema, prurito, dolor | Pocas lesiones, pequeñas, especies no asociadas con afectación mucosa o linfocutánea |
| Antimoniales pentavalentes-Estibogluconato de sodio-Antimonio de meglumina | IntralesionalesInyección de 0,2 a 5 ml por sesión cada tres a siete días, total de cinco a ocho sesiones de tratamiento (o hasta la curación clínica)Vía intramuscular o intravenosa20 mg de SbV/kg/día en una dosis diaria infundida durante 15 a 30 minutos por 20 días | Dolor, reacción alérgica local, edema, prurito y eritemaNáuseas, dolor abdominal,cefalea, mialgias y artralgias.Elevación de enzimas pancreáticas, elevación de transaminasas séricas,leucopenia leve e inespecífica.Cardiotoxicidad y alteraciones electrocardiográficas. | Escaso número y pequeñas lesionesEspecies no asociadas con afectación mucosa o linfocutáneaEspecies asociadas a afectación mucosa o linfocutánea, > 5 lesiones, > 3 cm, áreas cosmética o funcionalmente importantes. |
| Azoles-Fluconazol-Itraconazol | Vía oral12 mg/kg/día durante 6 semanas5-10 mg/kg/día por 42–56 días | Náuseas, vómitos, diarrea, hepatotoxicidadAumento de transaminasas séricas | Leshmaniasis cutánea, linfocutánea y mucocutánea,Eficacia variable según laespecie |
| Pentamidina | Vía intramuscular3–4 mg / kg cada dos días, 3–4 dosis | Pancreatitis, hipotensiónProlongación del intervalo QTHipercalemiaCitopeniasNefrotoxicidadElevación de transaminasas séricas | Exclusivamente para L.V. guyanensis |
| Anfotericina-Anfotericina desoxicolato-Anfotericina B liposomal | 0,5–1,0 mg/kg IV diariamente o cada dos días para una dosis acumulada de 15–30 mg/kg3 mg/kg/día IV durante 5 días y luego una sexta dosis el día 10 o diariamente durante 7 días para dosis acumuladas de 18–21 mg/kg** | NefrotoxicidadHipocalemiaAnemiaFlebitis venosa periféricaFiebre relacionada con la infusiónProlongación del intervalo QT | Lesiones complejas (especies asociadas a MC, > 5 lesiones, lesiones > 3 cm, áreas cosméticamente importantes(cara), áreas funcionalmente importantes, afectación de ganglios linfáticos), formas graves (visceral o mucosa), lesiones resistentes a la terapia de primera línea o pacientes coinfectados por VIH o inmunocomprometidos |
Puede ser aplicada por el propio paciente o familiares una vez por semana, exposición solar durante 2 horas, y repetir hasta la curación clínica.
La dosis se basa en el tratamiento de la leishmaniasis visceral.
FDA: Food and Drugs Administration; ̊C: grado Celsius; IV: intravenoso; MC: mucocutanea; VIH: virus de la inmunodeficiencia humana; L.L.: Leishmania Leishmania, L.V.: Leishmania Viannia; Sb: antimonio; SbV: antomonio pentavalente o sales de antimonio.
La miltefosina es una alquilfosfocolina desarrollada como agente antitumoral, descubriéndose posteriormente su actividad contra leishmania. En el año 2014 fue aprobada por la Food and drugs administration (FDA) para el tratamiento de la leishmaniasis visceral, cutánea y mucocutánea en pacientes ≥ 12 años (≥ 30 kg), siendo actualmente el único fármaco vía oral autorizado3. Sus efectos adversos se pueden observar en más de la mitad de los pacientes, aunque son mayoritariamente leves y bien tolerados. Casi el 90% de los efectos adversos son de grado 1 y consisten principalmente en diarrea, vómitos, elevación transitoria de transaminasas y disfunción renal leve, y no suelen ser motivo de interrupción terapéutica1,4 (tabla 2). Múltiples ensayos clínicos han demostrado una alta tasa de respuesta en leishmaniasis visceral y cutánea con miltefosina. Un metaanálisis reciente mostró respuestas similares en LC con miltefosina o antimoniales en el tratamiento de la L. Braziliensis, pero una significativamente mayor tasa de éxito terapéutico en el resto de las especies de leishmania al utilizar miltefosina5. En cuanto a la población pediátrica, un metaanálisis reciente que evaluó los tratamientos de LC en niños ≤ 12 años, encontró una respuesta satisfactoria con miltefosina en el 68 a 82,6% de casos afectos con LC6. Destaca un ensayo clínico aleatorizado realizado en Colombia que incluyó un total de 116 niños (2 a 12 años) con LC y asignados a tratamiento con antimonio de meglumina (20 mg Sb/kg/día intramuscular durante 20 días) o miltefosina (1,8–2,5 mg/kg/día vía oral durante 28 días), que mostró una tasa de respuesta con miltefosina superior al 80%, siendo no inferior al antimonio de meglumina y con una menor tasa de efectos adversos7. Son numerosos los casos clínicos y series de casos que demuestran la utilidad de miltefosina en el tratamiento de la LC del «Viejo Mundo»8,9, aunque los datos disponibles en niños son limitados6.
Mecanismo de acción, posología, efectos adversos, contraindicaciones e interacciones de la miltefosina
| Mecanismo de acción | Posología | Presentación | Efectos adversos | Contraindicaciones | Interacciones |
|---|---|---|---|---|---|
| DesconocidoSe le atribuye una posible interacción con fosfolípidos y esteroides en las membranas celulares parasitarias, la inhibición de la función mitocondrial y muerte celular similar a la apoptosis | Niños:2-11 años: 2,5 mg/kg durante 28 días≥ 12 años:< 25 kg: 50 mg/día durante 28 días>25kg: 50 mg dos veces al día durante 28 díasAdultos:30 a 44 kg: 50 mg dos veces al día durante 28 días≥ 45 kg: 50 mg 3 veces al día durante 28 díasAdministrar con comidas para disminuir efectos adversos gastrointestinales* | Capsulas duras fraccionables de 50 mg (nombre comercialImpavido®) | Frecuentes (> 10%): Anorexia, náuseas, vómitos, diarrea, dolor abdominal. Cefalea, mareos.Plaquetopenia (< 150.000: 62%; < 50.000: 2%)Elevación de transaminasas séricas (x3: 94%; x3-5: 6%)Incremento de creatinina sérica (≥ 1,5 veces por encima del valor basal: 10% a 25%)Raros (1 a 10%):Somnolencia, malestar, fatiga, parestesia.Prurito, celulitis, erupción cutánea, síndrome de Stevens-Johnson, urticariaDolor testicular, hinchazón testicularLinfangitis, anemia, linfadenopatía.Otros: debilidad, fiebre, agranulocitosis, disminución del volumen de eyaculación, aumento de la bilirrubina sérica, ictericia, melena, convulsiones, trombocitopenia, pancreatitis** | HipersensibilidadSíndrome de Sjögren-LarssonEmbarazo (estudios de toxicidad en ratas indican embriotoxicidad, fetotoxicidad y teratogenicidad). Mujeres en edad fértil deberán utilizar anticoncepción efectiva durante y hasta 3-5 meses después de finalizado el tratamiento.No hay datos sobre el riesgo durante la lactancia, no se recomienda su administración | No se conocen interacciones significativas |
La miltefosina puede ser detectable en plasma hasta seis meses postratamiento, y sus niveles intracelulares, hasta un mes después4. Esto explicaría que la respuesta clínica mejore progresivamente después de suspendido el fármaco. En algunos estudios se ha observado que los niños pueden presentar menores concentraciones plasmáticas e intracelulares de miltefosina que los adultos4, lo que podría influir en la respuesta terapéutica.
Pese a ser el único agente oral aprobado para el tratamiento de la leishmaniasis, su gran efectividad, buen perfil de seguridad y a estar incluido en el listado de fármacos esenciales por la Organización Mundial de la Salud, la miltefosina es considerada un medicamento «huérfano» dada su limitada disponibilidad a nivel mundial. En Europa sólo está registrada en Alemania (en España debe solicitarse como medicación extranjera) y tiene un alto coste para los sistemas sanitarios3. En España tiene un coste aproximado de 2.600€ (56 cápsulas duras de 50 mg), siendo significativamente superior al del imiquimod, terapia fodinámica con luz de día y a los antimoniales intralesionales. Sin embargo, podría ser coste-efectiva al considerar la adherencia, eficacia, costes indirectos de tiempo perdido, eventos adversos y costes directos al paciente10. Es importante destacar que la miltefosina ya no se encuentra protegida bajo patente comercial, lo que facilitaría el desarrollo de productos genéricos de menor coste.
Otra alternativa terapéutica para LC infantil es la terapia fotodinámica con luz de día, un novedoso estudio mostró una alta tasa de respuesta al aplicar el producto por el propio paciente (o sus familiares) una vez por semana hasta la resolución clínica, con mínimos efectos adversos11.
La terapia estándar de la LC puede tener una limitada adherencia en niños y efectos adversos potencialmente graves. La miltefosina puede ser una alternativa útil para el tratamiento de la leishmaniasis en estos casos, debido a su alta eficacia, administración oral y baja toxicidad.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.