Pese al avance terapéutico en la dermatitis atópica (DA), la información sobre el impacto y la interacción con las comorbilidades atópicas (como el asma, la rinoconjuntivitis y la patología ocular) es limitada. Este estudio pretende evaluar las características clínicas y epidemiológicas de pacientes con DA, así como la respuesta al tratamiento, considerando dichas comorbilidades.
Material y métodosSe realizó un análisis descriptivo de los datos del registro multicéntrico BIOBADATOP, una cohorte prospectiva de pacientes con DA que inician tratamiento sistémico, según la comorbilidad atópica.
ResultadosSe incluyeron 509 pacientes, siendo mayoritariamente adultos (81,9%), con DA grave (73,7%). Los pacientes con comorbilidad atópica personal (64%) presentaron con mayor frecuencia dermatitis flexural (89,7% vs. 81,5%), mayor media de tratamientos sistémicos utilizados (1,6 vs. 1,3) y valores basales mayores en la escala POEM (19,6 vs. 17,9). Entre los pacientes con comorbilidad atópica familiar (40,7%) hubo mayor número de pacientes pediátricos/adolescentes (24,2% vs. 13,9%) y con antecedente de rinoconjuntivitis alérgica (61,1% vs. 47,1%). No se observaron diferencias en la respuesta a los tratamientos a los 6 y 12 meses, en función de la presencia o ausencia de comorbilidades atópicas.
ConclusionesLos resultados sugieren que el antecedente de comorbilidad atópica se asocia con inicio temprano y curso persistente de la DA. Aunque no se observaron diferencias en la evolución a corto plazo, se destaca la necesidad de mayor seguimiento para comprender mejor el impacto de las comorbilidades en la DA.
Despite advances made in treatments for atopic dermatitis (AD), information on its impact and interaction with atopic comorbidities, such as asthma, rhinoconjunctivitis, and ocular disease is limited. This study aims to assess the clinical-epidemiological characteristics of patients with AD—treatment response included—while taking into consideration atopic comorbidities like these.
Materials and methodsData were analyzed from the multicenter BIOBADATOP registry (a prospective cohort of AD patients initiating systemic treatment). We conducted a descriptive analysis of the main characteristics collected in the registry in relation to atopic comorbidity.
ResultsWe included a total of 509 patients, mostly adults (81.9%) with severe AD (73.7%). Patients with personal atopic comorbidity (64%) more frequently exhibited flexural dermatitis (89.7% vs 81.5%), a higher mean of previous systemic treatments (1.6 vs. 1.3), and higher baseline values on the POEM scale (19.6 vs. 17.9). Patients with familial atopic comorbidity (40.7%) had a higher incidence of pediatric/adolescent patients (24.2% vs. 13.9%) and a history of allergic rhinoconjunctivitis (61.1% vs. 47.1%). No differences regarding treatment response were observed at the 6- and 12-month follow-ups based on the presence or absence of atopic comorbidities.
ConclusionsResults suggest that a history of atopic comorbidity is associated with an early onset and persistent course of AD. Although no differences were reported in the short-term treatment response, further follow-up is required to better understand the impact of comorbidities on AD.
La dermatitis atópica (DA) es una enfermedad inflamatoria crónica caracterizada por la presencia de brotes recurrentes e impredecibles de lesiones eczematosas. Aunque los síntomas tienden a manifestarse comúnmente antes de los 6 años, no es infrecuente que la enfermedad tenga su inicio en la edad adulta, lo que subraya la variabilidad en su presentación clínica1. La DA afecta aproximadamente al 15% de la población infantil en países desarrollados2,3 y está estrechamente relacionada con el concepto de estatus atópico, que abarca diversas enfermedades, como son las alergias alimentarias, el asma, la rinoconjuntivitis alérgica y la esofagitis eosinofílica. La interconexión de estas entidades sugiere una base genética y una respuesta inmune alterada como factores clave en el desarrollo y la persistencia de la DA4,5.
Se estima que la prevalencia de rinitis y/o asma en individuos con DA alcanza el 40,5% (distribuyéndose en un 25,7% para la rinitis y un 14,2% para asma)6, aunque puede haber variaciones significativas según la edad en la que se evalúe7. En el ámbito nacional, los resultados de la cohorte EpiChron3 mostraron que las comorbilidades crónicas más comunes en la población pediátrica con DA fueron el asma (13,1%), los trastornos psicosociales (7,9%), la discapacidad visual (7,8%), las anomalías congénitas de extremidades (5,8%) y los trastornos del desarrollo (3,2%), entre otras. Existen además, distintas cohortes publicadas donde los individuos con una presentación clínica más grave de la enfermedad tienen un riesgo más elevado de desarrollar comorbilidades, las cuales tienden a manifestarse con mayor intensidad6,8. Se destaca, por lo tanto, la importancia del adecuado cribado de las comorbilidades asociadas en estos pacientes para un correcto manejo global de la DA9.
Además del impacto de las lesiones cutáneas y las comorbilidades, el prurito persistente y el dolor asociado a la enfermedad pueden dar lugar a trastornos del sueño, ansiedad y/o depresión, lo que intensifica la carga emocional de los afectados. La necesidad de un enfoque integral se vuelve de nuevo evidente para brindar un cuidado completo y mejorar la calidad de vida de quienes viven con DA10.
En los últimos años se ha presenciado un avance en el tratamiento de la DA, gracias a la introducción de diversos tratamientos innovadores con mecanismos de acción diversos11. Estas nuevas alternativas terapéuticas abren la posibilidad de que los efectos beneficiosos se extiendan también a las comorbilidades atópicas aunque, por otro lado, el perfil de seguridad de los tratamientos podría verse modificado en función de la presencia de dichas comorbilidades12,13.
Sin embargo, la información con respecto al efecto y la interacción de los nuevos tratamientos y las comorbilidades atópicas es limitada. Esta proviene, en su mayoría, de los ensayos clínicos aleatorizados que respaldaron la aprobación comercial de los fármacos. Estos ensayos, si bien son cruciales en la aprobación y conocimiento de las expectativas de los fármacos, incluyen criterios de selección que no siempre reflejan la diversidad de pacientes presentes en la práctica clínica diaria y, a menudo, se descartan los pacientes con comorbilidades, especialmente cuando estas son de gravedad.
En este contexto, los registros que recopilan datos de pacientes en la práctica clínica habitual adquieren una importancia especial en su manejo práctico. Estos registros no solo complementan la evidencia obtenida en ensayos clínicos, sino que ofrecen una perspectiva más amplia y representativa de la efectividad y la seguridad de los tratamientos en condiciones de práctica real14.
El presente estudio tiene como objetivo describir las características clínicas y epidemiológicas de los pacientes con DA, así como la respuesta al tratamiento, en función de la presencia o ausencia de comorbilidades atópicas y antecedentes familiares de comorbilidad atópica.
Material y métodosPara la realización del estudio, se utilizaron pacientes procedentes del Registro Español de Dermatitis Atópica (BIOBADATOP). El registro BIOBADATOP ya ha sido descrito previamente14. Brevemente, se trata de una cohorte observacional prospectiva y multicéntrica, que desde su inicio en marzo de 2020, incluye a pacientes pediátricos, adolescentes y adultos con DA que han iniciado un tratamiento sistémico inmunomodulador. En las visitas iniciales se recopilan datos demográficos, información relacionada con el diagnóstico y datos basales de gravedad, medidos mediante las escalas Eczema Area and Severity Index (EASI), Dermatology Life Quality Index (DLQI) y Patient Oriented Eczema Measure (POEM). Asimismo, se registra información sobre comorbilidades y tratamientos previos utilizados. En las visitas de seguimiento, se documentan los cambios en la gravedad de la DA, el tratamiento sistémico principal y cualquier tratamiento concomitante. Además, se recopilan los eventos adversos, si los hubiera, utilizando el diccionario MedDRA.
La recopilación de datos de los pacientes en el registro se lleva a cabo mediante la asignación de un código de identificación único pseudonimizado, utilizando el sistema de captura de datos en línea Research Electronic Data Capture (REDCap).
Se realizó un análisis descriptivo de los pacientes incluidos desde el inicio (marzo de 2020) hasta el corte actual (septiembre de 2023) según presentaban comorbilidad atópica o no. La comorbilidad atópica se definió según fuese del propio paciente al presentar asma, rinoconjuntivitis alérgica o patología ocular atópica, o bien, de algún familiar de primer grado que presentase DA, asma, rinoconjuntivitis alérgica o patología ocular atópica.
El análisis estadístico se realizó mediante el programa Stata (versión 17.0 Statacorp, Texas, EE. UU.). Los datos demográficos y clínicos se describieron mediante estadísticos convencionales (medias y desviaciones estándar, frecuencias absolutas y relativas). Posteriormente se comparó la existencia de diferencias entre los grupos mediante la prueba de chi cuadrado, la prueba t de Student o la prueba de Mann-Whitney, según correspondiera. También se presentaron mediante diagramas de cajas las distintas respuestas a los tratamientos sistémicos a los 6 y 12 meses, según presencia o no de comorbilidad atópica. Un p-valor inferior a 0,05 se consideró estadísticamente significativo.
El registro BIOBADATOP ha recibido la aprobación del Comité Ético de Investigación Clínica de Aragón (PA18/051). Este proceso de aprobación se ajusta a los principios de la Declaración de Helsinki y cumple con la legislación vigente en materia ética y de investigación clínica. Todos los pacientes dieron su consentimiento por escrito para poder ser incluidos en el estudio.
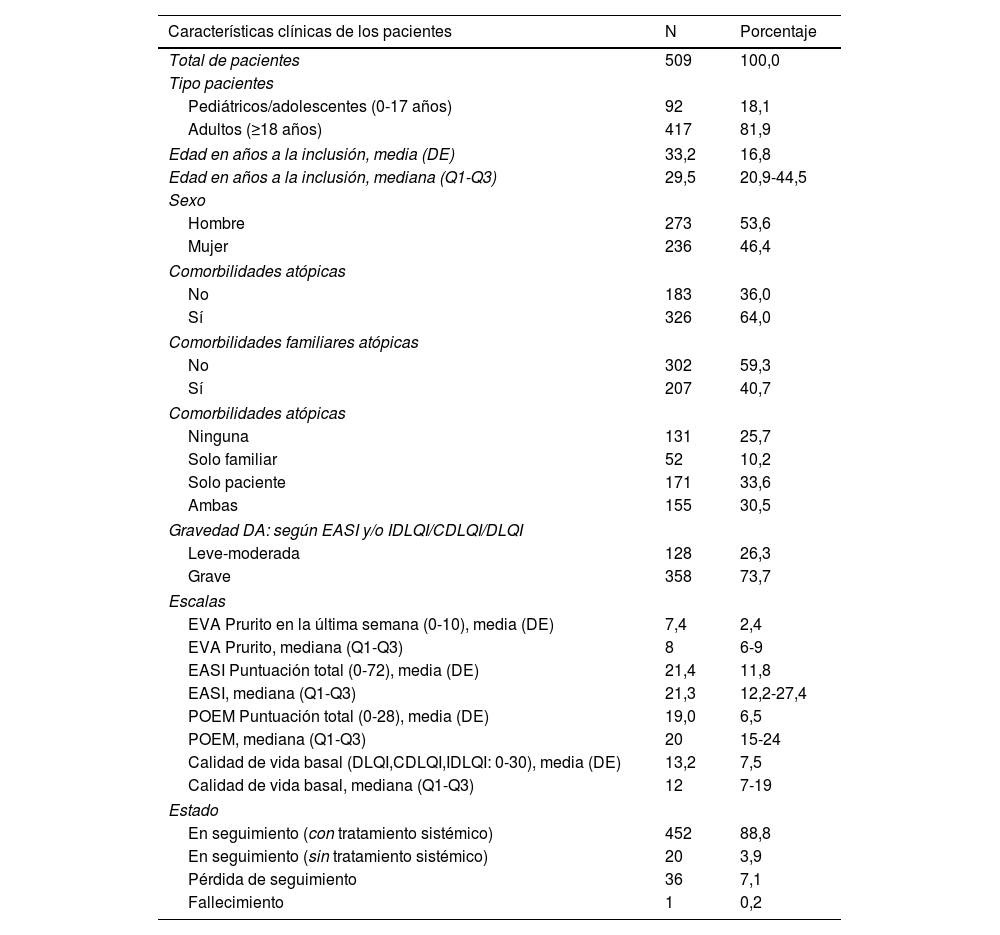
ResultadosCaracterísticas clínicas de los pacientes a estudioEn el presente estudio se incluyeron 509 pacientes con DA, procedentes del registro BIOBADATOP. La mayoría de los pacientes eran adultos (81,9%), con una mediana de edad de 29,5 años y un rango intercuartílico de 20,9 a 44,5 años. El período de seguimiento en el registro, en el momento del corte, tuvo una mediana de 9,6 meses y un rango intercuartílico de 4,8 a 21,6 meses. Un 73,7% de los pacientes presentaba una DA grave frente al 26,3% que presentaba una DA leve o moderada. Un 64% de los pacientes incluidos en el registro presentaban comorbilidad atópica personal y un 40,7% comorbilidad atópica familiar. Algunas otras características clínicas de los pacientes incluidos en el estudio se detallan en la tabla 1.
Características clínicas de los pacientes incluidos en el estudio
| Características clínicas de los pacientes | N | Porcentaje |
|---|---|---|
| Total de pacientes | 509 | 100,0 |
| Tipo pacientes | ||
| Pediátricos/adolescentes (0-17 años) | 92 | 18,1 |
| Adultos (≥18 años) | 417 | 81,9 |
| Edad en años a la inclusión, media (DE) | 33,2 | 16,8 |
| Edad en años a la inclusión, mediana (Q1-Q3) | 29,5 | 20,9-44,5 |
| Sexo | ||
| Hombre | 273 | 53,6 |
| Mujer | 236 | 46,4 |
| Comorbilidades atópicas | ||
| No | 183 | 36,0 |
| Sí | 326 | 64,0 |
| Comorbilidades familiares atópicas | ||
| No | 302 | 59,3 |
| Sí | 207 | 40,7 |
| Comorbilidades atópicas | ||
| Ninguna | 131 | 25,7 |
| Solo familiar | 52 | 10,2 |
| Solo paciente | 171 | 33,6 |
| Ambas | 155 | 30,5 |
| Gravedad DA: según EASI y/o IDLQI/CDLQI/DLQI | ||
| Leve-moderada | 128 | 26,3 |
| Grave | 358 | 73,7 |
| Escalas | ||
| EVA Prurito en la última semana (0-10), media (DE) | 7,4 | 2,4 |
| EVA Prurito, mediana (Q1-Q3) | 8 | 6-9 |
| EASI Puntuación total (0-72), media (DE) | 21,4 | 11,8 |
| EASI, mediana (Q1-Q3) | 21,3 | 12,2-27,4 |
| POEM Puntuación total (0-28), media (DE) | 19,0 | 6,5 |
| POEM, mediana (Q1-Q3) | 20 | 15-24 |
| Calidad de vida basal (DLQI,CDLQI,IDLQI: 0-30), media (DE) | 13,2 | 7,5 |
| Calidad de vida basal, mediana (Q1-Q3) | 12 | 7-19 |
| Estado | ||
| En seguimiento (con tratamiento sistémico) | 452 | 88,8 |
| En seguimiento (sin tratamiento sistémico) | 20 | 3,9 |
| Pérdida de seguimiento | 36 | 7,1 |
| Fallecimiento | 1 | 0,2 |
CDLQI: Children's Dermatology Life Quality Index; DA: dermatitis atópica; DE: desviación estándar; DLQI: Dermatology Life Quality Index; EASI: Eczema Area Severity Index; EVA: Escala Visual Analógica; IDLQI: Infant's Dermatology Life Quality Index; POEM: Patient-Oriented Eczema Measure; Q1: primer cuartil 1; Q3: tercer cuartil.
Las formas de presentación de la DA más comunes fueron la dermatitis flexural (86,8%), seguida de la dermatitis en cara-párpados (84,4%) y la dermatitis en las manos (60,1%). Como tratamientos utilizados previamente a la inclusión al registro, se encontraron como más comunes los corticosteroides orales (33,1%) seguidos de la ciclosporina (32,3%). El 23,9% de los pacientes no había utilizado ningún tratamiento previo.
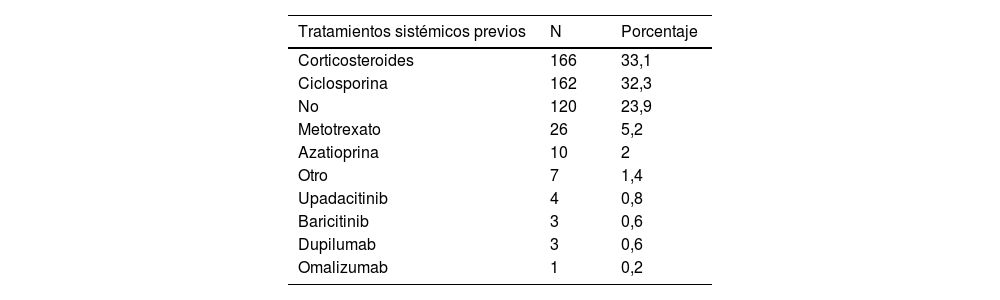
Se documentaron 749 tratamientos sistémicos iniciados, siendo dupilumab (37,1%) y ciclosporina (29,2%) los más frecuentes. Asimismo, se registraron 532 tratamientos tópicos, siendo los corticosteroides tópicos (50,4%) los más empleados. Para obtener una visión más completa de los tratamientos sistémicos y tópicos utilizados, se proporciona un desglose detallado en la tabla 2.
Tratamientos sistémicos y tópicos utilizados durante el seguimiento realizado
| Tratamientos sistémicos previos | N | Porcentaje |
|---|---|---|
| Corticosteroides | 166 | 33,1 |
| Ciclosporina | 162 | 32,3 |
| No | 120 | 23,9 |
| Metotrexato | 26 | 5,2 |
| Azatioprina | 10 | 2 |
| Otro | 7 | 1,4 |
| Upadacitinib | 4 | 0,8 |
| Baricitinib | 3 | 0,6 |
| Dupilumab | 3 | 0,6 |
| Omalizumab | 1 | 0,2 |
| Tratamientos sistémicos iniciados | N | Porcentaje |
|---|---|---|
| Dupilumab | 278 | 37,1 |
| Ciclosporina | 219 | 29,2 |
| Upadacitinib | 89 | 11,8 |
| Corticosteroides | 56 | 7,4 |
| Tralokinumab | 55 | 7,3 |
| Baricitinib | 19 | 2,5 |
| Metotrexato | 17 | 2,2 |
| Abrocitinib | 11 | 1,4 |
| Omalizumab | 1 | 0,1 |
| Otro | 4 | 0,5 |
| Tratamientos tópicos iniciados | N | Porcentaje |
|---|---|---|
| Corticosteroides | 490 | 50,4 |
| No | 441 | 45,3 |
| Inhibidores de la calcineurina | 37 | 3,8 |
| Otro | 5 | 0,5 |
Los pacientes con comorbilidad atópica presentaban con mayor frecuencia dermatitis en pliegues como forma clínica (89,7% vs. 81,5%, p=0,010), menor frecuencia de prúrigo nodular (8,5% vs. 18,1%, p=0,001), mayor número de tratamientos sistémicos utilizados previamente (1,6 vs. 1,3, p=0,010) y mayores valores medios basales de la escala POEM (19,6 vs. 17,9, p=0,021) respecto a los pacientes sin comorbilidad atópica.
No se observaron diferencias significativas entre la presencia o ausencia de comorbilidad atópica y el resto de formas clínicas de la DA, la gravedad basal en forma de EASI y/o calidad de vida, ni en la escala de EVA Prurito (véase tabla 3). Tampoco se observaron diferencias en relación con el tratamiento sistémico iniciado, fuese el primer o el segundo tratamiento utilizado.
Comparación de las características clínicas de los pacientes según presencia o ausencia de comorbilidad atópica personal
| Comorbilidades atópicas personales | ||||
|---|---|---|---|---|
| No | Sí | |||
| N | Porcentaje | N | Porcentaje | |
| Total de pacientes | 183 | 100,0 | 326 | 100,0 |
| Tipo pacientes | ||||
| Pediátricos/adolescentes (0-17 años) | 41 | 22,4 | 51 | 15,6 |
| Adultos (≥18 años) | 142 | 77,6 | 275 | 84,4 |
| P-valor=0,057 | ||||
| Sexo | ||||
| Hombre | 93 | 50,8 | 180 | 55,2 |
| Mujer | 90 | 49,2 | 146 | 44,8 |
| P-valor=0,340 | ||||
| Eczema numular | ||||
| No | 153 | 90,0 | 280 | 89,5 |
| Sí | 17 | 10,0 | 33 | 10,5 |
| P-valor=0,851 | ||||
| Prúrigo nodular | ||||
| No | 140 | 81,9 | 292 | 91,5 |
| Sí | 31 | 18,1 | 27 | 8,5 |
| P-valor=0,001 | ||||
| Eczema palmoplantar | ||||
| No | 147 | 86,5 | 276 | 87,3 |
| Sí | 23 | 13,5 | 40 | 12,7 |
| P-valor=0,785 | ||||
| Dermatitis en pliegues | ||||
| No | 32 | 18,5 | 33 | 10,3 |
| Sí | 141 | 81,5 | 288 | 89,7 |
| P-valor=0,010 | ||||
| Cara y párpados | ||||
| No | 24 | 17,8 | 41 | 14,5 |
| Sí | 111 | 82,2 | 241 | 85,5 |
| P-valor=0,393 | ||||
| Genitales | ||||
| No | 97 | 72,4 | 175 | 63,2 |
| Sí | 37 | 27,6 | 102 | 36,8 |
| P-valor=0,064 | ||||
| Manos | ||||
| No | 60 | 44,8 | 104 | 37,5 |
| Sí | 74 | 55,2 | 173 | 62,5 |
| P-valor=0,160 | ||||
| Eritrodermia | ||||
| No | 110 | 85,3 | 229 | 83,6 |
| Sí | 19 | 14,7 | 45 | 16,4 |
| P-valor=0,664 | ||||
| Tratamiento sistémico previo | ||||
| No | 50 | 27,9 | 70 | 21,7 |
| Sí | 129 | 72,1 | 253 | 78,3 |
| P-valor=0,115 | ||||
| Número de tratamientos sistémico previo, media (DE) | 1,3 | 1,2 | 1,6 | 1,5 |
| P-valor=0,010 | ||||
| Fototerapia previa | ||||
| No | 129 | 71,7 | 202 | 63,5 |
| Sí | 51 | 28,3 | 116 | 36,5 |
| P-valor=0,064 | ||||
| Gravedad DA: según EASI y/o IDLQI/CDLQI/DLQI | ||||
| Leve-moderada | 50 | 29,4 | 78 | 24,7 |
| Grave | 120 | 70,6 | 238 | 75,3 |
| P-valor=0,259 | ||||
| EVA Prurito en la última semana (0-10), media (DE) | 7,2 | 2,6 | 7,5 | 2,2 |
| P-valor=0,248 | ||||
| EASI Puntuación total (0-72), media (DE) | 20,7 | 11,2 | 21,8 | 12,1 |
| P-valor=0,339 | ||||
| POEM Puntuación total (0-28), media (DE) | 17,9 | 6,9 | 19,6 | 6,3 |
| P-valor=0,021 | ||||
| Calidad de vida basal (DLQI,CDLQI,IDLQI: 0-30), media (DE) | 12,3 | 7,8 | 13,6 | 7,3 |
| P-valor=0,122 | ||||
CDLQI: Children's Dermatology Life Quality Index; DA: dermatitis atópica; DE: desviación estándar; DLQI: Dermatology Life Quality Index; EASI: Eczema Area Severity Index; EVA: Escala Visual Analógica; IDLQI: Infant's Dermatology Life Quality Index; POEM: Patient-Oriented Eczema Measure.
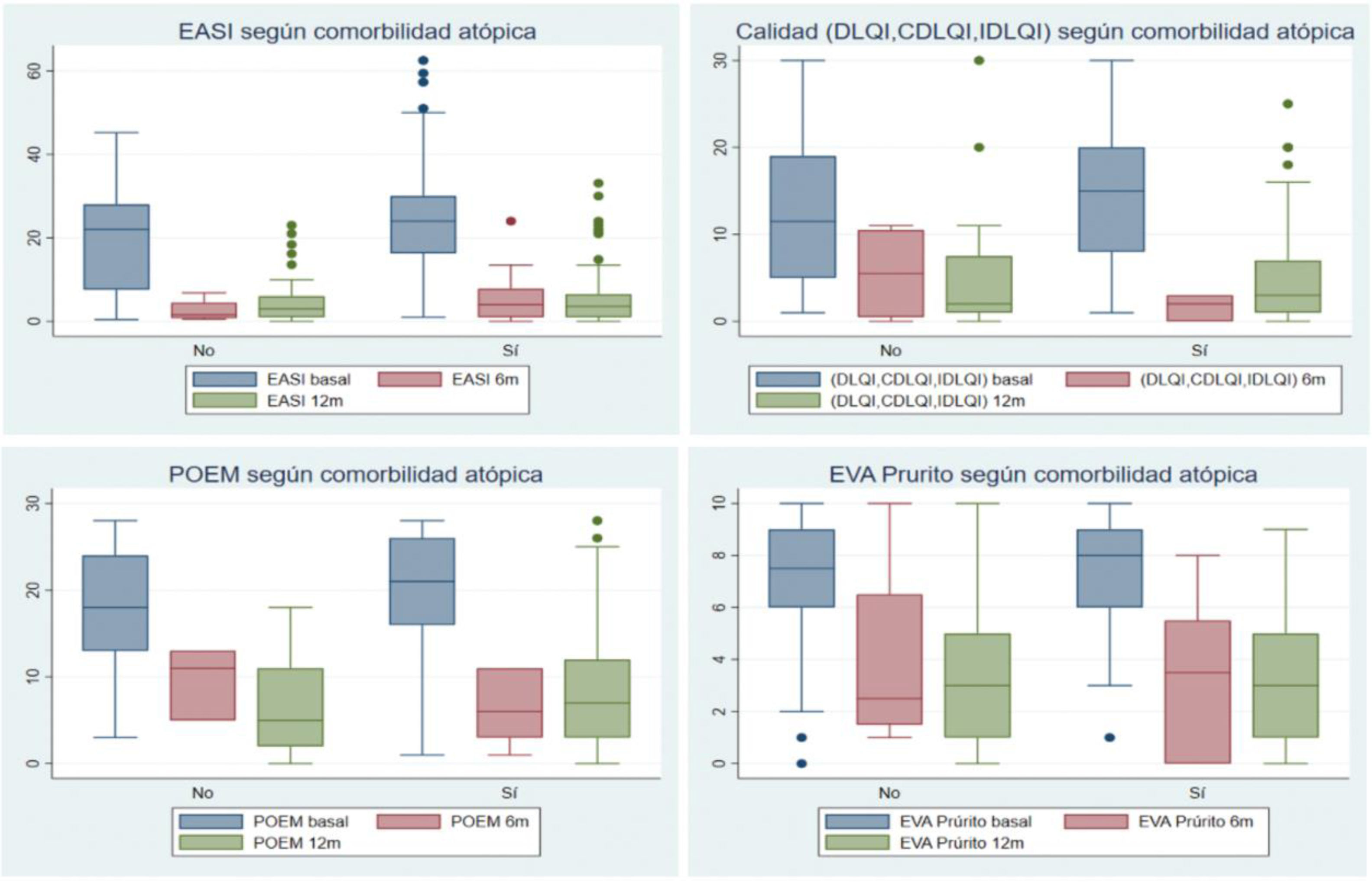
Finalmente, no se evidenciaron diferencias en relación con los antecedentes personales de comorbilidad atópica en la suspensión del primer o segundo fármacos prescritos, en el motivo de suspensión o cambio, en la posología utilizada, ni en la respuesta a los tratamientos sistémicos a los 6 y 12 meses (este último aspecto se representa en la figura 1).
Diagramas de cajas acerca de la respuesta a los tratamientos sistémicos a los 6 y 12 meses, en función de presentar o no comorbilidad atópica personal. Se evaluaron las respuestas a través de escalas de medición de la gravedad de la dermatitis atópica como son: el EASI, las escalas de calidad de vida (DLQI/IDLQI/CDLQI), el POEM y el EVA Prurito (en la última semana). No se observaron diferencias significativas en los pacientes con comorbilidad atópica personal respecto los que no presentaban dicha comorbilidad.
Entre los pacientes con comorbilidad atópica familiar hubo mayor número de pacientes pediátricos/adolescentes (24,2% vs. 13,9%, p=0,003) y presentaron con mayor frecuencia antecedentes de rinoconjuntivitis alérgica (61,1% vs. 47,1%, p=0,002), respecto los pacientes sin comorbilidad atópica familiar (véase tabla 4).
Comparación de las características clínicas de los pacientes según presencia o ausencia de comorbilidad atópica familiar
| Comorbilidades familiares atópicas | ||||
|---|---|---|---|---|
| No | Sí | |||
| N | Porcentaje | N | Porcentaje | |
| Total de pacientes | 302 | 100,0 | 207 | 100,0 |
| Tipo pacientes | ||||
| Pediátricos/adolescentes (0-17 años) | 42 | 13,9 | 50 | 24,2 |
| Adultos (≥18 años) | 260 | 86,1 | 157 | 75,8 |
| P-valor=0,003 | ||||
| Sexo | ||||
| Hombre | 164 | 54,3 | 109 | 52,7 |
| Mujer | 138 | 45,7 | 98 | 47,3 |
| P-valor=0,714 | ||||
| Asma | ||||
| No | 167 | 58,8 | 107 | 52,2 |
| Sí | 117 | 41,2 | 98 | 47,8 |
| P-valor=0,146 | ||||
| Rinoconjuntivitis alérgica | ||||
| No | 147 | 52,9 | 79 | 38,9 |
| Sí | 131 | 47,1 | 124 | 61,1 |
| P-valor=0,002 | ||||
| Patología ocular atópica | ||||
| No | 234 | 86,3 | 164 | 80,8 |
| Sí | 37 | 13,7 | 39 | 19,2 |
| P-valor=0,102 | ||||
| Eczema numular | ||||
| No | 257 | 91,1 | 176 | 87,6 |
| Sí | 25 | 8,9 | 25 | 12,4 |
| P-valor=0,203 | ||||
| Prúrigo nodular | ||||
| No | 251 | 86,9 | 181 | 90,0 |
| Sí | 38 | 13,1 | 20 | 10,0 |
| P-valor=0,281 | ||||
| Eczema palmoplantar | ||||
| No | 253 | 88,8 | 170 | 84,6 |
| Sí | 32 | 11,2 | 31 | 15,4 |
| P-valor=0,175 | ||||
| Dermatitis en pliegues | ||||
| No | 44 | 15,1 | 21 | 10,3 |
| Sí | 247 | 84,9 | 182 | 89,7 |
| P-valor=0,122 | ||||
| Cara y párpados | ||||
| No | 37 | 15,5 | 28 | 15,7 |
| Sí | 202 | 84,5 | 150 | 84,3 |
| P-valor=0,944 | ||||
| Genitales | ||||
| No | 160 | 68,1 | 112 | 63,6 |
| Sí | 75 | 31,9 | 64 | 36,4 |
| P-valor=0,345 | ||||
| Manos | ||||
| No | 89 | 38,0 | 75 | 42,4 |
| Sí | 145 | 62,0 | 102 | 57,6 |
| P-valor=0,373 | ||||
| Eritrodermia | ||||
| No | 187 | 81,7 | 152 | 87,4 |
| Sí | 42 | 18,3 | 22 | 12,6 |
| P-valor=0,121 | ||||
| Tratamiento sistémico previo | ||||
| No | 74 | 25,0 | 46 | 22,3 |
| Sí | 222 | 75,0 | 160 | 77,7 |
| P-valor=0,490 | ||||
| Número de tratamientos sistémicos previos, media (DE) | 1,5 | 1,4 | 1,5 | 1,3 |
| P-valor=0,732 | ||||
| Fototerapia previa | ||||
| No | 198 | 66,9 | 133 | 65,8 |
| Sí | 98 | 33,1 | 69 | 34,2 |
| P-valor=0,807 | ||||
| Gravedad DA: según EASI y/o IDLQI/CDLQI/DLQI | ||||
| Leve-moderada | 74 | 25,9 | 54 | 27,0 |
| Grave | 212 | 74,1 | 146 | 73,0 |
| P-valor=0,781 | ||||
| EVA Prurito en la última semana (0-10), media (DE) | 7,4 | 2,3 | 7,3 | 2,5 |
| P-valor=0,554 | ||||
| EASI Puntuación total (0-72), media (DE) | 22,1 | 11,9 | 20,4 | 11,5 |
| P-valor=0,137 | ||||
| POEM Puntuación total (0-28), media (DE) | 19,4 | 6,2 | 18,6 | 7,0 |
| P-valor=0,239 | ||||
| Calidad de vida basal (DLQI,CDLQI,IDLQI: 0-30), media (DE) | 13,4 | 7,4 | 12,9 | 7,6 |
| P-valor=0,500 | ||||
CDLQI: Children's Dermatology Life Quality Index; DA: dermatitis atópica; DE: desviación estándar; DLQI: Dermatology Life Quality Index; EASI: Eczema Area Severity Index; EVA: Escala Visual Analógica; IDLQI: Infant's Dermatology Life Quality Index; POEM: Patient-Oriented Eczema Measure.
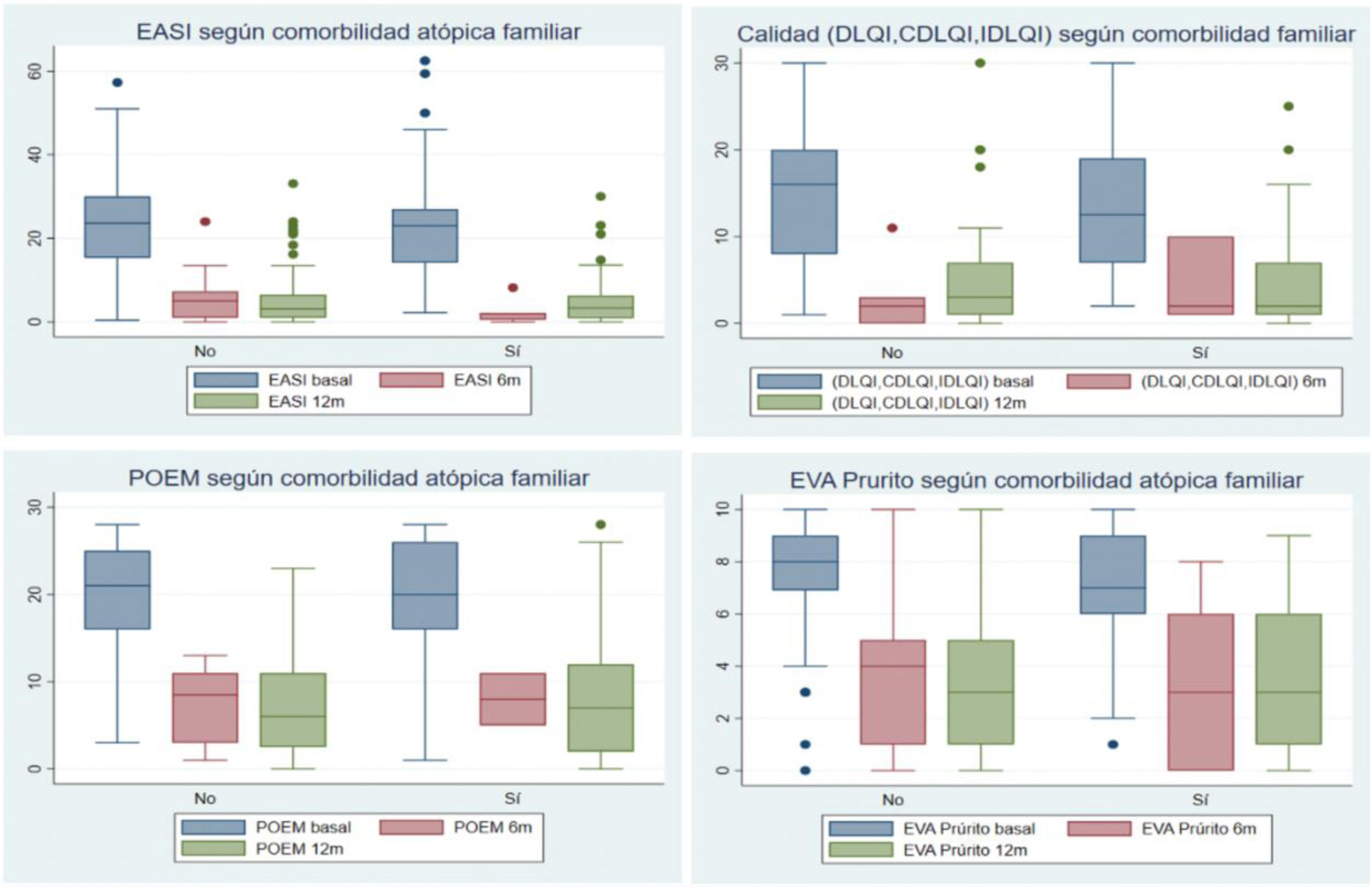
No se objetivaron diferencias en ambos grupos para el resto de variables evaluadas, ni en relación con la respuesta a los tratamientos sistémicos a los 6 y 12 meses (representado en la figura 2).
Diagramas de cajas acerca de la respuesta a los tratamientos sistémicos a los 6 y 12 meses, en función de presentar o no comorbilidad atópica familiar. Se evaluaron las respuestas a través de escalas de medición de la gravedad de la dermatitis atópica como son el EASI, las escalas de calidad de vida (DLQI/IDLQI/CDLQI), el POEM y el EVA Prurito (en la última semana). No se observaron diferencias significativas en los pacientes con comorbilidad atópica familiar respecto los que no presentaban dicha comorbilidad.
En nuestro estudio sobre DA y comorbilidad atópica, observamos similitudes en la mayoría de las características clínicas entre pacientes con y sin este antecedente. Sin embargo, aquellos con comorbilidad atópica mostraron mayor frecuencia de dermatitis flexural, un inicio más precoz de la DA, un mayor uso previo de tratamientos sistémicos y una puntuación basal más elevada en la escala POEM. Estos resultados permiten sugerir un perfil clínico caracterizado por un inicio temprano y un recorrido terapéutico extenso, implicando una mayor posibilidad de impacto por efectos secundarios de los tratamientos sistémicos. El mayor impacto del POEM puede indicar, en el contexto de unas características clínicas y una gravedad similares a los pacientes sin antecedente de comorbilidad atópica, un mayor impacto en la percepción de la enfermedad por parte del paciente. El efecto acumulativo del impacto tanto físico, psíquico e inflamatorio de la enfermedad cutánea puede tener también un efecto relevante en el recorrido vital del paciente, condicionando sus expectativas y perspectivas a lo largo de su vida, lo que se ha definido como cumulative life course impairment (CLCI)15. Es preciso destacar que la mayoría de los estudios en la literatura respaldan la idea de que las comorbilidades atópicas están asociadas con una mayor afectación en la percepción de la enfermedad y la calidad de vida16. Sin embargo, existen registros, como la cohorte italiana AtopyReg17, que presentan resultados opuestos a esta tendencia. Esto último podría deberse, según los autores, a la menor frecuencia de comorbilidades atópicas en pacientes con DA de inicio tardío, que se caracterizan por presentar puntajes más altos en las diversas escalas de evaluación utilizadas.
En cuanto a los pacientes con antecedentes familiares de atopia, nuestro estudio revela que hay un porcentaje mayor de pacientes pediátricos/adolescentes, circunstancia que indica, al igual que los antecedentes personales de comorbilidad atópica, una mayor probabilidad de un inicio precoz y un largo recorrido en la enfermedad. Además, estos pacientes presentaron con mayor frecuencia antecedentes de rinoconjuntivitis alérgica, coincidiendo con estudios previos que destacan la asociación entre rinitis alérgica y DA de inicio temprano18. A nivel nacional, la cohorte EpiChron también evidenció una relación significativa entre la rinitis alérgica y/o el asma en pacientes con DA, en el grupo de edades comprendidas entre los 3 y 10 años19.
Los antecedentes de comorbilidad atópica podrían funcionar, por lo tanto, como un marcador asociado a enfermedad precoz y prolongada, lo que podría hacer conveniente una gestión personalizada para minimizar el impacto de la enfermedad. De este modo, se ha comprobado cómo los adultos con DA y asma concomitante tenían patrones diferentes de utilización de la atención médica, con un mayor riesgo de hospitalización y visitas no programadas, en comparación con los adultos con DA o asma de forma separada20. Estos datos sugieren que el abordaje de forma integral tanto de la DA como de sus comorbilidades podría contribuir a reducir los costes de atención médica.
Otro aspecto de interés es el de conocer el impacto de estas comorbilidades en la evolución de la enfermedad con los tratamientos utilizados en la práctica clínica real, en particular, con los tratamientos innovadores. De los tratamientos disponibles, únicamente dupilumab presenta indicación en comorbilidades atópicas como asma, poliposis nasal o esofagitis eosinofílica. Para el resto de fármacos, la información es escasa y la presencia de comorbilidades incluso puede haber limitado el reclutamiento en ensayos clínicos21. Por este motivo, algunos autores han propuesto la elección de dupilumab en pacientes con comorbilidades22. En nuestro estudio, sin embargo, no se han observado diferencias significativas en la elección y la respuesta a los tratamientos (a los 6 y 12 meses) en función de la presencia o ausencia de comorbilidad atópica. A pesar de la falta de diferencias a corto plazo, la posibilidad de efectos a más largo plazo o la influencia de factores específicos en la respuesta a los tratamientos merecen un análisis más profundo, a partir de nuevos trabajos en este campo.
Es relevante reconocer las limitaciones del estudio, entre ellas se encuentran las propias de un estudio observacional, en el que es difícil evitar el efecto de las variables de confusión. Se debe tener en cuenta que, aunque se trata de un estudio multicéntrico, los pacientes incluidos provienen de centros especializados y es probable que estén más dispuestos a participar en investigaciones. Esta circunstancia podría limitar la generalización de los resultados a toda la población. En cuanto a los tratamientos utilizados, es importante considerar que fármacos como dupilumab estuvieron disponibles varios años antes que otras opciones terapéuticas, lo que podría haber influido en el número de pacientes tratados y en los patrones de prescripción, más allá de las características inherentes del fármaco. Por otra parte, los seguimientos del estudio aún son breves, siendo la mayoría de pacientes incluidos durante el último año. Tampoco se dispone de información sobre la actividad de las comorbilidades atópicas y su gravedad, que puede ser un factor relevante en la toma de decisiones. De hecho, parece plausible en el contexto de los datos presentados, que sea la actividad de la comorbilidad atópica (y su necesidad de tratamiento) el criterio que en mayor medida pueda influir en la elección del tratamiento, y no el antecedente en sí mismo. Como fortalezas destacamos el tamaño muestral obtenido mediante la recopilación prospectiva de datos, realizada de forma rigurosa a través del registro BIOBADATOP. Asimismo, se trata de una recogida de datos a nivel nacional, obteniendo una muestra diversa y amplia de los diferentes centros hospitalarios participantes, que refuerza la representatividad de los hallazgos obtenidos, mejorando la validez externa del estudio.
En definitiva, los antecedentes de comorbilidades personales o familiares podrían estar asociados a un inicio más precoz y un curso más persistente de la enfermedad, circunstancia relevante en la toma de decisiones en la práctica clínica real. Se requerirá un seguimiento a mayor largo plazo para comprender mejor la evolución de la enfermedad en estos subgrupos de pacientes y la respuesta a los nuevos tratamientos sistémicos.
FinanciaciónEste estudio forma parte de las publicaciones del registro BIOBADATOP, proyecto promovido por la Fundación Piel Sana de la AEDV, que a su vez cuenta con respaldo financiero de empresas farmacéuticas (como Sanofi, AbbVie, Pfizer y Almirall). Se llevó a cabo de manera independiente en cuanto a la planificación y ejecución del estudio. Las compañías farmacéuticas colaboradoras no tuvieron participación en el diseño, recopilación, gestión, análisis e interpretación de datos, así como en la preparación, revisión y aprobación del manuscrito. La decisión de enviar el manuscrito para su publicación también se tomó de manera autónoma, sin intervención de las empresas farmacéuticas colaboradoras.
Nuestro agradecimiento a todos los investigadores involucrados en el registro BIOBADATOP, por realizar un esfuerzo adicional en su práctica clínica diaria con la recogida de datos, así como a los pacientes o representantes legales por su disposición a acceder en la inclusión en el registro. Su participación es esencial para el avance del conocimiento en la DA, contribuyendo significativamente al progreso científico en este campo. Este trabajo ha sido realizado en el marco del programa Doctorado en Medicina de la Universidad Autónoma de Barcelona (M. Munera-Campos).