Desde la introducción de la inmunoterapia el tratamiento del melanoma ha sufrido una revolución, consiguiéndose cifras de supervivencia superiores a las que se alcanzaban con los tratamientos previos. Los fármacos inmunomoduladores disponibles actualmente van dirigidos principalmente frente a las moléculas de superficie CTLA-4 y PD-1, que ejercen un efecto inhibidor sobre la respuesta inmune antitumoral. Se trata de un tratamiento en pleno proceso de expansión, y la investigación se dirige hacia el descubrimiento de nuevas moléculas, las combinaciones de los fármacos disponibles o la identificación de biomarcadores que permitan seleccionar a los pacientes idóneos para cada terapia.
Approaches to treating melanoma have changed radically since the introduction of immunotherapy, and survival figures are now higher than possible with earlier therapies. The immunomodulators currently available mainly block CTLA-4 (cytotoxicT lymphocyte-associated molecule-4) and PD-1 (programed cell death protein 1) translocated to the cell surface, where they inhibit the antitumor immune response. Treatments blocking these molecules are being more widely used. Research now seeks new molecular targets, the best combinations of available drugs, and biomarkers that can identify ideal candidates for each one.
El melanoma es el 8.° cáncer en frecuencia y supone un 5% de los casos nuevos de cáncer, con un incremento mantenido en la incidencia1,2. En la población española el melanoma cutáneo tiene una tasa de incidencia de 8,7 por cada 100.00 habitantes3. La tasa de supervivencia en estadios precoces es superior al 95%, sin embargo en las formas diseminadas el pronóstico empeora considerablemente, con una supervivencia inferior al 20% a los 5 años2. El tratamiento con quimioterapia era la opción más aceptada en fases avanzadas, sin embargo las tasas de respuesta son inferiores al 15% y muestra escasa repercusión en la supervivencia4.
En la búsqueda de alternativas terapéuticas un campo fundamental ha sido el descubrimiento de la inmunoterapia. Desde hace décadas se conoce la relación que existe entre el sistema inmune y las células neoplásicas, y en este aspecto el melanoma cutáneo es probablemente uno de los tumores más inmunogénicos que existen. Sin embargo, la interacción entre el sistema inmune y el melanoma es dinámica, y las células tumorales poseen diversos mecanismos que les permiten evadir el reconocimiento y destrucción mediada por el sistema inmune, lo que favorece la progresión de la enfermedad5.
Durante años, las estrategias terapéuticas fueron dirigidas a incrementar la respuesta inmune mediante vacunas y bioquimioterapia, pero con resultados desalentadores6,7. Recientemente se ha recibido con entusiasmo el abordaje mediante una nueva estrategia: el uso de anticuerpos monoclonales frente a inhibidores de la respuesta inmune8.
Evidencia de la respuesta inmune en el melanomaA diferencia de otros tumores, en el caso del melanoma existen diversos hallazgos evidentes, tanto clínica como histológicamente, que demuestran la respuesta del sistema inmune frente al tumor9.
En la mayoría de los melanomas es habitual observar la presencia de un infiltrado inflamatorio tanto intra como peritumoral, y puede acompañarse de regresión tumoral. Los fenómenos de regresión aparecen hasta en un 35% de los casos de melanoma, y es una manifestación 6 veces más frecuente en el melanoma que en otros tumores10.
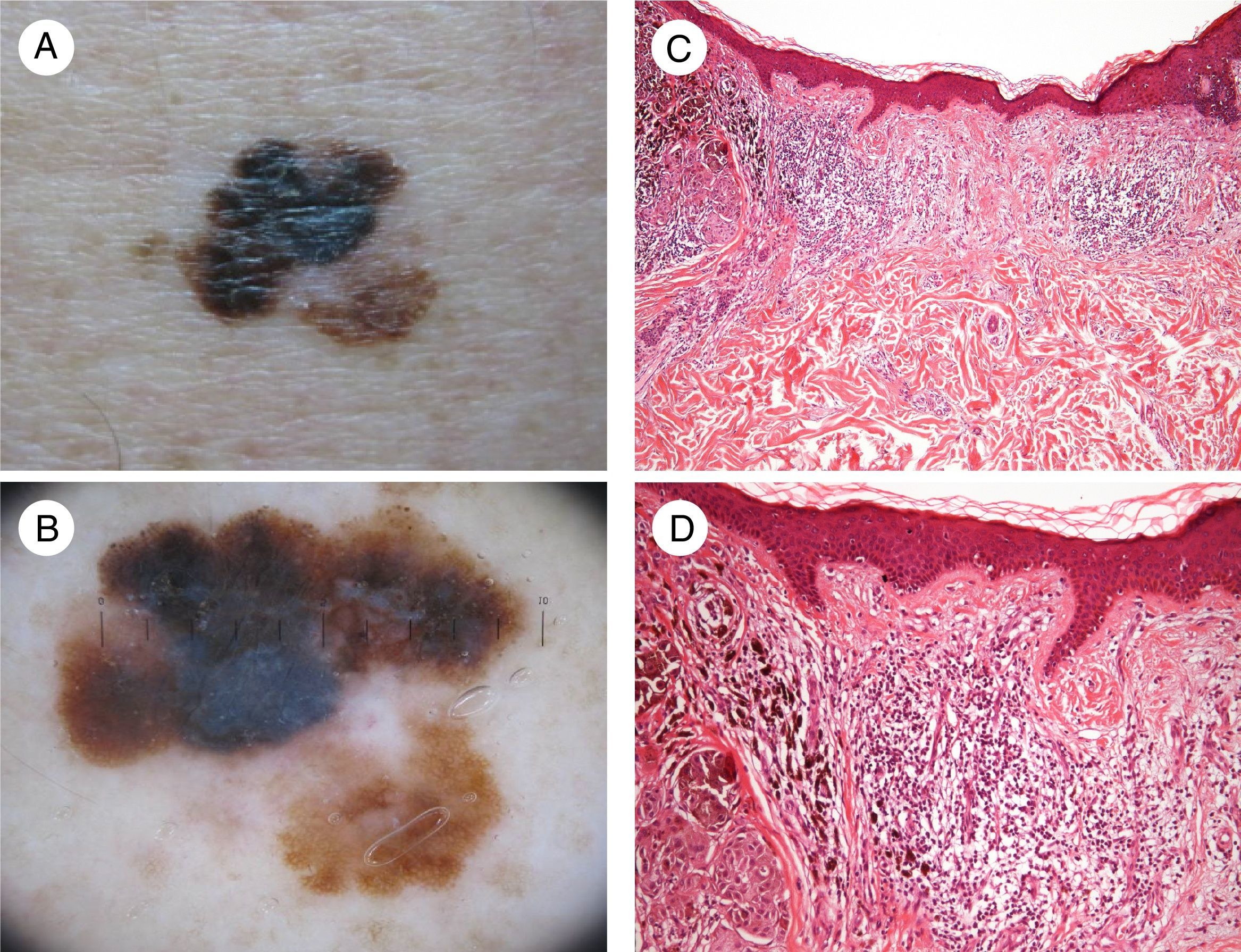
Otra característica descrita recientemente es la correlación entre la densidad de vénulas de endotelio alto y la densidad linfocitaria, asociadas a una mayor regresión del melanoma11. Además, la presencia de regresión se asocia a melanomas con un índice mitótico más bajo; es decir, a melanomas con una tasa de proliferación menor y por tanto mejor pronóstico12 (fig. 1).
Imagen de regresión en un melanoma. A. Imagen clínica en la que se aprecia una zona central con pérdida de pigmento. B. Dermatoscopia de la lesión que muestra un patrón multicomponente con un área blanca central. C y D. Imágenes histológicas donde se aprecia infiltrado linfocitario denso en la dermis sin alteración epidérmica, melanofagia y fibrosis de la dermis (hematoxilina-eosina, C [10x] y D [20x], aumentos de microscopio óptico).
El fenómeno de halo que aparece alrededor de los nevus es otra manifestación de autoinmunidad que puede llegar a producir la desaparición completa del nevus. También puede observarse la aparición de vitíligo en un 2-7% de los casos de melanoma avanzado tras la terapia sistémica, y se ha relacionado con una mejora del pronóstico13.
Aunque estos hechos solamente permiten formular hipótesis, numerosas investigaciones han demostrado la participación del sistema inmune en estos procesos: El infiltrado tumoral está compuesto fundamentalmente por linfocitos T, que son los mediadores de la respuesta inmune innata14. También, en los melanomas que presentan una regresión extensa se ha comprobado una amplificación oligoclonal de los linfocitos T15, y además, la transferencia celular adoptiva de linfocitos T aislados a partir de melanomas en regresión posee actividad citolítica frente a melanomas autólogos16.
Sin embargo, el desarrollo del melanoma supone un fracaso de la capacidad defensiva del sistema inmunitario. En dicho fracaso participan tanto factores propios de las células tumorales, como alteraciones del sistema de defensa en el que disminuye la capacidad para llevar a cabo su función efectora.
La activación subóptima de los linfocitos T específicos por una expresión escasa o ausente de antígenos en las células del melanoma es un hecho conocido que conduce al fracaso en la respuesta inmune17. También hay una disminución de la expresión de moléculas de adhesión endotelial en el tumor y además, ciertas células presentes en el infiltrado tumoral, como los macrófagos, secretan factores de crecimiento, citoquinas y factores supresores de la respuesta inmune18,19.
Por tanto, la respuesta inmune antitumoral de manera aislada no es suficiente para producir la eliminación de las células neoplásicas, pero sí facilitará la respuesta al tratamiento con inmunoterapia.
Antígenos frente a los que se desencadena la respuesta inmunePara la activación del linfocito T son necesarias 2 señales. El receptor de la célula T (TCR) reconoce el antígeno presentado por las células dendríticas a través del complejo mayor de histocompatibilidad (MHC). Por otro lado, el cluster of differentiation 28 (CD28) de la célula T, mediante la unión a sus ligandos B7-1 o B7-2, produce una señal coactivadora. En ausencia de esta segunda señal, la célula T no respondería ante el estímulo desencadenante y se produciría anergia20.
Estas células activadas deben migrar hasta la región del tumor y producir una respuesta de destrucción tumoral21. Sin embargo, es frecuente que estos linfocitos intratumorales tengan una capacidad de proliferación, producción de citoquinas y citólisis disminuida; aunque fuera del microambiente tumoral estas células demuestran una respuesta específica potente. Estos hechos sugieren que existen ciertas señales al nivel del microambiente tumoral que inhiben la función linfocitaria22.
La activación del TCR también produce señales que estimulan mediadores inhibitorios. El antígeno citotóxico de los linfocitos T (cytotoxic T-lymphocyte antigen [CTLA-4]) y la molécula muerte celular programada (programmed cell death 1 [PD-1]) son 2 receptores celulares de superficie implicados en la regulación de las células T activadas. Pertenecen a la superfamilia B7/CD28 y al unirse a sus ligandos, desencadenan vías inhibitorias que amortiguan la actividad de las células T23.
Antígeno citotóxico de los linfocitos TTras la activación de los linfocitos T, estos expresan CTLA-4. Este receptor se expresa entre 24-48horas después de la activación, y se une a B7 con una mayor afinidad que CD28, causando una señal supresora en las células T24.
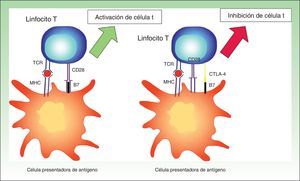
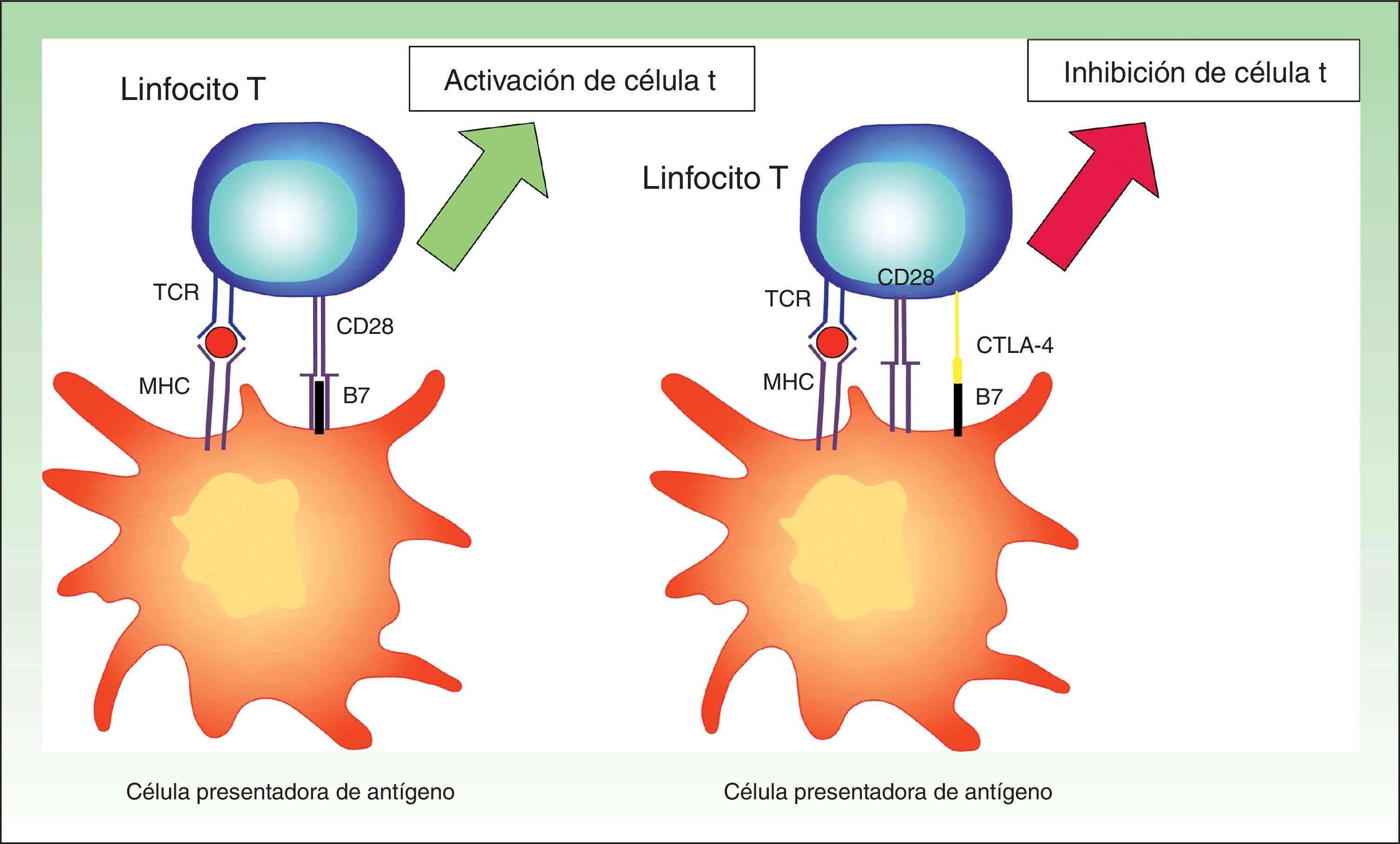
Es un potente coinhibidor implicado en el desarrollo de tolerancia desde etapas tempranas. Como demostraron los ensayos con ratones CTLA-4-/-, la falta de esta molécula producía un infiltrado masivo de linfocitos autoinmunes en diversos tejidos, provocando la muerte en las primeras 2 o 3 semanas25,26 (fig. 2).
Imagen esquemática de la activación de la célula T. Activación de la célula T tras la interacción entre el receptor de la célula T y el HLA y entre las moléculas coestimuladoras B7 y CD28 (izquierda). Inhibición de la respuesta tras la unión del CTLA-4 a B7 (derecha).
MHC: complejo mayor de histocompatibilidad; TCR: receptor de célula T.
Molécula de muerte celular programada 1 (PD1) y ligando de la molécula de muerte programada 1 (PD-L1)
PD-1 es un receptor transmembrana de la familia CD28 que normalmente se expresa en linfocitos CD4+ y CD8+ activados27. Tiene una función inmunosupresora, que en condiciones normales evita una respuesta inmune excesiva frente a células propias. La expresión de PD-1 es inducida por la activación de los linfocitos T, y deja de expresarse cuando la respuesta inmune ha eliminado el antígeno. Sin embargo, si la respuesta no es eficaz, la expresión de PD-1 se mantiene y genera un fenotipo de linfocitos T ineficaces28.
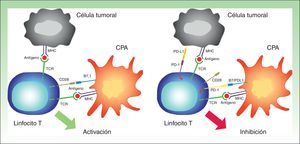
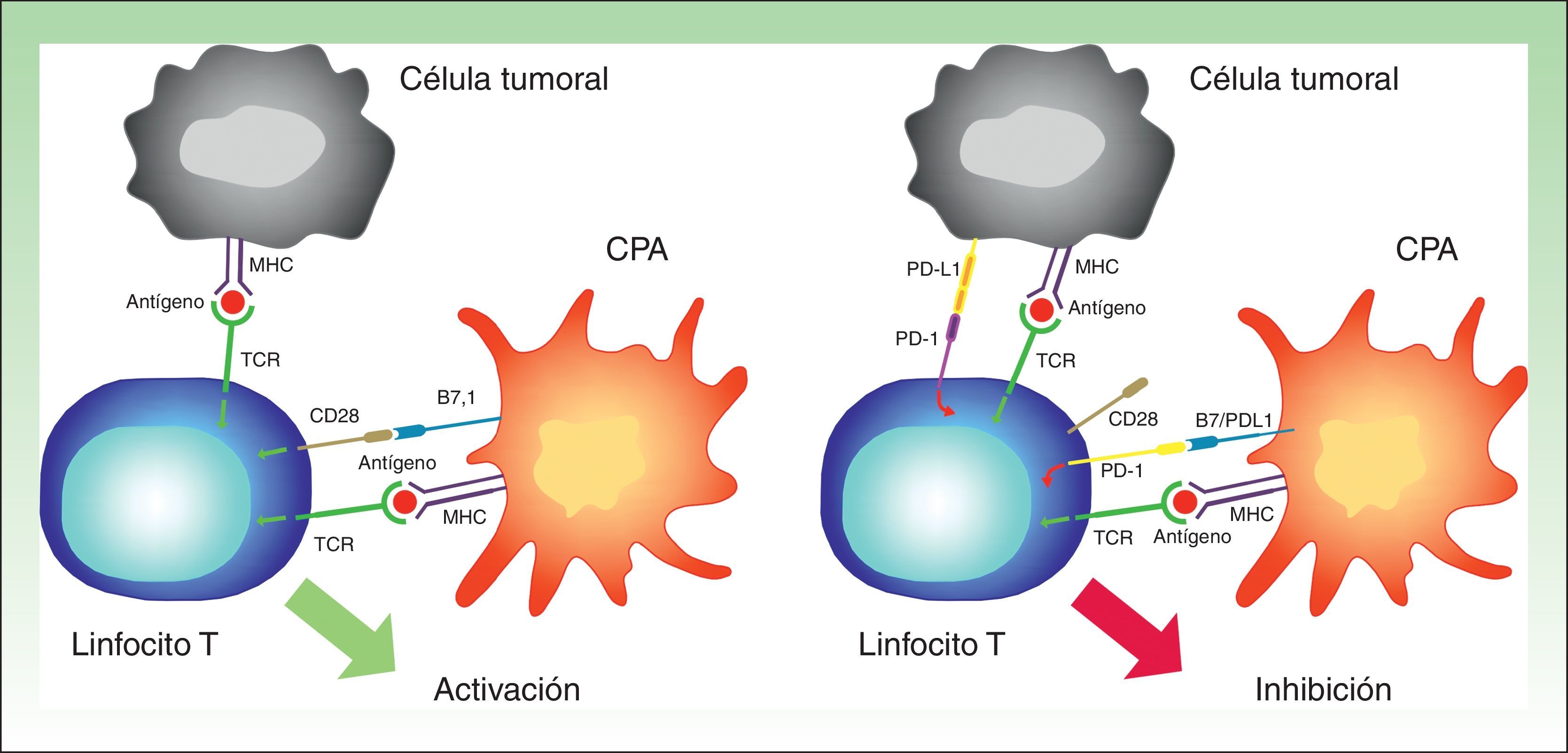
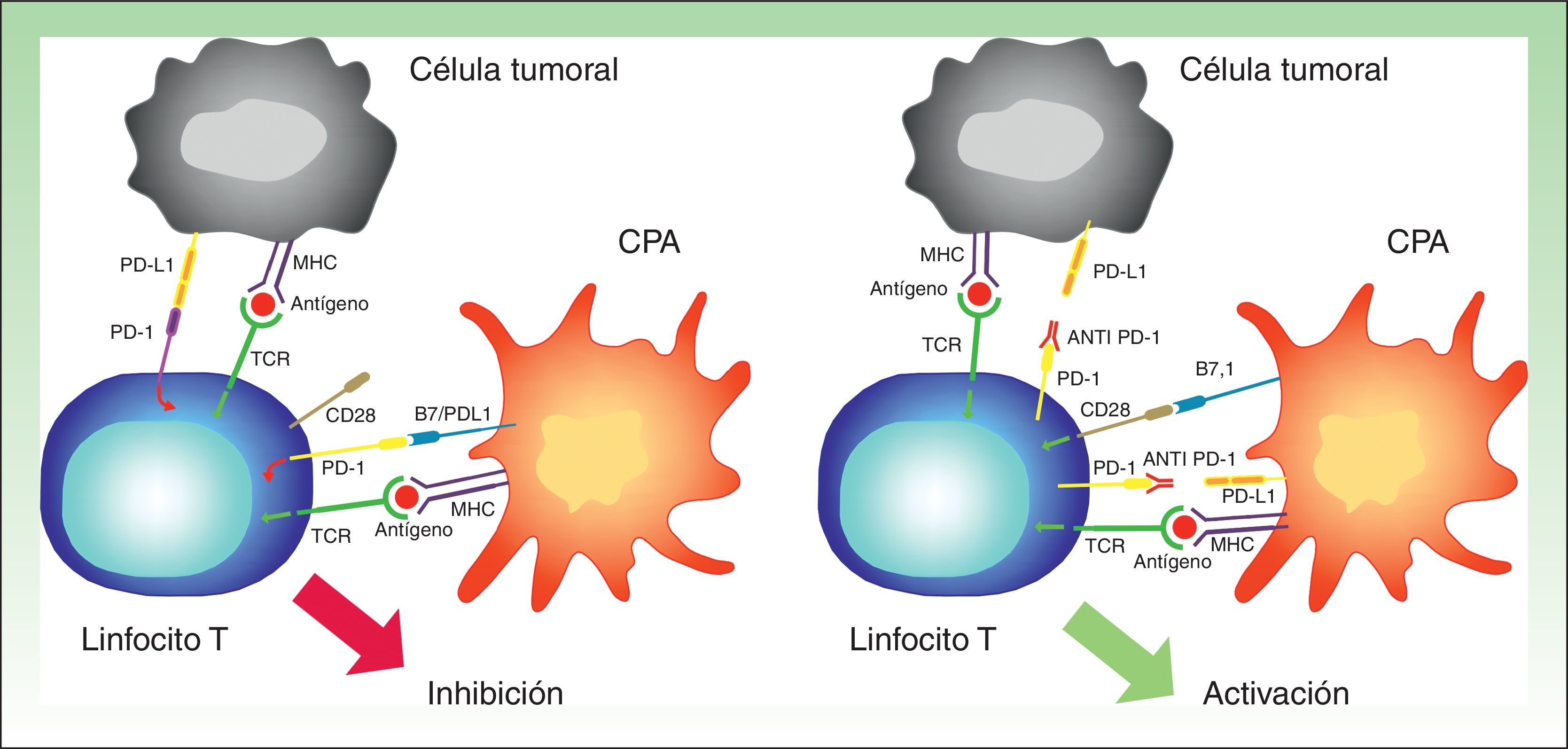
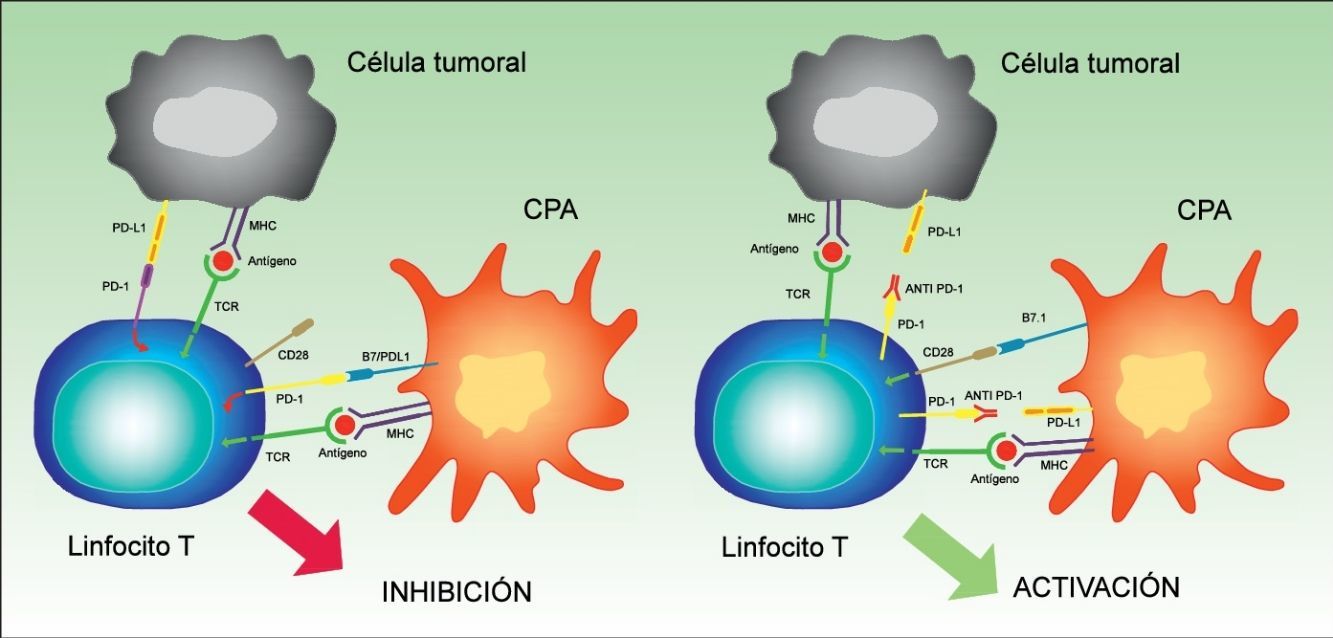
PD-1 tiene 2 ligandos: PD-L1 (también B7-H1 o CD274) y PD-L2 (B7-DC o CD273), siendo el primero el que se expresa en un mayor número de células. Cuando PD-L1 se expresa en la superficie de las células tumorales y se une a PD-1 de las células T, se activa una cascada de señalización que inactiva la respuesta del TCR, y por tanto impide la secreción de factores de crecimiento y señales de supervivencia29. En definitiva, la unión del PD-1 de los linfocitos a su ligando desempeña un papel fundamental al bloquear la respuesta inmune. (fig. 3).
Imagen esquemática de la actividad de PD-1 y PD-L1. A la izquierda activación de la célula T por interacción entre las moléculas activadoras y coactivadoras. A la derecha inhibición de la célula T tras la unión de PD-1 a PD-L1.
CPA: célula presentadora de antígenos; MHC: complejo mayor de histocompatibilidad; TCR: receptor del linfocito T.
Desde los años 80 se han diseñado múltiples fórmulas terapéuticas dirigidas a estimular la respuesta inmune antitumoral con un éxito limitado16. Sin embargo, en los últimos años ha surgido una nueva estrategia basada, más que en la activación directa del sistema inmune, en el bloqueo de los receptores que inhiben la respuesta inmune frente al tumor. Los anticuerpos empleados en estos tratamientos no se unen a las células tumorales, sino a los linfocitos, con el fin de activar su respuesta.
Inhibición de antígeno citotóxico de los linfocitos TDos o 3 días después de la activación de los linfocitos T se expresa CTLA-4 en su superficie, y produce una disminución de la actividad linfocitaria30. Por tanto, el bloqueo de este receptor permitiría el mantenimiento de la actividad de los linfocitos T específicos.
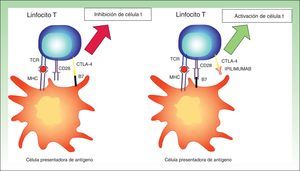
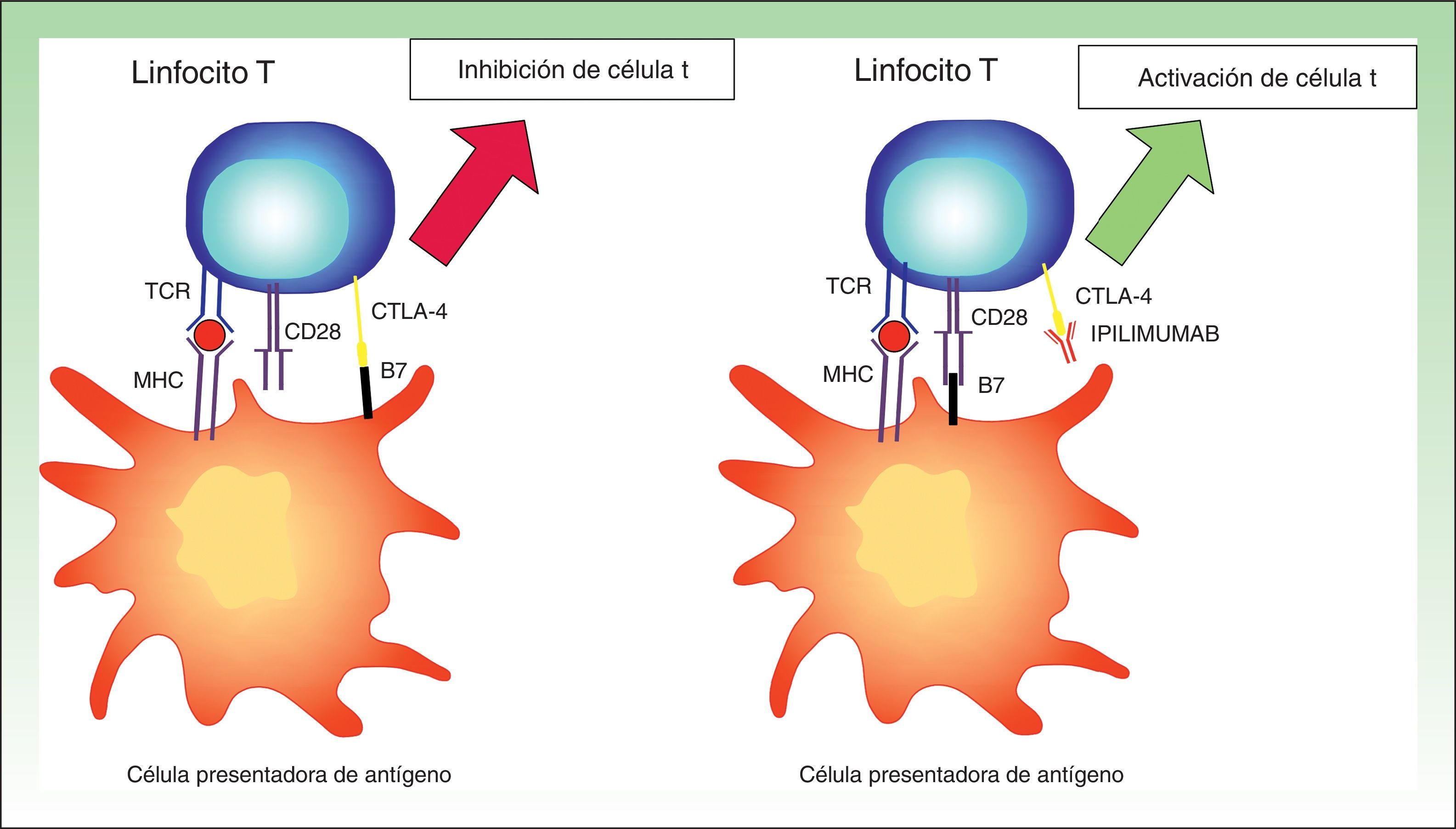
Este hecho se ha podido demostrar con la producción de anticuerpos monoclonales completamente humanos frente a CTLA-4, como el ipilimumab. Al interferir en la unión de CTLA-4 con B7 desaparece el estímulo inhibitorio y la actividad del linfocito se mantiene31. Con esta interacción se mantiene la actividad inmune frente a las células tumorales. Sin embargo, también se producen reacciones de tipo autoinmunitario frente a células no tumorales (fig. 4).
Imagen esquemática sobre la actividad del ipilimumab. A la izquierda inhibición del linfocito T por la unión entre CTLA-1 y B7. A la derecha activación del linfocito T por el bloqueo del CTLA-4 gracias a su unión al anticuerpo monoclonal (ipilimumab).
MHC: complejo mayor de histocompatibilidad, TCR: receptor de célula T.
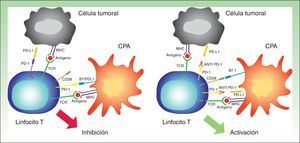
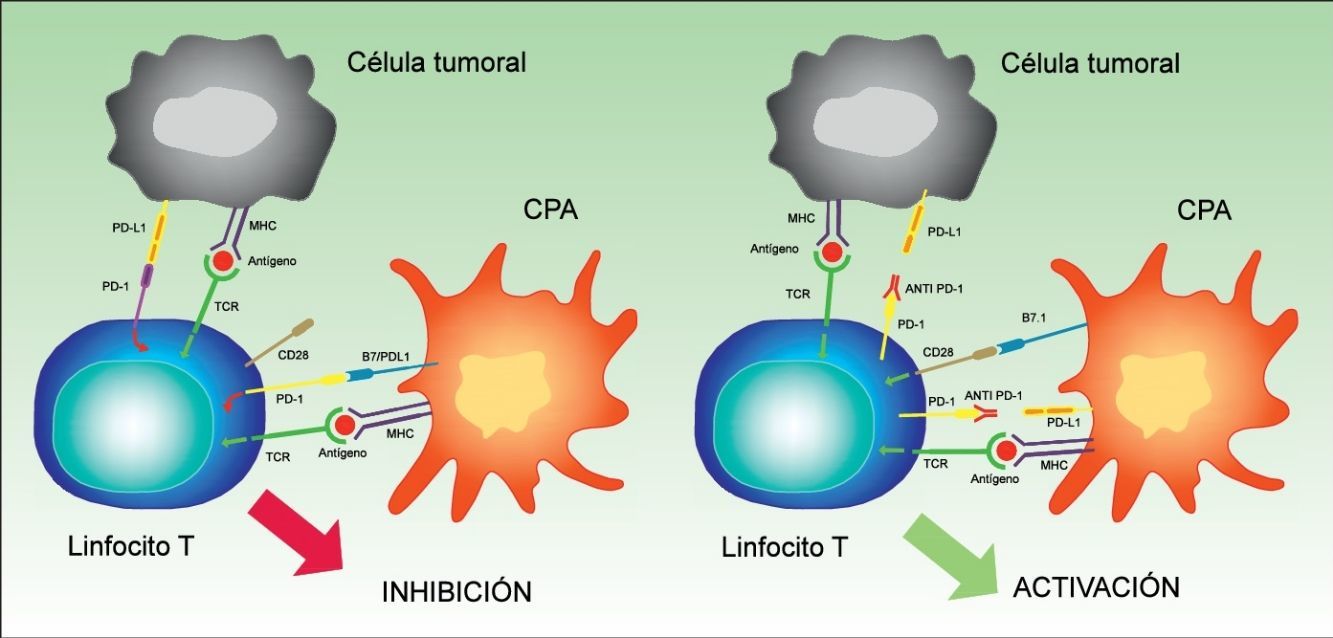
Para poder ejercer su efecto inhibidor, PD1 necesita unirse a sus ligandos. La mayoría de los tejidos, incluyendo células tumorales, expresan PD-L1. Por otro lado, PD-L2 únicamente se expresa en las células dendríticas, macrófagos, mastocitos y linfocitos B32. La expresión de PD-L1 en las células tumorales puede producirse por procesos oncogénicos secundarios a mutaciones activadoras, o por activación mediada por el interferón liberado por las células T específicas que infiltran el tumor33,34. Sin embargo, lo que parece claro es que la presencia previa de linfocitos T que expresan PD-1 es necesaria para inducir la expresión de PD-L1, y esto se conoce como «resistencia inmunitaria adquirida»35 (fig. 5).
Interacción entre PD-1 y PD-L1 que produce inhibición de la célula T (izquierda). Unión de los fármacos anti PD-1 como nivolumab o pembrolizumab al PD-1 de la superficie de los linfocitos que permite la activación del mismo, y por tanto la generación de una respuesta antitumoral (derecha).
CPA: célula presentadora de antígenos; MHC: antígeno mayor de histocompatibilidad; TCR: receptor de la célula T.
La inhibición de esta vía se puede hacer mediante el bloqueo de PD-1, de forma que se inhibe su unión tanto a PD-L1 como a PD-L2, o mediante el bloqueo de PD-L1, que únicamente impide la interacción PD-1 con PD-L1.
Los ratones que carecen de PD-1 y PD-L1 no fallecen de forma temprana (a diferencia de los knocked-out para CTLA-4), sino que desarrollan múltiples enfermedades de origen autoinmune de forma progresiva36,37. Esto explica el abanico de efectos secundarios que se produce en los pacientes tratados con estos agentes.
Virus oncolíticosLa terapia con virus es una nueva herramienta que ha demostrado eficacia frente a múltiples tumores sólidos, entre ellos el melanoma38. Los mejores resultados se han obtenido con el herpes simple tipo 1. Se trata de un virus intensamente oncolítico modificado genéticamente que presenta especificidad para la infección y replicación en las células tumorales, mientras que respeta a las células sanas39.
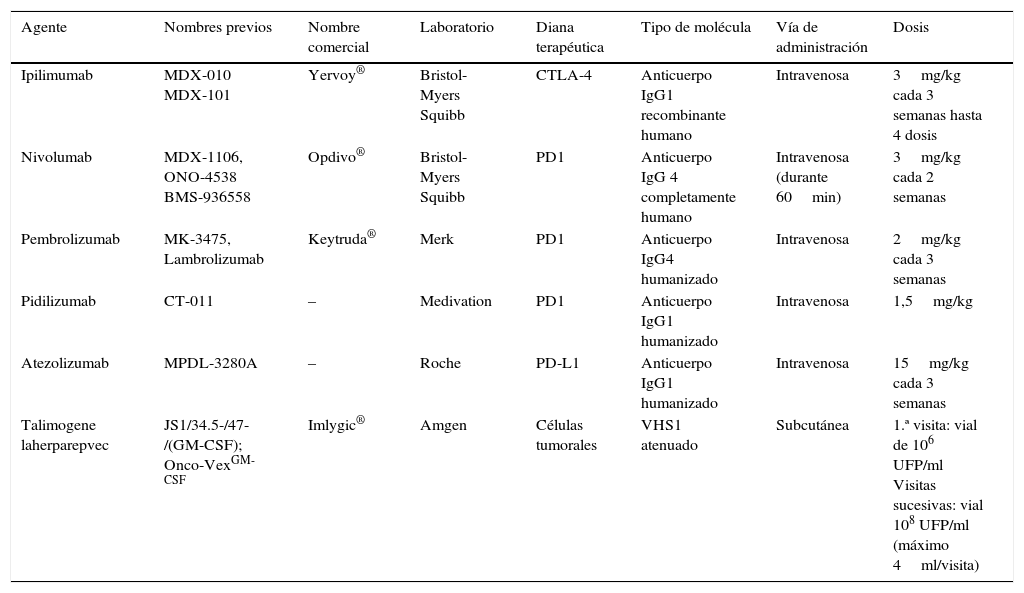
Fármacos inmunomoduladoresAnti-antígeno citotóxico de los linfocitos TIpilimumabEl Ipilimumab fue el primer fármaco inmunomodulador que demostró beneficio en la supervivencia de pacientes con melanoma metastásico31,40. Su uso fue aprobado por la Food and Drug Administration (FDA) en 2011 y pocos meses después por la Agencia Europea del Medicamento41 (tabla 1).
Datos comerciales, características y forma de administración de los fármacos inmunomoduladores disponibles en la actualidad
| Agente | Nombres previos | Nombre comercial | Laboratorio | Diana terapéutica | Tipo de molécula | Vía de administración | Dosis |
|---|---|---|---|---|---|---|---|
| Ipilimumab | MDX-010 MDX-101 | Yervoy® | Bristol-Myers Squibb | CTLA-4 | Anticuerpo IgG1 recombinante humano | Intravenosa | 3mg/kg cada 3 semanas hasta 4 dosis |
| Nivolumab | MDX-1106, ONO-4538 BMS-936558 | Opdivo® | Bristol-Myers Squibb | PD1 | Anticuerpo IgG 4 completamente humano | Intravenosa (durante 60min) | 3mg/kg cada 2 semanas |
| Pembrolizumab | MK-3475, Lambrolizumab | Keytruda® | Merk | PD1 | Anticuerpo IgG4 humanizado | Intravenosa | 2mg/kg cada 3 semanas |
| Pidilizumab | CT-011 | – | Medivation | PD1 | Anticuerpo IgG1 humanizado | Intravenosa | 1,5mg/kg |
| Atezolizumab | MPDL-3280A | – | Roche | PD-L1 | Anticuerpo IgG1 humanizado | Intravenosa | 15mg/kg cada 3 semanas |
| Talimogene laherparepvec | JS1/34.5-/47-/(GM-CSF); Onco-VexGM-CSF | Imlygic® | Amgen | Células tumorales | VHS1 atenuado | Subcutánea | 1.ª visita: vial de 106 UFP/ml Visitas sucesivas: vial 108 UFP/ml (máximo 4ml/visita) |
El estudio comparativo aleatorizado entre el ipilimumab y la dacarbazina demostró una mayor supervivencia global del grupo tratado con el ipilimumab42. La mediana de supervivencia es de 9,5 meses, pero de forma llamativa hasta un 22% de los pacientes sobreviven a largo plazo43.
Por su mecanismo de acción el ipilimumab está asociado a un elevado número de efectos adversos, la mayoría de los cuales son de tipo autoinmune y ocurren aproximadamente en el 60% de los pacientes44. Los más frecuente son: diarrea, colitis, dermatitis, hipofisitis y tiroiditis. Únicamente un 10-15% de estos efectos son de carácter moderado/grave (grado 3 o 4) y suelen resolverse entre 4 y 6 semanas con corticoides u otros inmunosupresores en poco tiempo45 (tabla 2).
Clasificación por grados de los efectos adversos al tratamiento farmacológico según la versión 4.0 de los criterios para la terminología común sobre efectos adversos elaborada por el National Cancer Institute
| Grado | Categoría | Descripción |
|---|---|---|
| I | Leve | Asintomático o síntomas leves. No requiere tratamiento |
| II | Moderado | Sintomático, limita las actividades de la vida diariaa. Requiere tratamiento local o sistémico no invasivo |
| III | Grave | No pone en peligro inmediato la vida del paciente pero limita las actividades básicas de la vida diariab. Requiere hospitalización |
| IV | Muy grave | Efectos adversos que ponen en peligro la vida del paciente. Requiere intervención urgente |
| V | Muerte | Muerte relacionada con la administración del fármaco |
Actividades de la vida diaria: tales como comprar/preparar comida o ropa, usar el teléfono, administrar dinero.
Actividades básicas de la vida diaria: tales como vestirse y desvestirse, alimentarse, aseo personal, deambulación independiente.Fuente: National Cancer Institute45.
Una característica común al uso de inmunomoduladores es la aparición de pseudoprogresión tras la introducción del fármaco. Se trata de un efecto derivado de la activación linfocitaria y la liberación de citoquinas, que producen quimiotaxis de mediadores de la inflamación, edema e incluso necrosis a nivel local, y esto genera un aumento transitorio del volumen de la lesión44. Este efecto es más frecuente en el melanoma que en otros tumores, y es fundamental conocer esta posibilidad para evitar la interrupción del tratamiento en ciertos pacientes en los que inicialmente se observa un aumento del volumen tumoral, pero que posteriormente podrían beneficiarse de la terapia.
Sin embargo, este efecto también limitaría la administración de estos fármacos a pacientes con enfermedad metastásica avanzada en localizaciones de alto riesgo, como son aquellos con metástasis en el sistema nervioso central. Un incremento de volumen tumoral, incluso transitorio, supone un riesgo vital en estos casos.
TremelimumabEs un anticuerpo IgG2 dirigido frente al CTLA-4. A pesar del éxito en las primeras fases, el ensayo en fase iii no demostró diferencias significativas respecto a la quimioterapia, por lo que no está disponible para su uso46.
Anti-PD-1NivolumabNivolumab fue el primer anti-PD1 que demostró buena tolerancia y respuesta significativa en varios pacientes con tumores sólidos47. Fue aprobado para el uso en nuestro país a finales de 2015, y está disponible desde febrero de 2016 para pacientes con melanoma irresecable o metastásico, independientemente de la mutación BRAF. Es un anticuerpo monoclonal que se une con alta afinidad a PD-1 e inhibe la interacción con PD-L1 y PD-L2, aumentando la proliferación y secreción de citoquinas de las células T específicas47,48.
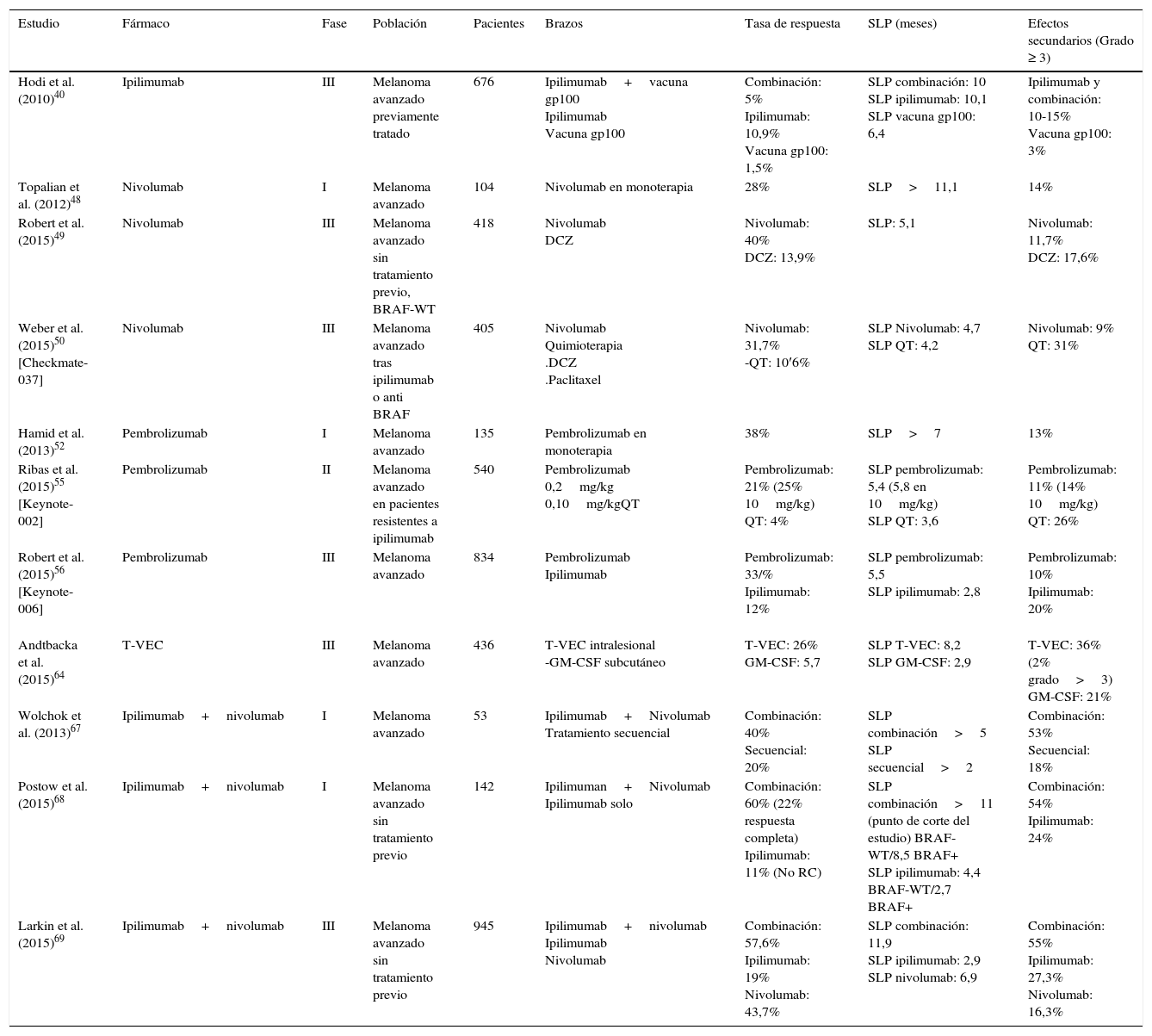
El primer ensayo publicado en fase iii demostró superioridad frente a la quimioterapia, confirmada en los ensayos posteriores48,49 (tabla 3). Las principales toxicidades asociadas al tratamiento son fatiga, diarrea, náuseas, anorexia y fiebre. Prácticamente todos los efectos adversos se resuelven espontáneamente o con la administración de corticoides sistémicos. Por otro lado, entre los efectos secundarios de tipo autoinmune destacan la afectación cutánea (exantema, prurito o vitíligo), gastrointestinal (diarrea o colitis), aumento de las enzimas hepáticas, hipo o hipertiroidismo y pneumonitis51. Por este motivo, aunque la frecuencia de estos efectos es baja, es necesaria una monitorización cuidadosa de estos pacientes y la instauración de tratamiento en los casos necesarios.
Esquema resumen en el que se muestran algunos de los ensayos clínicos más signficativos y los resultados en cuanto a tasa de respuesta, supervivencia y efectos adversos
| Estudio | Fármaco | Fase | Población | Pacientes | Brazos | Tasa de respuesta | SLP (meses) | Efectos secundarios (Grado ≥ 3) |
|---|---|---|---|---|---|---|---|---|
| Hodi et al. (2010)40 | Ipilimumab | III | Melanoma avanzado previamente tratado | 676 | Ipilimumab+vacuna gp100 Ipilimumab Vacuna gp100 | Combinación: 5% Ipilimumab: 10,9% Vacuna gp100: 1,5% | SLP combinación: 10 SLP ipilimumab: 10,1 SLP vacuna gp100: 6,4 | Ipilimumab y combinación: 10-15% Vacuna gp100: 3% |
| Topalian et al. (2012)48 | Nivolumab | I | Melanoma avanzado | 104 | Nivolumab en monoterapia | 28% | SLP>11,1 | 14% |
| Robert et al. (2015)49 | Nivolumab | III | Melanoma avanzado sin tratamiento previo, BRAF-WT | 418 | Nivolumab DCZ | Nivolumab: 40% DCZ: 13,9% | SLP: 5,1 | Nivolumab: 11,7% DCZ: 17,6% |
| Weber et al. (2015)50 [Checkmate-037] | Nivolumab | III | Melanoma avanzado tras ipilimumab o anti BRAF | 405 | Nivolumab Quimioterapia .DCZ .Paclitaxel | Nivolumab: 31,7% -QT: 10′6% | SLP Nivolumab: 4,7 SLP QT: 4,2 | Nivolumab: 9% QT: 31% |
| Hamid et al. (2013)52 | Pembrolizumab | I | Melanoma avanzado | 135 | Pembrolizumab en monoterapia | 38% | SLP>7 | 13% |
| Ribas et al. (2015)55 [Keynote-002] | Pembrolizumab | II | Melanoma avanzado en pacientes resistentes a ipilimumab | 540 | Pembrolizumab 0,2mg/kg 0,10mg/kgQT | Pembrolizumab: 21% (25% 10mg/kg) QT: 4% | SLP pembrolizumab: 5,4 (5,8 en 10mg/kg) SLP QT: 3,6 | Pembrolizumab: 11% (14% 10mg/kg) QT: 26% |
| Robert et al. (2015)56 [Keynote-006] | Pembrolizumab | III | Melanoma avanzado | 834 | Pembrolizumab Ipilimumab | Pembrolizumab: 33/% Ipilimumab: 12% | SLP pembrolizumab: 5,5 SLP ipilimumab: 2,8 | Pembrolizumab: 10% Ipilimumab: 20% |
| Andtbacka et al. (2015)64 | T-VEC | III | Melanoma avanzado | 436 | T-VEC intralesional -GM-CSF subcutáneo | T-VEC: 26% GM-CSF: 5,7 | SLP T-VEC: 8,2 SLP GM-CSF: 2,9 | T-VEC: 36% (2% grado>3) GM-CSF: 21% |
| Wolchok et al. (2013)67 | Ipilimumab+nivolumab | I | Melanoma avanzado | 53 | Ipilimumab+Nivolumab Tratamiento secuencial | Combinación: 40% Secuencial: 20% | SLP combinación>5 SLP secuencial>2 | Combinación: 53% Secuencial: 18% |
| Postow et al. (2015)68 | Ipilimumab+nivolumab | I | Melanoma avanzado sin tratamiento previo | 142 | Ipilimuman+Nivolumab Ipilimumab solo | Combinación: 60% (22% respuesta completa) Ipilimumab: 11% (No RC) | SLP combinación>11 (punto de corte del estudio) BRAF-WT/8,5 BRAF+ SLP ipilimumab: 4,4 BRAF-WT/2,7 BRAF+ | Combinación: 54% Ipilimumab: 24% |
| Larkin et al. (2015)69 | Ipilimumab+nivolumab | III | Melanoma avanzado sin tratamiento previo | 945 | Ipilimumab+nivolumab Ipilimumab Nivolumab | Combinación: 57,6% Ipilimumab: 19% Nivolumab: 43,7% | SLP combinación: 11,9 SLP ipilimumab: 2,9 SLP nivolumab: 6,9 | Combinación: 55% Ipilimumab: 27,3% Nivolumab: 16,3% |
BRAF+: pacientes con mutación en BRAF; BRAF-WT: pacientes sin mutación en BRAF (wild type); DCZ: dacarbazina; QT: quimioterapia; RC: Respuesta completa; SLP: supervivencia libre de progresión; T-VEC: talimogene laherparepvec.
Bajo los autores del estudio, entre corchetes, el nombre de identificación del estudio.
Es el anticuerpo monoclonal con la mayor afinidad por PD1 de los fármacos disponibles. Los resultados de los estudios de fase i y fase ii favorecieron la aprobación acelerada del fármaco en pacientes con melanoma avanzado sin respuesta a ipilimumab52,53. Tanto la tasa de respuesta al fármaco como la supervivencia son superiores a las obtenidas con quimioterapia y con ipilimumab54–56. Los efectos secundarios más frecuentes son astenia, erupción cutánea, prurito y diarrea52,55 (tabla 3).
Desde enero de 2016 tanto nivolumab como pembrolizumab están aprobados por la Agencia Española del Medicamento para el uso en pacientes con melanoma avanzado (irresecable o metastásico)57,58.
El pidilizumab, otro anti PD1, demostró resultados inferiores a los obtenidos con nivolumab o pembrolizumab, por lo que no se encuentra aprobado para esta indicación59.
Anti PD-L1AtezolizumabLos primeros resultados del tratamiento de pacientes con este anticuerpo anti PD-L1 han demostrado respuestas hasta en el 29% de los pacientes con melanoma. Además, en combinación con vemurafenib ha demostrado tasas de respuesta objetiva (completas y parciales) del 76%60.
BMS-936559Es un anticuerpo tipo IgG4 completamente humano dirigido frente a PD-L1. En los estudios iniciales ha demostrado tasas de respuesta superiores al 17% y con un porcentaje bajo de efectos adversos (9%)61.
MED14736Anticuerpo IgG1 humanizado frente a PD-L1. Actualmente se encuentra en estudio combinado con dabrafenib+trametinib. Los datos provisionales muestran respuestas superiores al 65% con aparición de efectos adversos graves en un 35-40% de los pacientes62.
Virus oncolíticosTalimogene laherparepvecDesde finales de 2015 está aprobado el talimogene laherparepvec para el tratamiento de pacientes con melanoma irresecable y metástasis regionales o a distancia (estadios IIIB, IIIC y IVM1a) sin afectación visceral63. Es un VHS-1 atenuado, producido mediante recombinación génica, diseñado para replicarse de forma específica en el interior de las células tumorales y para producir factor estimulante de colonias de granulocitos y macrófagos humano (GM-CSF), y de esta manera estimula la respuesta antitumoral sistémica.
La administración del fármaco es subcutánea, y debe realizarse directamente sobre las lesiones cutáneas de melanoma. En caso de ser múltiples deben tratarse primero las de mayor tamaño.
El tratamiento con talimogene laherparepvec ha demostrado tasas de respuesta del 26%, con un perfil de efectos adversos favorable y aumento de la supervivencia a largo plazo64. Además, en comparación con el ipilimumab y el vemurafenib, la supervivencia global ha demostrado ser comparable o ligeramente superior con este fármaco, especialmente en los pacientes sin metástasis viscerales65.
Combinación de fármacosCTLA-4 y PD-1 ejercen una función inhibitoria a través de vías diferentes, y por tanto el bloqueo de ambos favorecería la destrucción tumoral por el sistema inmune. Este hecho fue comprobado inicialmente en modelos animales66 y posteriormente en humanos. Hasta el momento se han realizado ensayos controlados combinando nivolumab e ipilimumab, con una tasa de respuesta superior a la que se consigue con monoterapia67–69. Sin embargo, la toxicidad grave aparece en más de la mitad de los pacientes tratados. Los efectos severos más frecuentes son colitis, diarrea y elevación de enzimas hepáticas, que en la mayoría de los casos requieren el uso de glucocorticoides sistémicos68,69.
La combinación de nivolumab e ipilimumab se encuentra aprobada desde septiembre de 2015 por la FDA y pendiente de aprobación por la Agencia Europea del Medicamento.
Indicadores de respuestaTras el éxito de las terapias inmunomoduladoras, la investigación se ha dirigido a la identificación de los posibles marcadores que permitan identificar a los pacientes con mayor probabilidad de respuesta al fármaco.
La expresión de PD-L1 en las muestras tumorales previas al tratamiento es la que se ha asociado de forma más clara, con un incremento en la tasa de respuesta a los anti PD-1 y anti PD-L134,70,71. Por el contrario, en el tratamiento combinado con ipilimumab y nivolumab no se ha observado relación entre la expresión de PD-L1 y la tasa de respuesta68.
Por otro lado, la expresión de PD-L1 tiene varios inconvenientes para poder considerarse un biomarcador adecuado. Se trata de un marcador cuya expresión es muy variable, incluso en piezas de un mismo paciente. Además, aunque se observa mayor beneficio clínico en los pacientes PD-L1+, también existe un número considerable de pacientes PD-L1- con respuesta a los tratamientos60,70.
Otro efecto de confusión es que la liberación de interferón por las células CD8+, que infiltran el margen y el parénquima tumoral, induce la expresión de PD-L1 en las células tumorales, lo que se conoce como resistencia inmune adaptativa. Por ello, la expresión de PD-L1 es un marcador indirecto de activación de linfocitos T antígeno específicos. Los tumores con mayor cantidad de PD-L1 y PD-1 son los que presentan una mejor respuesta, pero es necesaria la presencia previa de linfocitos CD8+ específicos72.
De forma general, para predecir la respuesta a cualquier inmunomodulador, el mejor indicador disponible actualmente sigue siendo la presencia de CD8+ en el margen del tumor72.
Perspectivas futurasCombinaciones futurasActualmente existen múltiples ensayos en marcha que combinan los inmunomoduladores entre sí y con otras terapias para el uso en pacientes con melanoma avanzado.
Tanto CTLA-4 como PD-1 inhiben la respuesta inmune por diferentes vías, y por tanto es fundamental considerar su utilización de una forma sinérgica. En cuanto a las terapias diana o tras el tratamiento con virus oncolíticos, los antígenos que se liberan como resultado de la muerte de las células tumorales son presentados a los linfocitos por las células presentadoras de antígenos, además de determinadas citocinas y quimiocinas. Todo esto induce una respuesta inmune antitumoral, y en este sentido los fármacos anti BRAF, los virus oncolíticos o las vacunas peptídicas podrían favorecer la respuesta a los inmunomoduladores73.
Terapia adyuvanteEl tratamiento preventivo de los pacientes con mayor riesgo metastásico es uno de los retos fundamentales en el manejo del melanoma. Hasta este momento la cirugía, la biopsia de ganglio centinela y el interferón α son los métodos empleados para controlar los tumores localmente avanzados. Sin embargo, la posibilidad de tratar eficazmente a estos pacientes con otros agentes podría cambiar el progreso de esta enfermedad y el manejo de la misma por los dermatólogos.
En octubre de 2015 la FDA, gracias a los resultados de un ensayo, aprobó el uso de Ipilimumab como tratamiento adyuvante en pacientes con melanoma localmente avanzado. Es aplicable a pacientes con melanoma en estadio iii, con metástasis ganglionares >1mm y resección ganglionar completa74. Los datos a 5 años de este mismo estudio demuestran una tasa del 40,8% de pacientes libres de recurrencia a los 5 años frente a un 30,3% en el grupo tratado con placebo75. Sin embargo, hasta un 45% de los pacientes tratados presentaban efectos adversos de grado 3 o 4, aunque con un manejo adecuado se reduce notablemente la gravedad de los mismos. Los efectos adversos más frecuentes con esta terapia son la diarrea, la colitis, los efectos endocrinológicos (hipofisistis con hipopituitarismo, hipo o hipertiroidismo, disfunción adrenal), vitíligo, exantemas, prurito y fatiga.
Además del ipilimumab, en este momento existen múltiples estudios en marcha que emplean fármacos inmunomoduladores de forma adyuvante en tumores de alto riesgo tras la resección completa, y cuyos resultados se publicarán en los próximos años76.
ConclusiónDesde la introducción de los tratamientos inmunoterapéuticos, hace apenas un lustro, el panorama del tratamiento del melanoma ha sufrido una revolución, consiguiéndose cifras de supervivencia muy superiores a las que se alcanzaban con los tratamientos anteriores.
Sin embargo, el descubrimiento de nuevas terapias también trae consigo la necesidad de realizar nuevos estudios que permitan conocer mejor el mecanismo de acción de estos fármacos. La investigación en este campo debe ir dirigida a seleccionar qué pacientes son los más adecuados para el tratamiento y con qué fármacos o combinación de los mismos se espera una mayor respuesta. Además, la combinación con otros tratamientos, como las terapias diana o los virus oncolíticos, podría mejorar la eficacia del tratamiento.
En definitiva, el estímulo de la respuesta inmune es un elemento fundamental en el tratamiento frente al melanoma, y probablemente formará parte de todos los esquemas terapéuticos que vayan surgiendo frente a este tumor.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Queremos agradecer a la Dra. Isabel Pinazo y al Dr. Carlos Monteagudo su colaboración en la realización de esta revisión.



![Imagen de regresión en un melanoma. A. Imagen clínica en la que se aprecia una zona central con pérdida de pigmento. B. Dermatoscopia de la lesión que muestra un patrón multicomponente con un área blanca central. C y D. Imágenes histológicas donde se aprecia infiltrado linfocitario denso en la dermis sin alteración epidérmica, melanofagia y fibrosis de la dermis (hematoxilina-eosina, C [10x] y D [20x], aumentos de microscopio óptico). Imagen de regresión en un melanoma. A. Imagen clínica en la que se aprecia una zona central con pérdida de pigmento. B. Dermatoscopia de la lesión que muestra un patrón multicomponente con un área blanca central. C y D. Imágenes histológicas donde se aprecia infiltrado linfocitario denso en la dermis sin alteración epidérmica, melanofagia y fibrosis de la dermis (hematoxilina-eosina, C [10x] y D [20x], aumentos de microscopio óptico).](https://static.elsevier.es/multimedia/00017310/0000010800000008/v1_201710010019/S0001731017301175/v1_201710010019/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w9/t1/zx4Q/XH5Tma1a/6fSs=)