Valorar la efectividad y seguridad del propranolol oral (PO) para tratar hemangiomas infantiles (HI).
Material y métodosEstudio prospectivo de los HI tratados con PO entre octubre de 2008 y marzo de 2011. Fueron candidatos a tratamiento los HI en fase proliferativa con rápido crecimiento, compromiso de alguna estructura vital o ulceración y para evitar problemas funcionales o estéticos tras la fase proliferativa. Los pacientes se trataron con 2mg/kg/día de PO, y fueron controlados ambulatoriamente. Se valoró la respuesta terapéutica mediante una escala en la que se consideró la reducción del volumen, aclaramiento del color y mejoría de los síntomas del HI, además del grado de satisfacción paterna. Se registró el momento de respuesta inicial y máxima, efectos secundarios y secuelas.
ResultadosSe trataron 20 casos de HI (17 niñas y 3 niños). Las localizaciones predominantes fueron: periorbitaria (20%), nariz (15%), cuello/nuca (15%) y tronco (15%). La mayoría HI fueron focales y en fase proliferativa (90%). El tratamiento se inició entre 2 y 19 meses, siendo el principal motivo para empezarlo el rápido crecimiento (50%). El inicio de respuesta se observó en el 70% de los casos a los 5 días y en solo 2 tardíamente (más de un mes). El pico máximo de respuesta se obtuvo a los 3 meses. En el 55% de casos la respuesta fue excelente, buena en el 35%, mínima en el 10% y en ninguno nula. Fueron factores predictores de respuesta el HI focal, la fase proliferativa, la localización periorbitaria y la ulceración. No hemos constatado efectos adversos importantes.
ConclusiónHemos comprobado la efectividad clínica del PO en la reducción de los HI, pero no su completa desaparición al concluir el tratamiento, persistiendo parte de su volumen, color, telangiectasias o cicatrices. El PO ha resultado seguro bajo control ambulatorio.
To assess the safety and effectiveness of oral propranolol (OP) in the treatment of infantile hemangiomas.
Material and methodWe conducted a prospective study of infantile hemangiomas (IHs) treated with oral propranolol between October 2008 and March 2011. We included fast-growing IHs in the proliferative phase, IHs affecting vital structures, ulcerated IHs, and IHs that could cause functional or aesthetic problems after the proliferative phase. The patients received oral propranolol 2mg/kg/d and were monitored on an outpatient basis. Response to treatment was assessed by volume reduction, lightening of color, improvement of symptoms, and parent satisfaction. Time of initial and peak response, as well as side effects and sequelae, were recorded.
ResultsWe analyzed 20 IHs, corresponding to 17 girls and 3 boys. The main sites of involvement were around the eyes (20%), the nose (15%), the neck (15%), and the trunk (15%). Ninety percent of the hemangiomas were focal and in the proliferative phase. Treatment was started between the ages of 2 and 19 months and the main reason for starting treatment was rapid growth (50% of cases). Initial response was observed in 70% of cases and only in 2 of them it took over a month. Peak response occurred at 3 months. All the IHs responded to treatment; response was excellent in 55% of cases, good in 35%, and minimal in 10%. The following factors were predictive of response: focal IH, proliferative phase, periorbital location, and ulceration. No serious side effects were observed.
ConclusionOral propranolol was clinically effective in reducing the volume and color of infantile hemangiomas, although the reduction was not complete and telangiectasia and scarring persisted after treatment. Oral propranolol also proved to be safe for use in outpatients.
El tratamiento habitual de los hemangiomas infantiles (HI) de crecimiento rápido o que producen problemas funcionales o estéticos importantes ha sido hasta hace poco la administración de corticoides orales a elevadas dosis, a fin de inducir la fase de regresión en los mismos1. Tras la publicación inicial que demostró el efecto beneficioso del propranolol en el tratamiento de estos HI2, se ha extendido el uso de este fármaco y se han generado numerosas publicaciones de revisión o de presentación de casos aislados, series3–13, estudios multicéntricos14,15 o estudios comparativos con corticosteroides orales16. Todo ello para intentar poner luz en el debate existente en cuanto a los posibles riesgos y beneficios asociados a su uso y poder generar evidencia científica que permita establecer las indicaciones, los controles a seguir y, en definitiva, establecer su perfil de efectividad y seguridad en esta indicación.
Aunque el propranolol es un fármaco bien conocido y usado en cardiología infantil para el tratamiento de distintas cardiopatías, su posible nueva indicación en el manejo de los HI abre en estos pacientes una nueva perspectiva de tratamiento, en que las experiencias obtenidas entre todos pueden resultar de gran utilidad para optimizar su manejo con garantías para los pacientes. Por este motivo, presentamos este trabajo realizado prospectivamente en 20 casos de HI, con el que aportamos los datos obtenidos en efectividad y seguridad en la práctica clínica en régimen de control ambulatorio.
Material y métodoEntre octubre de 2008 y marzo de 2011 se realizó un estudio prospectivo de todos los casos diagnosticados de HI, que fueron atendidos en la consulta monográfica de dermatología pediátrica de nuestro hospital. La evolución de los pacientes se siguió hasta agosto de 2011. En cada uno de ellos se registró el tipo de hemangioma, su fase evolutiva, localización, tamaño, color, distribución, presencia o no de ulceración y sintomatología asociada. Los HI de cabeza de localización segmentaria o situados en la línea media fueron sometidos a pruebas de imagen (RMN, angioRMN o ecografía), exploración cardiológica y oftalmológica; los HI de localización periorbitaria fueron sometidos a examen oftalmológico y las lesiones focales, profundas o mixtas, de gran tamaño (>5cm) fueron estudiadas mediante eco-doppler. A los pacientes con HI múltiples (5 o más) se les realizó además una ecografía hepática. En los HI múltiples y en los de gran tamaño se realizó una determinación de TSH.
Selección de pacientesSe consideraron candidatos a tratamiento con propranolol los HI que estaban en fase proliferativa en los que existía alguna complicación, como compromiso de alguna estructura vital, ulceración o sangrado y los HI sin complicaciones, pero cuyo desarrollo rápido hacía previsible un posible problema de tipo funcional o estético. Asimismo, se consideraron para tratamiento aquellos HI en los que habiendo finalizado la fase proliferativa se planteaba un posible beneficio, ya fuese por su localización o para reducir el volumen de la tumoración antes de la cirugía. Fueron criterios de exclusión los pacientes con síndrome de PHACE, con cardiopatías que requirieran tratamiento o con antecedentes de asma o hipoglucemia. Tras informar a los padres de la opción terapéutica, si estos estaban de acuerdo, firmaban un documento de consentimiento informado.
Evaluación previa al tratamientoTodos los niños fueron sometidos a una evaluación cardiológica que incluyó un electrocardiograma y un ecocardiograma, además de control de peso, constantes (tensión arterial [TA], frecuencia cardíaca [FC]) y analítica completa.
Preparación del fármacoSe realizó en el Servicio de Farmacia del hospital mediante una formulación magistral, diluyendo el propranolol puro en un jarabe con sacarosa según farmacopea. La solución se renovaba mensualmente a fin de evitar el uso de aditivos y estabilizantes, y su concentración se iba incrementando para adaptarse al peso del paciente, con el fin de tener que administrar menos volumen de la solución en cada toma. La dosis de fármaco que se utilizó en todos los casos fue de 2mg/kg/día repartida en 3 tomas y administrada vía oral mediante una jeringa.
Cuando se decidía finalizar el tratamiento se pautaba una disminución progresiva de la dosis que se reducía a 1mg/kg/día durante 15 días y a 0,5mg/kg/día otros 15 días.
Monitorización del tratamientoLos pacientes fueron controlados a las 5horas de la primera dosis, al quinto día, cada 15 días durante el primer mes y posteriormente cada mes. Antes de cada revisión se controlaba la TA, la FC, la glucemia y el peso en el hospital de día de pediatría. En cada consulta de revisión se registraban en una gráfica las anteriores cifras, que eran comparadas con los percentiles de las gráficas estándar ajustadas por edad y sexo y los parámetros de anteriores controles. Se anotaban los cambios de color, temperatura, tamaño o consistencia observados por los padres, así como si referían algún acontecimiento adverso. Posteriormente se exploraba al paciente, teniendo en cuenta las modificaciones en el tamaño, color, consistencia o características funcionales relacionadas con el HI. En cada visita se tomaban imágenes fotográficas de control. Se registró el momento de inicio de la respuesta terapéutica y el momento en que se producía la respuesta máxima, a partir de la cual ya no se observaba ninguna modificación en el hemangioma. Al finalizar el tratamiento se anotaba si existía alguna secuela y de qué tipo.
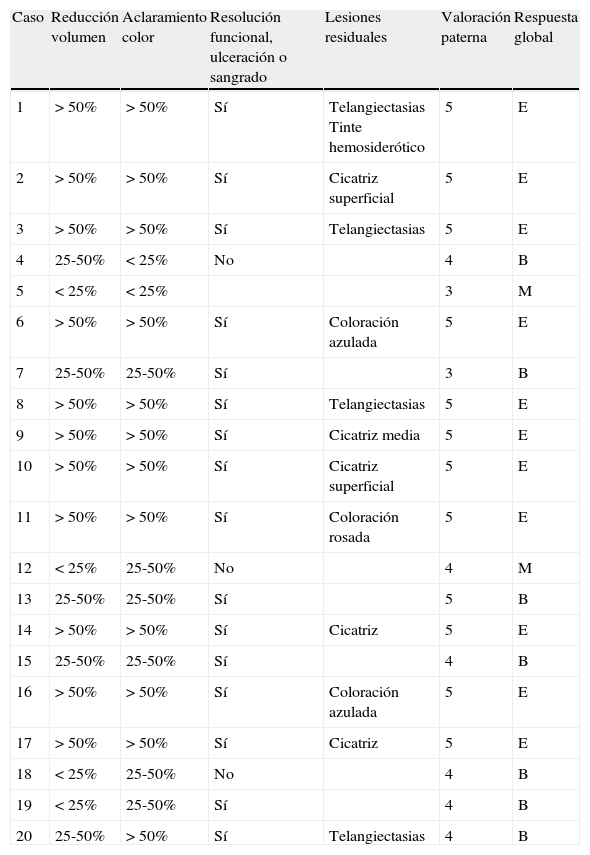
Valoración global de efectividadLa respuesta terapéutica al propranolol se estableció en 4 categorías como excelente, buena, mínima o nula. Esta evaluación era efectuada por un dermatólogo y un pediatra que debían de tener una concordancia del 100% en la valoración, y asimismo se tenía en cuenta el componente de satisfacción manifestado por los padres. La evaluación se efectuaba en cada revisión. Se consideraron 4 categorías de respuesta que debían cumplir todos los siguientes requisitos. Se consideró una respuesta excelente, cuando existía: a) una reducción estimada de más del 50% de volumen del HI; b) un 50% de aclaramiento en su color; c) una recuperación del déficit funcional, sangrado o ulceración; d) mínimas secuelas (eritema, telangiectasias o pequeña cicatriz); y e) una respuesta 4 a 5 en el grado de satisfacción manifestado por los padres (en una escala de 0 a 5, en que 0 era insatisfacción total y 5 satisfacción máxima). Se consideró una respuesta buena si: a) la reducción del volumen era entre el 25 y el 50%; b) el aclaramiento del color era entre el 25 y el 50%; c) existía una recuperación del déficit funcional, ulceración o sangrado; d) había secuelas mínimas o evidentes; y e) un grado de satisfacción paterna entre 3 y 4. Se consideró una respuesta mínima cuando se consiguió una ausencia de progresión del hemangioma o una reducción menor al 25%, o una falta de recuperación funcional o de la ulceración o sangrado y un grado de satisfacción paterna menor de 3, mientras que se consideró una respuesta nula si el HI progresaba en su crecimiento o aparecían efectos adversos importantes que obligaran a suspender la medicación definitivamente (tabla 1). La valoración global de efectividad expuesta en la tabla 1 hace referencia a la realizada al finalizar el tratamiento (en los casos que lo han finalizado) o en la última revisión (en los casos que continúan con él).
Valoración global de eficacia de los hemangiomas infantiles tratados con propranolol. Se ha considerado la respuesta como excelente (E), buena (B), mínima (M) o nula (N)
| Caso | Reducción volumen | Aclaramiento color | Resolución funcional, ulceración o sangrado | Lesiones residuales | Valoración paterna | Respuesta global |
| 1 | >50% | >50% | Sí | Telangiectasias Tinte hemosiderótico | 5 | E |
| 2 | >50% | >50% | Sí | Cicatriz superficial | 5 | E |
| 3 | >50% | >50% | Sí | Telangiectasias | 5 | E |
| 4 | 25-50% | <25% | No | 4 | B | |
| 5 | <25% | <25% | 3 | M | ||
| 6 | >50% | >50% | Sí | Coloración azulada | 5 | E |
| 7 | 25-50% | 25-50% | Sí | 3 | B | |
| 8 | >50% | >50% | Sí | Telangiectasias | 5 | E |
| 9 | >50% | >50% | Sí | Cicatriz media | 5 | E |
| 10 | >50% | >50% | Sí | Cicatriz superficial | 5 | E |
| 11 | >50% | >50% | Sí | Coloración rosada | 5 | E |
| 12 | <25% | 25-50% | No | 4 | M | |
| 13 | 25-50% | 25-50% | Sí | 5 | B | |
| 14 | >50% | >50% | Sí | Cicatriz | 5 | E |
| 15 | 25-50% | 25-50% | Sí | 4 | B | |
| 16 | >50% | >50% | Sí | Coloración azulada | 5 | E |
| 17 | >50% | >50% | Sí | Cicatriz | 5 | E |
| 18 | <25% | 25-50% | No | 4 | B | |
| 19 | <25% | 25-50% | Sí | 4 | B | |
| 20 | 25-50% | >50% | Sí | Telangiectasias | 4 | B |
Las variables cualitativas se han expresado en frecuencia y porcentaje, mientras que las cuantitativas en media y desviación estándar. Para contrastar si las variables cuantitativas siguen una distribución normal se ha aplicado el test Kolmogorov-Smirnov. Para comparar las variables cualitativas entre sí se ha utilizado el test de la Chi cuadrado y para comparar variables cualitativas con variables cuantitativas el test de la «t» de Student con la corrección de Levene. El nivel de significación estadística se estableció con una p≤0,05. Todos los datos han sido recogidos y procesados mediante el paquete estadístico SPSS versión 17.0.
ResultadosDatos generales del estudioEn el período del estudio fueron atendidos un total de 45 pacientes con HI. A 23 de ellos se les ofreció el propranolol oral como opción terapeútica, pero en 3 casos los padres rechazaron dicho tratamiento. Se trataron un total de 20 niños (17 niñas y 3 niños), lo que supone un 44% del total de niños con HI atendidos en dicho período. Las características detalladas de la población estudiada, así como los resultados generales del estudio se muestran en las tablas 2 y 3 (figs. 1–5).
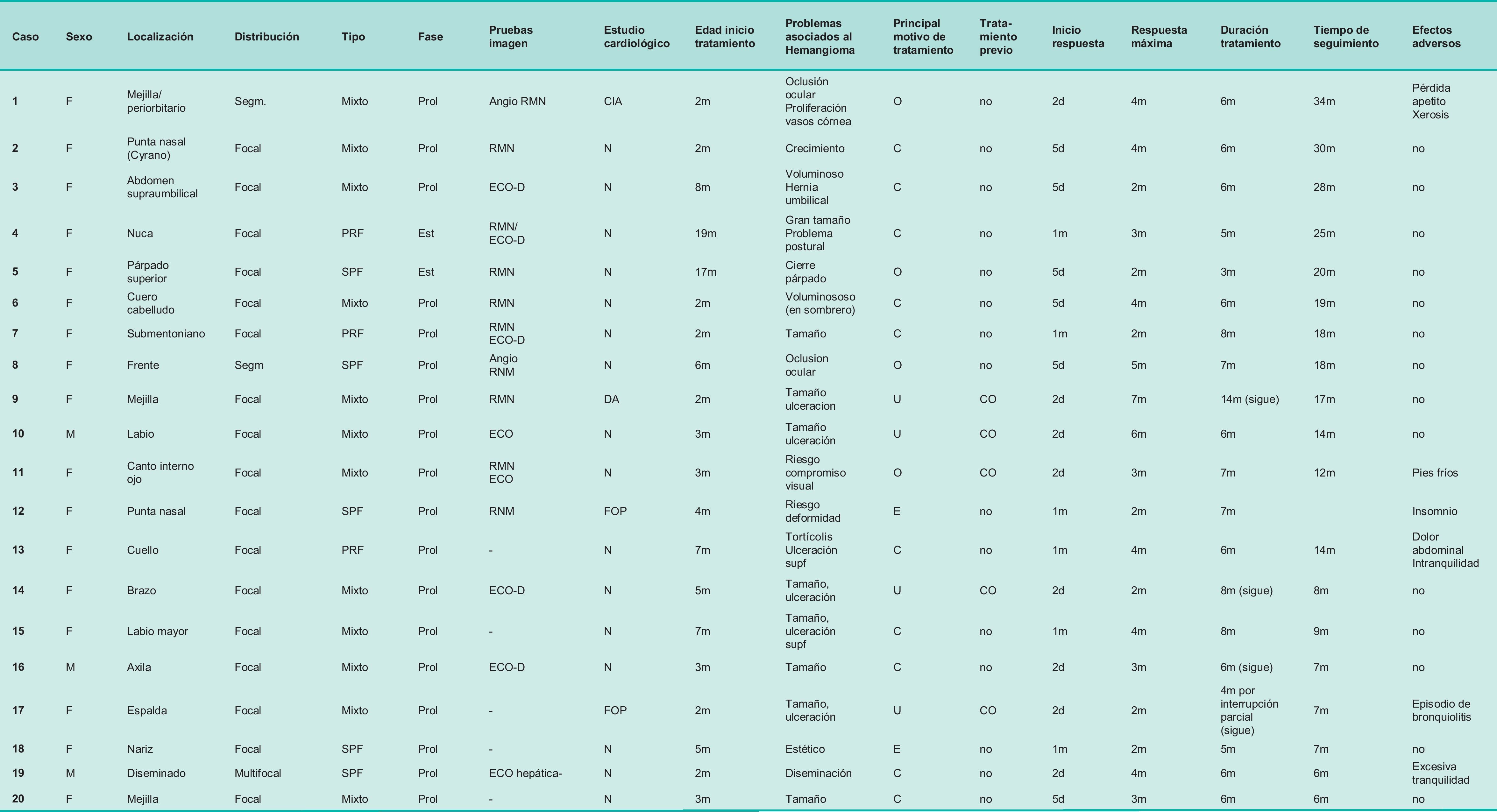
Características detalladas de los hemangiomas infantiles tratados con propranolol
C: crecimiento; CIA: comunicación interauricular; CO: corticosteroides orales; d: días; DA: ductus arterioso; E: riesgo deformidades o estético; ECO: ecografía; ECO_D: ecodoppler; Est: estabilización; F: femenino; FOP: foramen oval permeable; M: masculino; m: meses; N: normal; O: cierre ocular; PRF:profundo; Prol: proliferativa; RMN: resonancia magnética nuclear; Segm: segmentario; SPF: superficial; U: ulceración.
Datos generales obtenidos en la población estudiada
| Características | % (n) |
| Sexo | |
| Niña | 85 (17) |
| Niño | 15 (3) |
| Media de edad | 5,2 meses |
| Rango de edad | De 2 a 19 meses |
| Edad de inicio del tratamiento | |
| <6 meses | 75 (15) |
| >6 meses | 25 (5) |
| Distribución del hemangioma | |
| Segmentario | 10 (2) |
| Focal | 85 (17) |
| Multifocal | 5 (1) |
| Tipo de hemangioma | |
| Superficial | 25 (5) |
| Mixto | 65 (14) |
| Profundo | 5 (1) |
| Fase | |
| Proliferativa | 90 (18) |
| Estabilización | 10 (2) |
| Tratamientos previos | |
| Corticoides orales | 25 (5) |
| Localización | |
| Área periorbitaria | 20 (4) |
| Nariz | 15 (3) |
| Tronco | 15 (3) |
| Cuello-nuca | 15 (3) |
| Otros | 35 (7) |
| Motivo de tratamiento | |
| Crecimiento rápido | 50 (10) |
| Ulceración | 20 (4) |
| Compromiso apertura ocular | 20 (4) |
| Evitar secuelas o deformidades | 10 (2) |
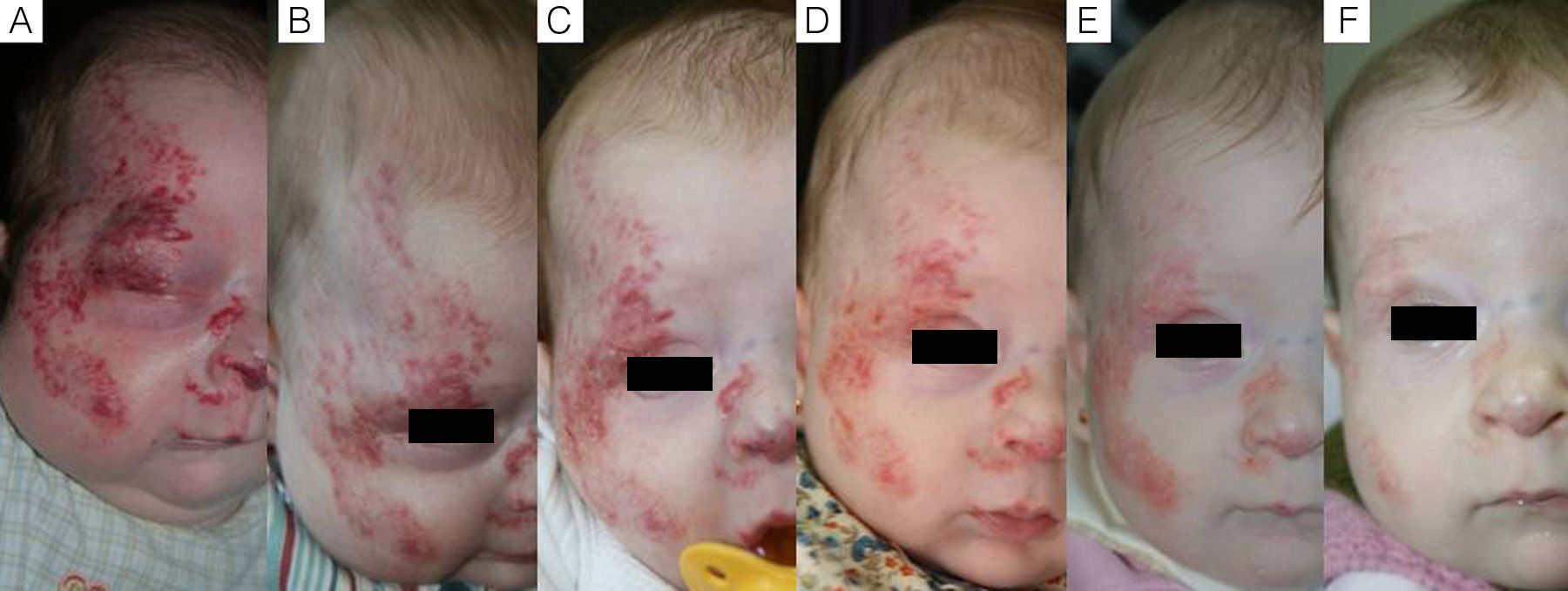
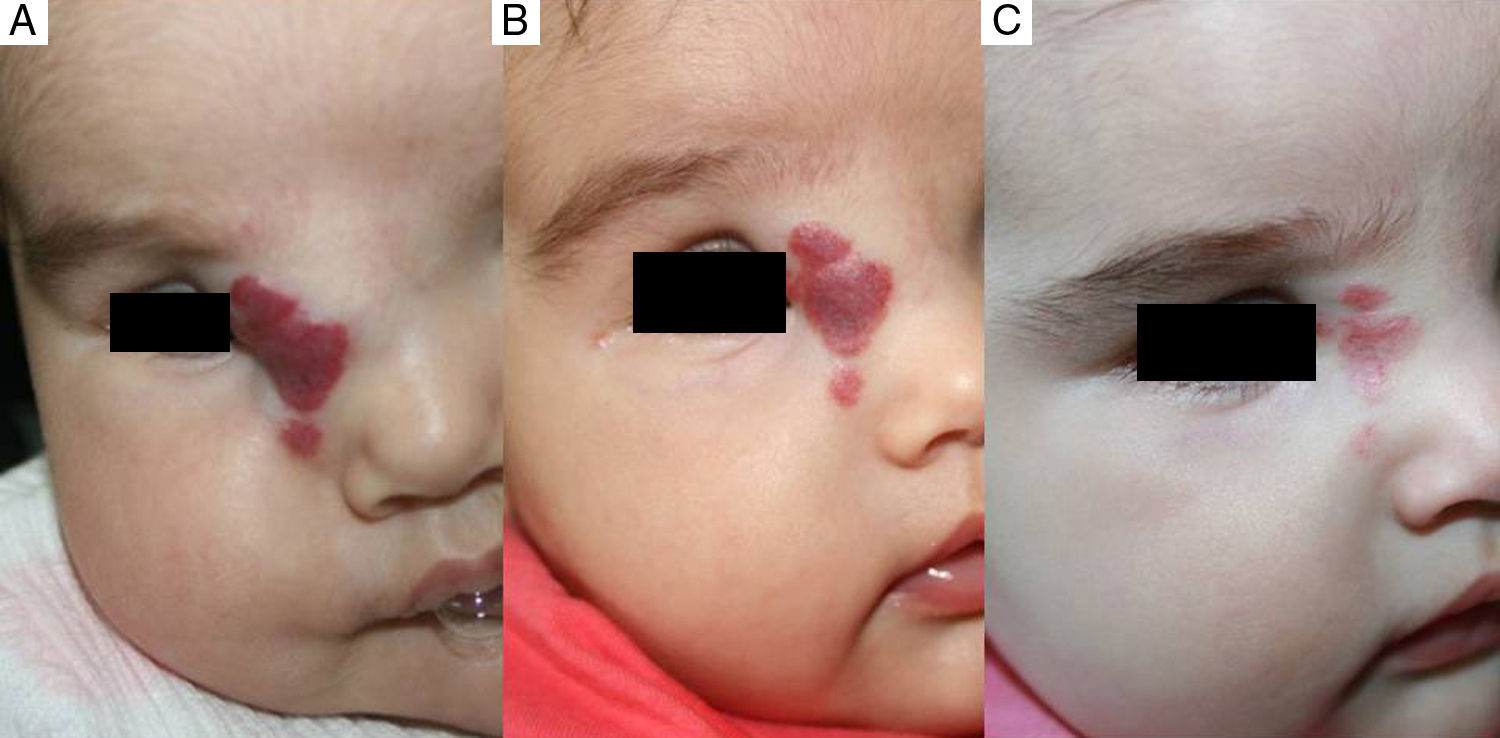
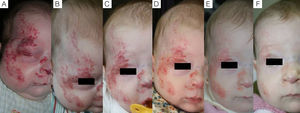
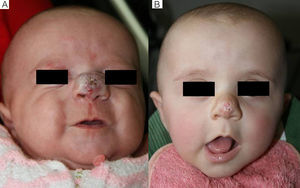
Caso 1. A. Hemangioma segmentario facial con oclusión ocular, antes de iniciar el tratamiento. B. A los 5 días se aprecia inicio de la apertura ocular. C. A los 12 días apertura casi completa y aclaramiento. D. A los 3 meses de tratamiento. E. A los 6 meses. F. A los 11 meses, un mes después de finalizar el tratamiento.
Atendiendo a los criterios anteriormente expuestos para la valoración de la eficacia del tratamiento, constatamos un 55% de casos con excelente respuesta, un 35% con buena respuesta y un 10% con respuesta mínima. En ningún caso se calificó la respuesta global a propranolol como nula (tabla 1).
Factores predictores de respuestaNo se han encontrado diferencias estadísticamente significativas en cuanto a la respuesta global al tratamiento con ninguno de los factores estudiados (sexo, tipo de HI o localización), aunque resulta destacable el porcentaje de respuesta excelente obtenido para los casos de HI periorbitarios (75%). También destacamos, aun sin significación estadística, que de todas las calificaciones designadas como respuesta excelente un 80% eran hemangiomas focales y el 100% eran de tipo superficial o mixto y se encontraban en fase proliferativa. Igualmente sin obtener significación estadística, resulta llamativo que el 80% de los resultados excelentes se obtuvieron en pacientes en los que se inició el tratamiento antes de los 6 meses. En todos los casos en que el motivo principal de tratamiento fue la ulceración se obtuvo una respuesta excelente o buena, y en aquellos que se trataron por rápido crecimiento un 55,6% fueron calificados como respuesta buena y un 33,3% como excelente. Un 55% de pacientes con respuesta excelente habían sido previamente tratados.
Al comparar diversos factores entre sí destacamos, aunque sin significación estadística, que el 80% de los pacientes menores de 6 meses respondieron en los 2-3 primeros días, y que todos los que presentaron una respuesta máxima a los 2 meses son asimismo menores de dicha edad. La rapidez en el inicio de respuesta se observó en el 75% de los HI periorbitarios y en el 100% de los faciales. Por el contrario, el 66,7% de todos los HI nasales inicaron la respuesta al tratamiento de forma más tardía (a los 20-35 días). Los HI superficiales y los que se encontraban en fase proliferativa también respondieron precozmente (92,9% ambos).
DiscusiónDesde la publicación del artículo de Leauté-Labrezze et al. en el año 20082 se han realizado múltiples estudios para constatar la efectividad del tratamiento oral con propranolol en los hemangiomas infantiles, aunque pocas series incluyen más de 20 pacientes3,5,6,10,11,13–15, y apenas existen estudios de carácter prospectivo6. Destacamos en España los artículos recientemente publicados por Bagazgoitia et al.14 que incluyen 71 pacientes en un estudio multicéntrico retrospectivo y el de Bernabeu et al.3, un estudio descriptivo observacional de 28 casos. Nuestro estudio se ha efectuado prospectivamente en una cohorte de 20 pacientes para evaluar tanto la efectividad global y la seguridad como los diferentes factores que podrían influir en la respuesta de los HI al tratamiento con propranolol.
Las características epidemiológicas de los pacientes estudiados se corresponden con los de los HI en general17 y los incluidos en otras series14. Predominan el sexo femenino, la localización en la cabeza-cuello, la distribución focal, el tipo superficial y la fase proliferativa. La edad predominante en la que se inició el tratamiento fue a los 2-3 meses, y solo se ha utilizado en dos niñas mayores de 12 meses.
La mayoría de niños no habían recibido tratamiento previo, y a los 5 pacientes que habían recibido tratamiento con corticoides sin respuesta se les retiró la medicación progresivamente.
Algunos pacientes presentaban HI con varios problemas que podían justificar su tratamiento, sin embargo se consideró solo el motivo principal para instaurar el propranolol, que fue en la mayoría de casos (50%) el crecimiento rápido del hemangioma, para evitar el compromiso de estructuras adyacentes, destacando 4 casos (20%) con afectación periocular y compromiso de la apertura del ojo. Estos hallazgos coinciden con la tendencia actual de utilización del propranolol para HI de alto riesgo18. Destacamos asimismo la ulceración como segunda causa para iniciar el tratamiento.
El estudio cardiológico previo al inicio del tratamiento fue predominantemente normal en nuestros pacientes, y a pesar de que se detectaron 2 casos de CIA y un ductus arterioso persistente, estos hallazgos no impidieron el inicio del tratamiento tras la consulta con cardiología infantil. Asimismo, no se detectaron alteraciones en la RMN ni en el estudio oftalmológico, excepto en el caso 1 en que se apreciaron unos vasos retinianos tortuosos, sin otras alteraciones aparte del cierre ocular.
En cuanto a la posología del propranolol, en general, existe evidencia suficiente de que la dosis de 2mg/kg/día es la indicada, que es la que hemos empleado en nuestro estudio. Asimismo, se recomienda su administración en 3 tomas teniendo en cuenta la farmacocinética del fármaco. Sin embargo, algunos autores han utilizado dosis de 3mg/kg/día7, mientras que otros proponen empezar con dosis más bajas e incrementarlas progresivamente, según los controles15,19, e incluso ir doblando la dosis hasta 4mg/kg/día si no existe respuesta3,15. Conviene señalar que el propranolol oral no está comercializado para su uso en lactantes, por lo que es necesario recurrir a su preparación magistral. En nuestros pacientes su elaboración en el Servicio de Farmacia del hospital ha permitido adecuar la concentración de la solución al progresivo incremento de peso del lactante, y por tanto ha garantizado su correcta administración y posología. La fórmula magistral elaborada sin estabilizantes y con sacarosa permite administrar el fármaco sin incorporar posibles sustancias alergénicas que podrían ser nocivas para niños de tan corta edad. Sin embargo, el mejor excipiente está por establecer, teniendo en cuenta que se ha descrito algún caso de caries precoz en relación con el uso de un preparado de propranolol con sucrosa20, aunque no está claro si el propio efecto bloqueador beta del propranolol al disminuir la salivación puede favorecer la aparición de caries.
Existe un claro consenso de que antes de iniciar el tratamiento con propranolol para un HI debe efectuarse una valoración cardiológica previa12,14,16. La exclusión de casos con historia de hiperreactividad bronquial, el seguimiento analítico para descartar hipoglucemia, así como la monitorización de la TA y la FC son premisas ineludibles. El debate se centra en la mejor manera de monitorizar el uso de propranolol. Según algunos autores el riesgo de hipotensión y bradicardia, sobre todo en lesiones voluminosas o múltiples, puede comprometer el gasto cardíaco. Asimismo, se ha hablado del riesgo de hiperglucemia21 asociando secuelas neurológicas permanentes6,21. Estos posibles efectos han inducido a algunos autores a desarrollar una pauta de tratamiento con hospitalización durante 48 horas, empezando por una dosis de 0,16mg/kg/día, que se incrementa gradualmente, si los niveles de glucosa y las constantes son normales hasta la dosis de 2mg/kg/día9,19. Por otra parte, la larga experiencia en el uso de propranolol en lactantes con cardiopatías congénitas, desde etapas muy tempranas y a dosis mayores, no avalaría este supuesto, excepto durante la primera semana de vida, en la que la especial labilidad de los niños desaconseja su uso. La seguridad del propranolol se ha comprobado incluso en niños de muy bajo peso22. De forma excepcional se han descrito otros efectos adversos como diarrea23 o hipercaliemia24, y aunque en la mayoría de series publicadas los efectos secundarios detectados son escasos y de poca consideración siguen prevaleciendo los mensajes de prudencia ante la generalización del uso de este fármaco. Del mismo modo que otros autores5,8, en nuestros pacientes optamos por un seguimiento ambulatorio, y en ninguno de ellos hemos observado alteraciones en las cifras de glucemia ni durante su tratamiento atribuibles a una posible hipoglucemia. De hecho, este posible efecto adverso se podría evitar administrando el fármaco con las comidas y evitando su uso en lactantes menores de un mes, así como su uso simultáneo con corticoides orales que pueden incrementar dicho riesgo21. En este sentido, sería aconsejable advertir a los padres de los posibles síntomas de la hipoglucemia para que acudieran al hospital en caso de presentarlos.
Las cifras de TA, tanto sistólica como diastólica, y la FC se han mantenido en todos los casos y en todas las revisiones dentro de los percentiles normales por edad y sexo. La toma de TA por personal entrenado es quizás uno de los puntos a tener en cuenta en el control de estos niños, ya que en caso contrario se pueden distorsionar los valores. La curva de ganancia ponderal se ha ajustado en todos los casos dentro de los valores de referencia. Asimismo, un paciente, al que por error se le administró una dosis 8 veces mayor de la que le correspondía no presentó problemas, hecho ya referido con anterioridad25. El riesgo de que se desencadene una crisis asmática ha de tenerse muy en cuenta, evitando dicho tratamiento o interrumpiéndolo en pacientes con episodios de bronquiolitis, como ocurrió en uno de nuestros pacientes. El propranolol estaría formalmente contraindicado en el asma bien establecido, en el que sea necesario el uso continuo de broncodilatadores. El hecho de que la mitad de nuestros pacientes con respuesta excelente hubieran recibido tratamiento previo con corticoides orales refleja la gravedad de los HI de estos pacientes.
Queremos señalar que en nuestra experiencia el control ambulatorio de estos pacientes bajo supervisión ha sido efectivo y satisfactorio, y como han propuesto algunos autores quizás podría reducir los costes derivados de la hospitalización5.
En cuanto a la eficiencia, en nuestros casos la respuesta global obtenida ha sido predominantemente excelente, y en ninguno se ha considerado nula. A pesar de las limitaciones que puedan atribuirse al sistema de valoración de la respuesta que hemos utilizado en nuestros pacientes, podemos afirmar, al igual que en otros estudios, que el propanolol es efectivo para el tratamiento de los HI. Es importante destacar en este punto que no existe un consenso en cuanto a la forma de medir y ponderar la respuesta al tratamiento (5 expertos, valoración de color-tamaño, etc.) que varía según los diferentes estudios3,10,14. El tipo de valoración que hemos realizado es similar a la de Bayleis et al.26, si bien hemos sido más exigentes al requerir un 100% de concordancia entre los dos evaluadores y al incluir la escala de valoración paterna. Desde nuestro punto de vista, aunque no se haya referido en publicaciones previas, sería importante tener en cuenta la apreciación de los padres para la valoración final de la eficacia del tratamiento, ya que son una pieza fundamental en el adecuado seguimiento y la adherencia al tratamiento. Tal vez este consenso sería una herramienta a definir en un futuro por los expertos.
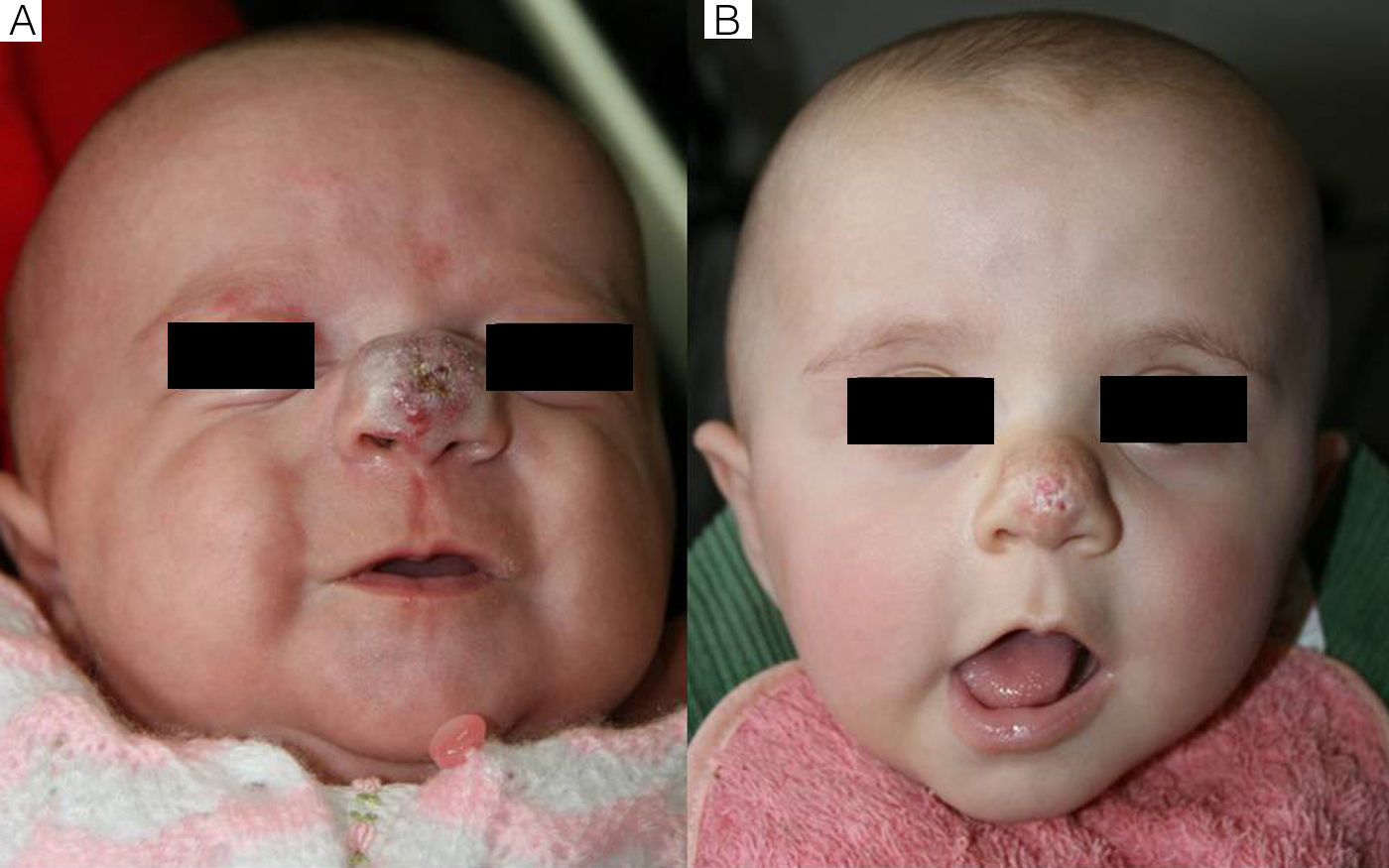
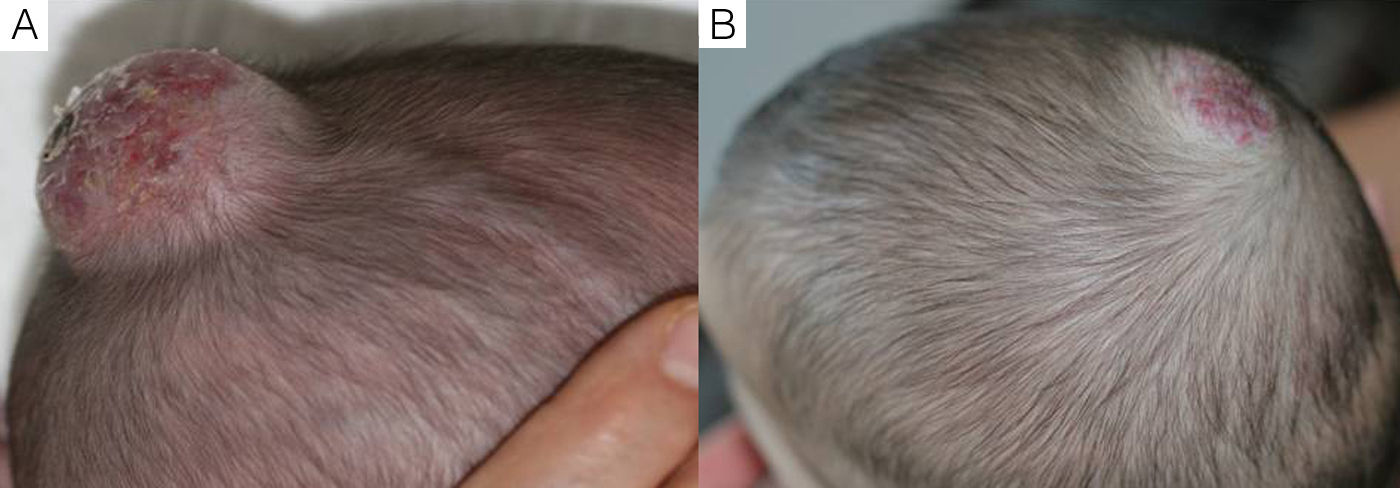
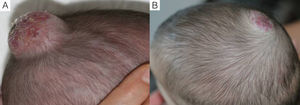
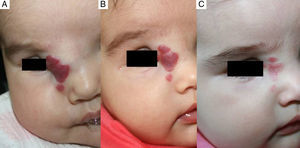
En cuanto a la relación entre la efectividad global y la localización del HI observamos que en todos los casos de localización periorbitaria obtuvimos una rápida apertura palpebral, con la consiguiente mejoría en el pronóstico de la visión del ojo afecto, coincidiendo con la experiencia positiva descrita por otros autores11,14. Es de destacar el caso número 1 (fig. 1), en el que la exploración oftalmológica previa al inicio del tratamiento objetivó la existencia de unos vasos retinianos tortuosos, siendo la valoración posterior prácticamente normal. Otros autores han observado mejoría de otras alteraciones oculares, como microftalmia o astigmatismo27. Por tanto, la indicación del propranolol en los HI periorbitarios está bastante clara, y de hecho este fármaco se ha posicionado como de primera línea en estos casos13. Sin embargo, destacamos el caso de un HI en el párpado cuyo tratamiento se inició tardíamente, a los 17 meses, cuya respuesta clínica fue mínima. En cuanto a los HI en otras localizaciones destacamos en nuestra serie que en los HI nasales se obtuvo una respuesta variable, ya que solo fue excelente en un caso (fig. 2), mientras que en el cuero cabelludo la respuesta fue excelente (fig. 3). Resaltamos asimismo la ausencia de casos con compromiso de las vías respiratorias. Finalmente hemos tratado un caso de hemangiomatosis neonatal benigna, sin hemangiomas viscerales, en que se decidió iniciar el tratamiento ante el aumento progresivo del número de lesiones que aumentaban en 2 al día hasta llegar a 23 elementos, consiguiéndose frenar la aparición de nuevas lesiones y la reducción de las lesiones previas. En la literatura se ha descrito algún caso de hemangiomatosis neonatal difusa asociada a hemangiomas viscerales que han respondido al tratamiento con propranolol28.
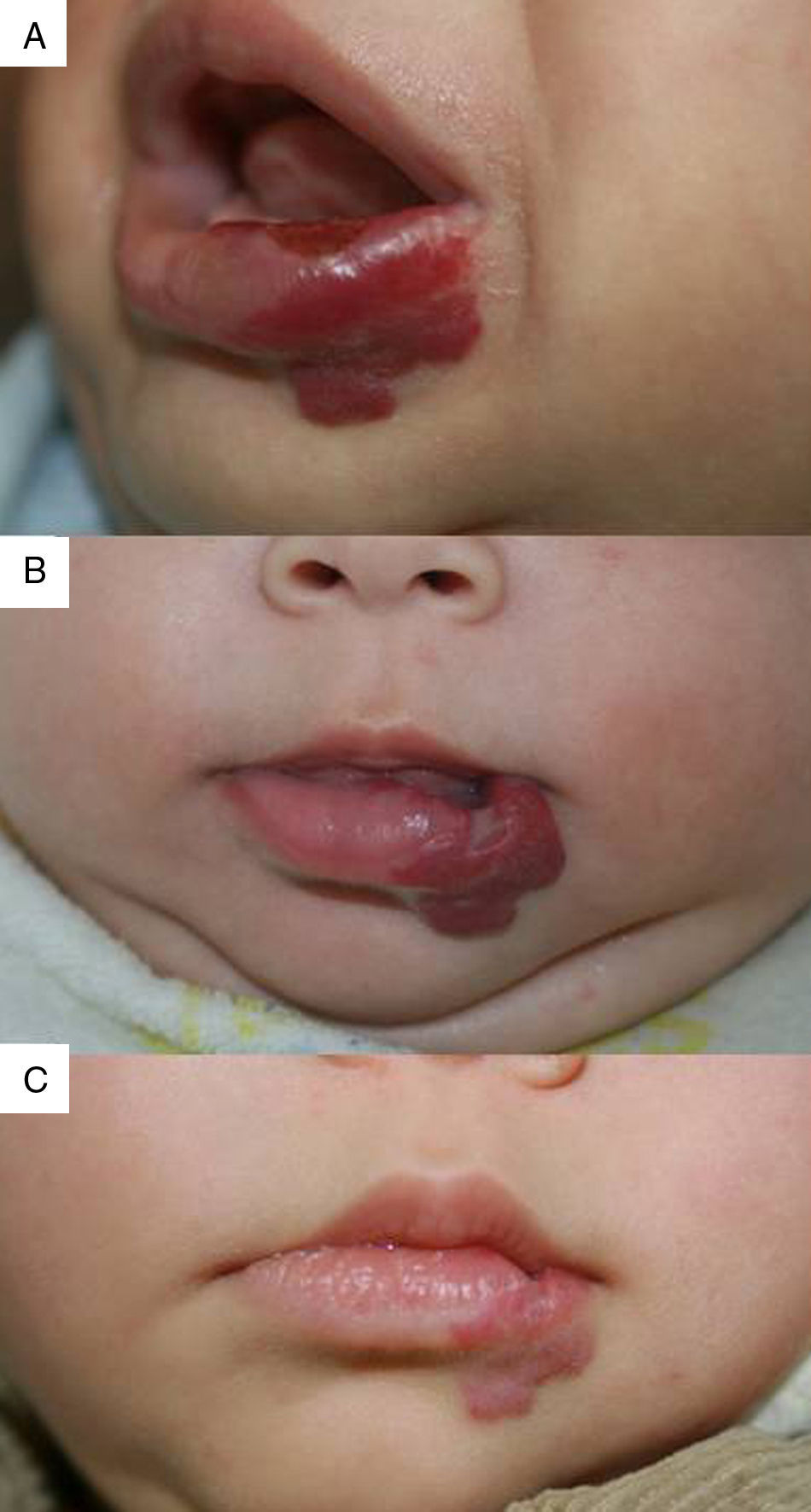
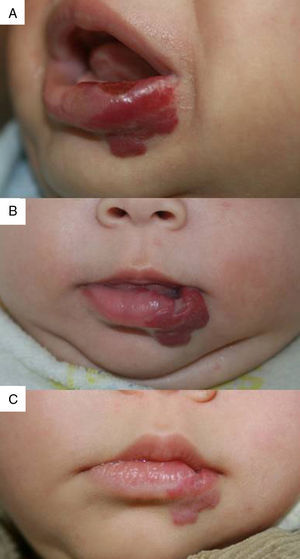
Hemos constatado la rápida resolución de la ulceración en todos los casos, independientemente de la localización en labio (fig. 4), espalda, brazo o cara. Todos los HI ulcerados habían recibido corticoides orales con anterioridad que se retiraron rápidamente al introducir el propranolol, por lo que no consideramos que hayan tenido un efecto determinante en la respuesta terapéutica obtenida. El tiempo de cicatrización, que se correspondería con el de la respuesta máxima, osciló entre 2 y 6 meses (tiempo medio: 4,2 meses). Algunos autores obtienen excelentes respuestas en los HI ulcerados y recomiendan el propranolol como una opción terapéutica de primera línea en los HI ulcerados9. Sin embargo, en otros trabajos la resolución de la ulceración no ha sido satisfactoria en la mayoría de casos3, por lo que está aún por confirmar si el propranolol supondrá una clara alternativa a la corticoterapia oral o al láser, como se ha propuesto29.
Queremos destacar la rapidez de acción en un elevado porcentaje de casos, ya percibida por los padres a los 2 días del inicio del tratamiento, que ya notaban cambio de color y ablandamiento del hemangioma, y que se pudo constatar en la segunda revisión, a los 5 días. En los casos en que existía oclusión ocular la apertura del ojo se consiguió en menos de una semana (fig. 1). En cuanto a la respuesta máxima la obtuvimos de modo preponderante antes de los 5 meses del inicio del tratamiento. Solo en 3 de nuestros casos el inicio de respuesta fue tardío (un mes). Los hallazgos presentados en este estudio coinciden con los existentes en la literatura, tanto en la rapidez de acción3,11,12 como en el pico de respuesta máxima del fármaco14. En los casos en que la respuesta se obtuvo precozmente el beneficio global ha sido bueno o excelente, mientras que aquellos en que el inicio de respuesta fue tardío la eficacia ha sido menor. Estos casos quizás podrían considerarse como respondedores parciales, y cabría plantearse la posibilidad de aumentar la dosis de manera precoz.
La mayoría de los casos han seguido tratamiento durante 6-7 meses; en un caso se prolongó durante 14 meses y 3 pacientes siguen aún con propranolol. Este es un punto importante, ya que como se ha demostrado, el propranolol ejerce su efecto no solo en la fase proliferativa, sino incluso después, por lo que no está claro cuándo es el mejor momento de suspender el tratamiento30. En los casos presentados, siguiendo la tendencia existente, hemos prolongado el tratamiento durante unos 6 meses o hasta finalizada la fase proliferativa para evitar el rebrote. En 2 de los casos (caso 1 y 10) se produjo un rebrote al reducir la dosis de propranolol y tras suspenderlo en otro (caso 8), lo que obligó a reintroducirlo y prolongar el tiempo de tratamiento. Se ha demostrado que el propranolol también actúa una vez finalizada la fase de proliferación del hemangioma y que en caso de tener que instaurar un segundo ciclo de tratamiento actuaría de nuevo con la misma eficacia4.
La mayoría de efectos secundarios que han presentado nuestros pacientes han sido de poca relevancia e inespecíficos, aunque descritos en relación con el propranolol como alteraciones del sueño, excesiva tranquilidad o intranquilidad, pérdida del apetito o frialdad acral. No hemos encontrado otras alteraciones de mayor gravedad como hipoglucemia, hipotensión, diarrea, hipocaliemia o alteraciones respiratorias, y el episodio de bronquiolitis observado en un caso no impidió seguir con el tratamiento una vez conseguido su control.
Hay que tener en cuenta que el propranolol produce una mejoría importante y global de los HI evitando el progreso de la fase proliferativa y acelerando su involución, sin que se consiga su desaparición completa en la mayoría de casos, ya que puede persistir el HI, pero con menor volumen y color más claro. Algunas secuelas, como el cambio de color, las telangiectasias o las cicatrices pueden observarse incluso en los casos en que la respuesta al tratamiento ha sido excelente. La presencia de una coloración periférica hemosiderótica puede ser transitoria y atribuible a la extravasación hemática tras la destrucción vascular. A pesar de estas secuelas, probablemente, una vez alcanzada la respuesta máxima al tratamiento y estabilizada la lesión, el HI no conseguiría mejorar, aun alargando indefinidamente el tratamiento con propranolol.
En conclusión, aun con las limitaciones propias de un trabajo con un reducido número de casos, consideramos que el propranolol es un medicamento eficaz y rápido en su acción para el tratamiento de los HI, aunque estos no lleguen a desaparecer totalmente y en la mayoría de casos persistan cambios de color, volumen, telangiectasias o cicatrices superficiales al concluir el tratamiento. Asimismo, se trata de un medicamento seguro, sin efectos secundarios importantes, cuyo control se puede seguir ambulatoriamente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.