La urticaria crónica espontánea, también conocida como urticaria crónica idiopática o urticaria crónica, es un proceso frecuente con una prevalencia estimada de entre el 0,5 y el 1% de la población general. Es un proceso que interfiere en la calidad de vida del paciente y ocasiona un notable impacto en los costes sanitarios directos e indirectos. La urticaria crónica es una entidad que plantea dificultades de manejo terapéutico. Se considera que los fármacos antihistamínicos H1 no sedantes son el tratamiento de primera elección. Su prescripción a las dosis recomendadas solo consigue una reducción de los síntomas en menos del 50% de los pacientes. Aunque las guías terapéuticas recomiendan incrementar las dosis en casos de respuestas no adecuadas, persiste un grupo de pacientes en los que no se consigue controlar la sintomatología. Existe, pues, la necesidad del desarrollo de nuevas alternativas terapéuticas cuya eficacia se establezca bajo criterios de medicina basada en la evidencia.
Chronic spontaneous urticaria, also known as chronic idiopathic urticaria or simply chronic urticaria, is a common disorder that has a prevalence in the general population that ranges between 0.5% and 1%. This condition negatively affects the patient's quality of life and has considerable impact on direct and indirect health-related costs. Chronic urticaria is difficult to manage. Nonsedating H1 antihistamines are the first line of therapy, but fewer than 50% of patients experience relief at recommended dosages. Although guidelines call for increasing the dosage when response is inadequate, some patients still do not achieve adequate control of symptoms. New treatment alternatives, with proven efficacy under the standards of evidence-based medical practice, must therefore be developed.
Existe un amplio espectro de factores que pueden desencadenar el desarrollo de lesiones de urticaria y/o angioedema, incluyendo estímulos físicos (frío, calor, presión, vibración, luz ultravioleta), fármacos (AINE, IECAs, opiáceos), infecciones (Helicobacter pylori, parásitos intestinales), alimentos, déficit de complemento o mecanismos autoinmunes. Hasta el momento no se ha asociado la urticaria con malignidad a diferencia de la vasculitis urticariforme. Al no haber un consenso en la definición de los criterios de imputabilidad, existe una gran variabilidad entre los distintos autores sobre la identificación de los factores etiológicos implicados en la urticaria crónica (UC) espontánea. En algunas series se identifica un factor etiológico en hasta un 40-50% de los casos. El término tradicional de UC idiopática debe evitarse o solo reservarse para aquellos casos en los que no se puede determinar ningún factor etiológico1–5.
La principal célula efectora en la génesis del habón es el mastocito cutáneo que tras su activación presenta un fenómeno de degranulación y la liberación de histamina y de otros mediadores vasoactivos y proinflamatorios. Los opioides, la IgE (el mastocito tiene en su membrana un receptor de alta afinidad para IgE [FC¿RI]), los factores del complemento (C5A) o la sustancia P, entre otros, son potenciales activadores del mastocito. Una vez activado, el mastocito libera gránulos que contienen principalmente histamina y también otros mediadores de la inflamación como factor activador de plaquetas (PAF), TNF alfa, IL-3, IL-4, IL-5, IL-6, IL-8, IL-13, GM-CSF, PGD-2 y leucotrienos (LTC4, LTD4, LTEA). La histamina, TNF alfa e IL-8 estimulan también las moléculas de adhesión endotelial con lo que se favorece la migración de eosinófilos, monocitos y neutrófilos desde el torrente sanguíneo a la piel3,4. Recientemente se ha propuesto que la trombina podría tener un papel en la patogenia de la UC, ya que se ha visto que aumenta la permeabilidad vascular, actúa en la vía del complemento y favorece la degranulación del mastocito6.
La UC (habones y/o angioedema>6 semanas) es una enfermedad cutánea con unas tasas de prevalencia en la población general de aproximadamente 0,1-3%7. Muchos de los pacientes con UC refieren una disminución considerable de la calidad de vida como consecuencia del prurito, alteraciones del sueño, fatiga, aislamiento social o trastornos emocionales, siendo comparable su impacto en la calidad de vida de los pacientes con el que presentan los pacientes con enfermedades coronarias graves8,9. La UC espontánea representa cerca del 70% de todas las UC y puede persistir durante varios años.
Se ha demostrado que aproximadamente un tercio de los pacientes con UC espontánea presentan una respuesta positiva tras la inyección intradérmica del propio suero (autorreactividad sérica) en la prueba del suero autólogo (ASST). Sin embargo, solo en algunos de estos pacientes puede demostrarse la presencia de autoanticuerpos contra el FC¿RI o contra la propia IgE (autoinmunidad). La UC autoinmune (UCA) representa un 30-50% de todas las UC.
En la UCA existe una activación permanente de los mastocitos cutáneos como consecuencia de la presencia de autoanticuerpos funcionales IgG contra la subunidad alfa del FC¿RI (30-50%) o directamente contra la IgE de los mastocitos (5-10%). Los basófilos también expresan FC¿RI, por lo que en pacientes con UCA suele detectarse una reducción de los niveles de basófilos. Puede demostrarse la capacidad del suero del paciente de inducir degranulación del basófilo sano mediante la detección de autoanticuerpos funcionales in vitro. Recientemente, se ha descrito que autoanticuerpos IgE antitiroperoxidasa también pueden inducir la degranulación del mastocito. En la degranulación del mastocito se ha implicado también el papel de la vía clásica del complemento, sobre todo el factor C5A que aparte de promover la degranulación de los mastocitos y basófilos, interviene la quimiotaxis atrayendo a neutrófilos, eosinófilos y monocitos. En un 25% de las UCA se detectan anticuerpos antitiroideos (en contraste con un 6% en la población general) y se ha asociado frecuentemente a enfermedades como la tiroiditis de Hashimoto y la enfermedad de Graves (menos frecuente). También se ha descrito su asociación con otras enfermedades autoinmunes como la diabetes mellitus o el vitíligo.
Bases generales del tratamiento de la urticaria crónicaMedidas generalesEn el tratamiento de la urticaria es importante evitar los posibles desencadenantes o agravantes inespecíficos como el calor, el estrés, el alcohol y algunos fármacos como el ácido acetilsalicílico, los AINE, los IECA (especialmente si se manifiesta como angioedema con o sin habones) o la codeína. Pueden utilizarse lociones refrescantes antipruriginosas como calamina o mentol al 1% en crema acuosa2,3,10,11.
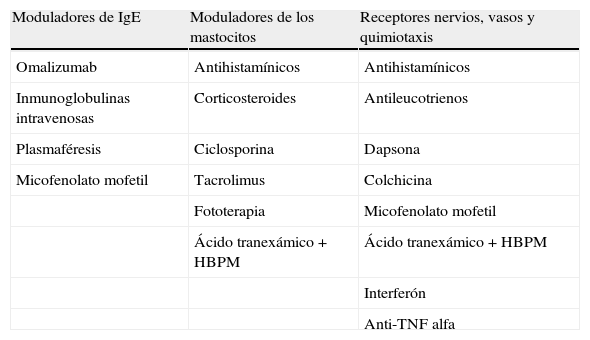
Tratamiento farmacológicoLos tratamientos de la UC se pueden clasificar en relación con sus distintos efectos funcionales. La mayoría de los fármacos modulan la capacidad de degranulación del mastocito y de liberación de sus mediadores. Se incluyen en este grupo ciertos antihistamínicos, los corticosteroides, la ciclosporina A (CsA), el tacrolimus, el metotrexato o la fototerapia. Los fármacos empleados rutinariamente en la terapia de la UC ejercen su efecto bloqueando los receptores y modulando los mediadores que situados sobre las fibras nerviosas y los vasos sanguíneos inducen prurito, vasodilatación y quimiotaxis. Se trata de los fármacos mayoritariamente empleados en el manejo de la UC e incluyen antihistamínicos (anti-H1 y H2), antileucotrienos, o la dapsona, por ejemplo. Algunos principios activos actúan previamente a la activación de la célula efectora o mastocito. Este grupo incluye el omalizumab (un anticuerpo monoclonal con capacidad para unirse a la IgE), la plasmaféresis o las inmunoglobulinas intravenosas (tabla 1).
Mecanismo de acción de los tratamientos de la urticaria crónica
| Moduladores de IgE | Moduladores de los mastocitos | Receptores nervios, vasos y quimiotaxis |
| Omalizumab | Antihistamínicos | Antihistamínicos |
| Inmunoglobulinas intravenosas | Corticosteroides | Antileucotrienos |
| Plasmaféresis | Ciclosporina | Dapsona |
| Micofenolato mofetil | Tacrolimus | Colchicina |
| Fototerapia | Micofenolato mofetil | |
| Ácido tranexámico+HBPM | Ácido tranexámico+HBPM | |
| Interferón | ||
| Anti-TNF alfa |
HBPM: heparina de bajo peso molecular; TNF: tumoral necrosis factor.
La histamina desempeña un papel clave en la formación de la lesión típica de urticaria. Se ha observado que en pacientes afectos de UC los niveles locales de histamina son mayores que en individuos sanos tanto en la piel afecta como en la piel sana12. Existen 4 tipos de receptores para la histamina en la piel: los receptores H1 mayoritariamente se ubican en endotelio, músculo liso y sistema nervioso central, los receptores H2 se sitúan también en las células parietales del tubo digestivo y los H3 en el sistema nervioso central y el músculo liso bronquial. Los receptores H4 son actualmente objeto de investigación terapéutica y se hallan presentes en las células dendríticas de la piel, el timo, el bazo, el intestino delgado y el colon. Los antihistamínicos son eficaces en el tratamiento de la urticaria debido a su efecto agonista inverso sobre los receptores H1.
Los antihistamínicos han sido utilizados en el tratamiento de la UC desde hace más de 60 años y siguen siendo el tratamiento de primera elección. La mayoría de los síntomas de la urticaria son la consecuencia de las acciones de la histamina sobre los receptores H1 localizados en las células endoteliales (habón) y en las terminaciones nerviosas sensitivas (prurito). Los antihistamínicos actúan sobre el endotelio de las vénulas poscapilares disminuyendo la extravasación y la formación del habón, y sobre las fibras nerviosas aferentes C de la piel reduciendo el prurito. También tienen efecto sobre los reflejos axonales cutáneos, mecanismo por el que consiguen disminuir el eritema. Muchos de los antihistamínicos poseen actividad antiinflamatoria al reducir los niveles de mediadores preformados y neoformados de citocinas y moléculas de adhesión celular lo que conlleva una disminución del reclutamiento de células inflamatorias (linfocitos, monocitos, neutrófilos, eosinófilos). Estas acciones pueden atribuirse principalmente a 2 mecanismos: la estabilización de las membranas de basófilos y mastocitos por parte de antihistamínicos H1 y la inhibición de factores de transcripción citoplasmática como el factor nuclear kappa-B13.
Los antihistamínicos se pueden clasificar en función del receptor sobre el cual actúan en anti-H1, anti-H2, anti-H3 y anti-H4. Actualmente los antihistamínicos utilizados en el tratamiento de la UC corresponden a antihistamínicos H1 de primera generación, antihistamínicos H1 de segunda generación y antihistamínicos H2.
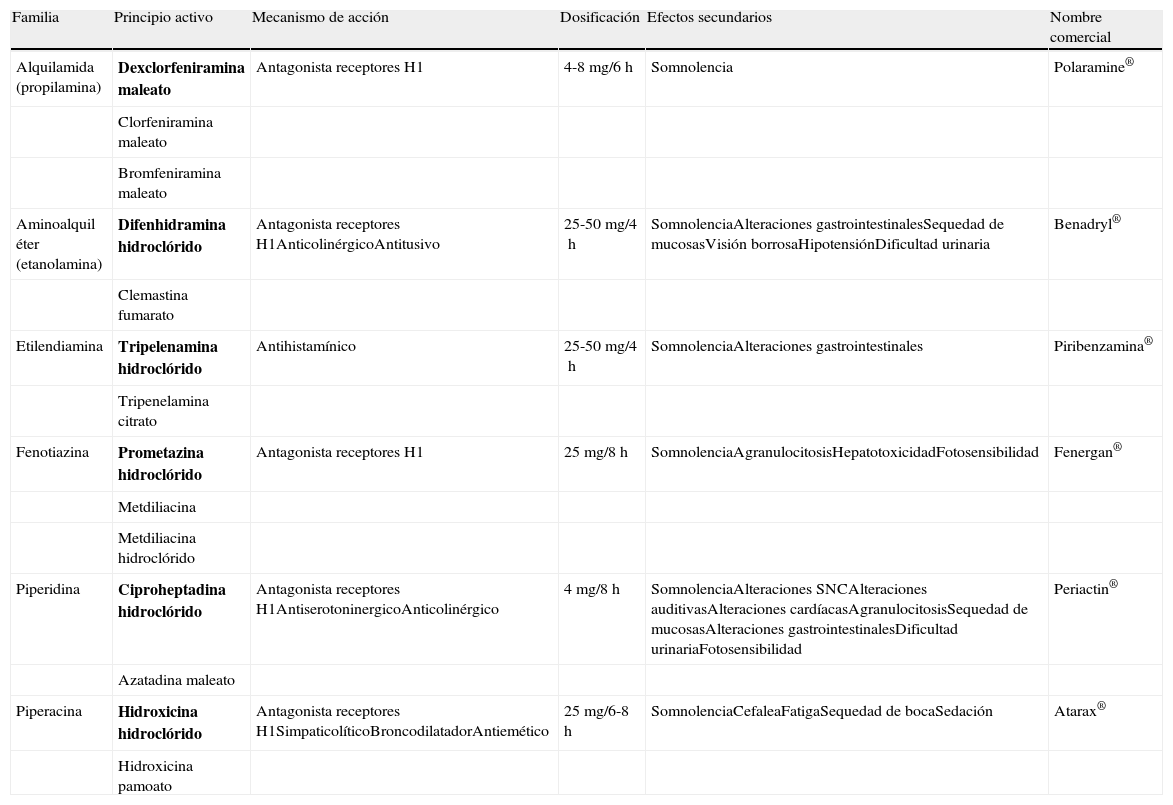
Los antihistamínicos H1 de primera generación han sido utilizados desde hace muchos años para el tratamiento de la UC y otras enfermedades de base alérgica. Poseen efectos anticolinérgicos y atraviesan la barrera hematoencefálica, por lo que presentan un efecto sedante. Dichos efectos secundarios pueden limitar la adherencia al tratamiento, por lo que suelen reservarse para aquellos casos en los que la sintomatología pruriginosa es de predominio nocturno (que impide conciliar el sueño) y en pacientes no respondedores a antihistamínicos de segunda generación. Dentro de este grupo se encuentran la hidroxicina, la difenhidramina, ciproheptadina y la dexclorfeniramina (tabla 2).
Tabla comparativa de los antihistamínicos H1 de primera generación
| Familia | Principio activo | Mecanismo de acción | Dosificación | Efectos secundarios | Nombre comercial |
| Alquilamida (propilamina) | Dexclorfeniramina maleato | Antagonista receptores H1 | 4-8mg/6h | Somnolencia | Polaramine® |
| Clorfeniramina maleato | |||||
| Bromfeniramina maleato | |||||
| Aminoalquil éter (etanolamina) | Difenhidramina hidroclórido | Antagonista receptores H1AnticolinérgicoAntitusivo | 25-50mg/4h | SomnolenciaAlteraciones gastrointestinalesSequedad de mucosasVisión borrosaHipotensiónDificultad urinaria | Benadryl® |
| Clemastina fumarato | |||||
| Etilendiamina | Tripelenamina hidroclórido | Antihistamínico | 25-50mg/4h | SomnolenciaAlteraciones gastrointestinales | Piribenzamina® |
| Tripenelamina citrato | |||||
| Fenotiazina | Prometazina hidroclórido | Antagonista receptores H1 | 25mg/8h | SomnolenciaAgranulocitosisHepatotoxicidadFotosensibilidad | Fenergan® |
| Metdiliacina | |||||
| Metdiliacina hidroclórido | |||||
| Piperidina | Ciproheptadina hidroclórido | Antagonista receptores H1AntiserotoninergicoAnticolinérgico | 4mg/8h | SomnolenciaAlteraciones SNCAlteraciones auditivasAlteraciones cardíacasAgranulocitosisSequedad de mucosasAlteraciones gastrointestinalesDificultad urinariaFotosensibilidad | Periactin® |
| Azatadina maleato | |||||
| Piperacina | Hidroxicina hidroclórido | Antagonista receptores H1SimpaticolíticoBroncodilatadorAntiemético | 25mg/6-8h | SomnolenciaCefaleaFatigaSequedad de bocaSedación | Atarax® |
| Hidroxicina pamoato |
Los nombres en negrita corresponden al principio activo del fármaco que aparece en la ultima columna con nombre comercial.
Los antihistamínicos H1 de segunda generación también han demostrado su eficacia en el tratamiento de los síntomas de la urticaria. Algunos incluso han demostrado una mayor afinidad en su unión al receptor de la histamina que los antihistamínicos H1 de primera generación (por ejemplo la rupatadina)14. No atraviesan la barrera hematoencefálica, por lo que no ocasionan efectos sedantes y no suelen presentar efectos secundarios anticolinérgicos. Son el único tratamiento con evidencia clase 1 y grado de recomendación A. Son fármacos de elección en el tratamiento actual de la UC. No obstante, en gran parte de los pacientes los síntomas persisten a pesar del tratamiento con antihistamínicos a dosis recomendadas. En un estudio reciente realizado por Maurer et al., se observó que hasta un 50% de los pacientes con UC no respondían a las dosis recomendadas de antihistamínicos5, probablemente como consecuencia de que las dosis recomendadas han sido establecidas para el tratamiento de otras enfermedades de base alérgica como la rinitis estacional. En estos casos se recomienda aumentar la dosis de antihistamínico hasta 4 veces la dosis recomendada. En la formación del habón en los pacientes con UC han sido implicados otros mediadores liberados por los mastocitos como son citocinas, eicosanoides, proteasas y PAF15. Recientemente se ha observado que PAF puede inducir in vitro la degranulación de los mastocitos cutáneos16. Nosotros mismos hemos podido estudiar las peculiaridades del habón inducido por PAF en voluntarios sanos. Un habón que en estos casos era independiente de la degranulación del mastocito17.
Dos potentes antihistamínicos H1 de segunda generación, terfenadina y astemizol, fueron retirados del mercado por la aparición de efectos secundarios cardíacos (arritmias ventriculares -torsade de pointes-). Desde entonces, tanto la «Food and Drug Administration» como la Agencia Europea de Medicamentos requieren estudios de cardiotoxicidad en el desarrollo de cualquier nuevo fármaco antihistamínico.
Se han realizado múltiples ensayos clínicos comparando los distintos antihistamínicos de segunda generación entre ellos y con un grupo placebo, no habiéndose detectado diferencias estadísticamente significativas en cuanto a control de los síntomas, perfil de seguridad ni calidad de vida del paciente13,18–22. Los antihistamínicos H1 de segunda generación incluyen los siguientes fármacos:
AcrivastinaPosee una vida media corta, por lo que debe administrarse 3 veces al día (el resto de los antihistamínicos suelen recomendarse una vez al día). Su inicio de acción es rápido. Se excreta intacto en orina, por lo que debe evitarse su uso en casos de insuficiencia renal moderada23.
CetirizinaEs el metabolito activo de la hidroxicina, por lo que puede presentar efectos sedantes, especialmente a dosis altas. La cetirizina alcanza la concentración máxima en plasma en un periodo de tiempo muy corto, lo que puede representar una ventaja clínica importante por su rápida biodisponibilidad. Posee efectos antialérgicos sobre los mediadores inflamatorios liberados por los mastocitos sobre todo a dosis altas. Debe evitarse en casos de insuficiencia renal grave24.
LevocetirizinaEnantiómero activo de la cetirizina. Más potente13. Posee una potencia superior con respecto a otros antihistamínicos en la inhibición del habón y del eritema tras la inyección intradérmica de histamina25.
LoratadinaMetabolismo de primer paso hepático donde se transforma a su molécula activa, la desloratadina. Posee propiedades antialérgicas26.
DesloratadinaEs el principio activo de la loratadina, por lo que es más potente que esta. Tiene el tiempo medio de eliminación más prolongado (T1/227h) con lo cual es necesario dejar de tomarlo 6 días antes de realizar «prick test» cutáneo. Se une de forma selectiva y con alta afinidad al receptor H1. Posee asimismo actividad antiinflamatoria y antialérgica al actuar sobre citocinas y moléculas de adhesión celular. Inhibe otros mediadores implicados en la aparición de habones como las citocinas IL-4, IL-13, IL-6, TNF alfa y GM-CSF, quimiocinas como IL-8, RANTES y moléculas de adhesión como P-selectina e ICAM-1. Reduce la quimiotaxis de los eosinófilos y su activación in vitro27,28. Tanto la desloratadina como la loratadina deben ser utilizados con precaución en casos de insuficiencia renal severa.
MizolastinaEstá contraindicada en enfermedades cardíacas clínicamente significativas, ya que puede producir prolongación del intervalo QT. No debe administrarse concomitantemente con fármacos que inhiban el metabolismo hepático por la vía del citocromo P450 (incluidos antibióticos macrólidos y antifúngicos imidazólicos) ni con fármacos con propiedades potencialmente arrítmicas (antidepresivos tricíclicos como doxepina incluidos). Su uso está contraindicado en casos de insuficiencia hepática.
EbastinaEs un antihistamínico H1 de segunda generación con estructura basada en oxipiperidina. Tiene metabolismo de primer paso hepático. Su forma activa es la carebastina. Se elimina principalmente por orina. Produce una inhibición dosis-dependiente de la liberación de histamina por los mastocitos cutáneos. Tiene actividad sobre los receptores H1 y también inhibe la liberación de mediadores inflamatorios por los mastocitos22,29. En pacientes con insuficiencia renal o hepática hay que ajustar dosis (habitualmente 10mg).
RupatadinaEs un nuevo antihistamínico de segunda generación de vida media larga. Es un antagonista dual de los receptores H1 a nivel periférico y PAF. Rupatadina inhibe competitivamente la agregación plaquetaria inducida por PAF in vitro aunque en menor medida que su antagonista específico. Posee también propiedades antiinflamatorias: inhibe la quimiotaxis de eosinófilos in vivo e in vitro, suprime la formación de citocinas inflamatorias de los linfocitos T activados in vitro e impide la degranulación y la liberación de histamina y otras citocinas por los mastocitos cutáneos14,15,22,30,31. Está indicado para el tratamiento de la UC y la rinitis alérgica. La dosis habitual es de 10mg. El número de pacientes con UC respondedores a rupatadina aumenta significativamente si se dobla la dosis (20mg). Es un fármaco seguro y bien tolerado.
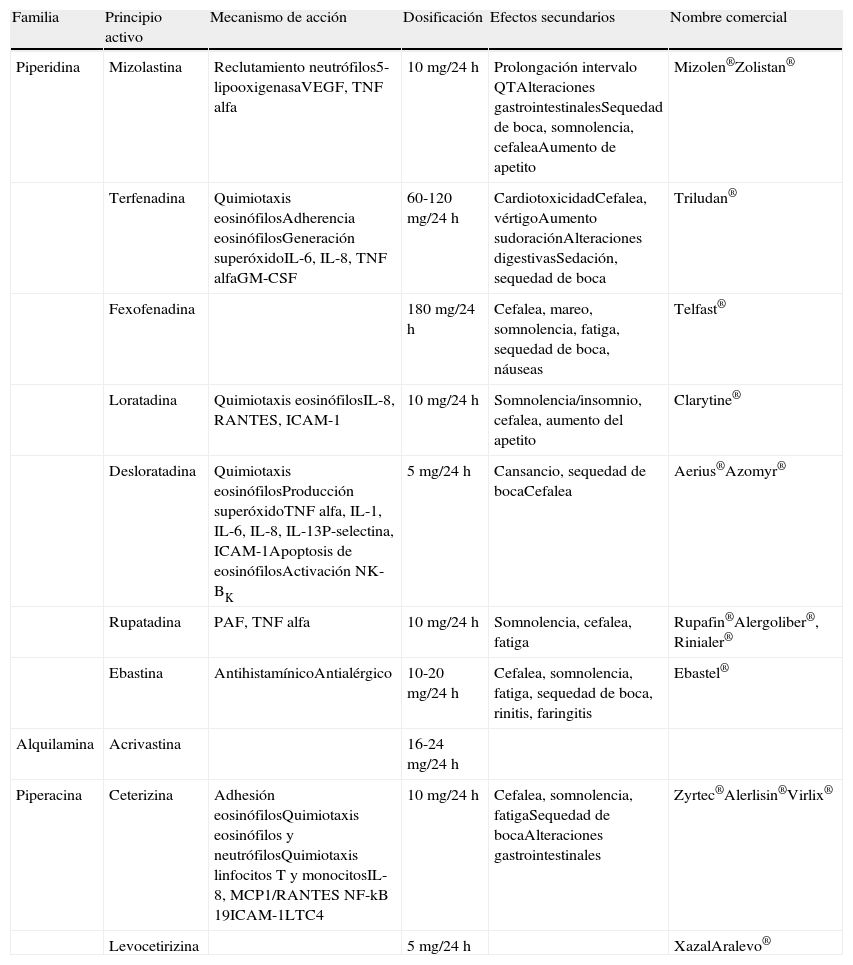
FexofenadinaPotente antihistamínico selectivo para los receptores H1 periféricos. Es un fármaco eficaz para el tratamiento tanto de la UC como de la rinitis alérgica32 (tabla 3).
Tabla comparativa de los antihistamínicos H1 de segunda generación
| Familia | Principio activo | Mecanismo de acción | Dosificación | Efectos secundarios | Nombre comercial |
| Piperidina | Mizolastina | Reclutamiento neutrófilos5-lipooxigenasaVEGF, TNF alfa | 10mg/24h | Prolongación intervalo QTAlteraciones gastrointestinalesSequedad de boca, somnolencia, cefaleaAumento de apetito | Mizolen®Zolistan® |
| Terfenadina | Quimiotaxis eosinófilosAdherencia eosinófilosGeneración superóxidoIL-6, IL-8, TNF alfaGM-CSF | 60-120mg/24h | CardiotoxicidadCefalea, vértigoAumento sudoraciónAlteraciones digestivasSedación, sequedad de boca | Triludan® | |
| Fexofenadina | 180mg/24h | Cefalea, mareo, somnolencia, fatiga, sequedad de boca, náuseas | Telfast® | ||
| Loratadina | Quimiotaxis eosinófilosIL-8, RANTES, ICAM-1 | 10mg/24h | Somnolencia/insomnio, cefalea, aumento del apetito | Clarytine® | |
| Desloratadina | Quimiotaxis eosinófilosProducción superóxidoTNF alfa, IL-1, IL-6, IL-8, IL-13P-selectina, ICAM-1Apoptosis de eosinófilosActivación NK-BK | 5mg/24h | Cansancio, sequedad de bocaCefalea | Aerius®Azomyr® | |
| Rupatadina | PAF, TNF alfa | 10mg/24h | Somnolencia, cefalea, fatiga | Rupafin®Alergoliber®, Rinialer® | |
| Ebastina | AntihistamínicoAntialérgico | 10-20mg/24h | Cefalea, somnolencia, fatiga, sequedad de boca, rinitis, faringitis | Ebastel® | |
| Alquilamina | Acrivastina | 16-24mg/24h | |||
| Piperacina | Ceterizina | Adhesión eosinófilosQuimiotaxis eosinófilos y neutrófilosQuimiotaxis linfocitos T y monocitosIL-8, MCP1/RANTES NF-kB 19ICAM-1LTC4 | 10mg/24h | Cefalea, somnolencia, fatigaSequedad de bocaAlteraciones gastrointestinales | Zyrtec®Alerlisin®Virlix® |
| Levocetirizina | 5mg/24h | XazalAralevo® |
GM-CSF: factor estimulante de las colonias de granulocitos-macrófagos; ICAM: molécula de adhesión intercelular; IL: interleucina; LTC4: leucotrieno C4; PAF: factor activador de plaquetas (platelet activation factor); RANTES: regulated and normal T cell expressed and secreted; TNF alfa: factor de necrosis tumoral; VEGF: factor de crecimiento del endotelio vascular.
Los antihistamínicos H2 tienen un papel controvertido en el tratamiento de la UC. Los vasos sanguíneos cutáneos contienen tanto receptores H1 como receptores H2 y la activación de ambos tipos induciría la formación de habón y eritema, aunque la activación de H2 posee un escaso efecto sobre el prurito. Existen diversos estudios de valoración de la eficacia de la combinación antihistamínicos H1 y antihistamínicos H2 en los que se observa un posible efecto sinérgico. Sin embargo, esta asociación no parece justificada en el tratamiento de la UC al no haberse demostrado una eficacia significativamente superior. En este grupo se encuentran cimetidina, ranitidina, nizatidina y famotidina13,18.
Situaciones especiales2–4,10,11,13,18,23Embarazo y lactanciaDebe intentar evitarse el uso de cualquier fármaco durante el embarazo, incluidos los antihistamínicos, especialmente durante el primer trimestre. Los antihistamínicos se sitúan en las categorías B y C de riesgo durante el embarazo. Dentro de la categoría B (no existe evidencia de daño fetal durante el embarazo) se incluyen los antihistamínicos de segunda generación cetirizina y loratadina. Suele recomendarse, dada la mayor experiencia acumulada, la prescripción de antihistamínicos de primera generación como clorfeniramina. Si hay que utilizar un antihistamínico durante la fase de lactancia se aconseja también la cetirizina o la loratadina a las menores dosis posibles.
InfanciaTodos los antihistamínicos se pueden usar en niños mayores de 12 años. Para el tratamiento de la UC está aprobado el uso en mayores de 2 años la cetirizina, la loratadina y la desloratadina.
Insuficiencia renal/hepáticaLos antihistamínicos que se eliminan en mayor proporción por la orina son la cetirizina (60%) y la levocetirizina (85%). El resto de los antihistamínicos de segunda generación solo presentan una excreción urinaria del 10-20%. La mayoría de estos fármacos suelen conllevar un metabolismo que implica un primer paso hepático vía citocromo P-450 o CYP, a excepción de la cetirizina, la levocetirizina, la fexofenadina y la desloratadina. De todos modos, en caso de enfermedad renal o hepática grave se recomienda disminuir la dosis de todos los antihistamínicos H1 de segunda generación.
Antidepresivos tricíclicosLos antidepresivos tricíclicos como la amitriptilina o sobre todo la doxepina han sido utilizados ampliamente en el tratamiento de la UC por su potente efecto antihistamínico H1 y H2. Sin embargo, su uso está limitado por sus efectos sedantes y anticolinérgicos que se potencian con el uso de alcohol, y por el riesgo relativo de arritmias cardíacas secundarias al alargamiento del intervalo QT. Suele recomendarse su administración por la noche (por sus efectos sedantes) y son especialmente útiles en casos en los que coexiste depresión. En el tratamiento de la UC la doxepina se usa a dosis de 10-30mg13,18.
AntileucotrienosEl más utilizado es el montelukast, un antagonista del receptor de los leucotrienos que se ha utilizado en el tratamiento del asma y en la urticaria. Existe muy poca evidencia de su eficacia en monoterapia2,3,10,33,34. Pueden asociarse a antihistamínicos H1 en urticarias de difícil control. Aunque su respuesta es poco predecible, existen estudios que sugieren que el montelukast puede ser efectivo en el tratamiento de la urticaria autoinmune, la urticaria por presión retardada y en la urticaria complicada con intolerancia al ácido acetilsalicílico o a colorantes alimentarios, pero no ha mostrado ninguna o casi ninguna efectividad en urticaria crónica idiopática. Se ha utilizado para tratar la urticaria eosinofílica (infiltrado eosinofílico en la biopsia cutánea) dado que los eosinófilos activados inducen la síntesis de mediadores eicosanoides generados a partir de ácido araquidónico y leucotrienos, particularmente LTC4, LTD4 y LTE3. Los leucotrienos actúan atrayendo células a los lugares de la inflamación y así amplificando la respuesta inflamatoria.
CorticosteroidesNo existen estudios controlados del uso de los corticosteroides en el tratamiento de la urticaria/angioedema pero su efectividad generalmente se acepta como tal (grado de recomendación D). Se recomienda su prescripción a ciclos cortos y en pautas descendentes en el tratamiento de exacerbaciones severas de la UC especialmente cuando se acompaña de angioedema por el riesgo de dificultad respiratoria secundaria. También pueden administrarse cuando existen dificultades en el control de los síntomas con antihistamínicos en monoterapia o cuando se desea obtener una mejoría clínica rápida. Se han utilizado asimismo en el tratamiento de la urticaria vasculitis. Se recomienda administrar la dosis mínima eficaz y evitar tratamientos prolongados para eludir sus efectos secundarios. Los corticosteroides tópicos no deben utilizarse en la UC2.
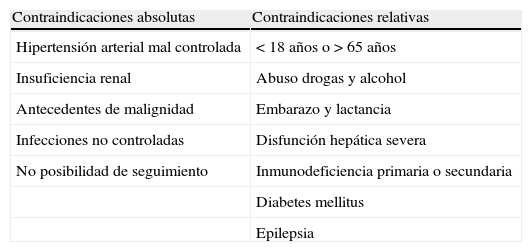
Ciclosporina ALa CsA es un inhibidor de la calcineurina, proteína con actividad fosfatasa que permite la entrada del factor nuclear de células T del citoplasma al núcleo y la expresión del gen de la IL-2 que activa las células T y estimula la secreción de interferón gamma, factor estimulador de colonias de granulocitos y macrófagos. Por lo tanto, la CsA actúa bloqueando la síntesis de IL-2 provocando una situación de inmunosupresión celular y humoral35,36. Los principales efectos secundarios son la neurotoxicidad y la hipertensión arterial (tabla 4). En el manejo de la UC la ciclosporina está indicada en pacientes con UC grave con ASST positiva que no han respondido a antihistamínicos. Se usa a dosis de 3-5mg/kg/día por lo menos durante 2 meses. Las dosis y la duración óptima del tratamiento no han sido definidas y no existen criterios predictivos de respuesta37. Se ha observado también respuesta en pacientes con UC espontánea (sin evidencia de autoanticuerpos funcionales -ASST negativa-), aunque no está tan bien documentado en la literatura y los efectos del tratamiento son menos predecibles que en pacientes con UCA38.
Contraindicaciones para tratamiento con ciclosporina A
| Contraindicaciones absolutas | Contraindicaciones relativas |
| Hipertensión arterial mal controlada | <18 años o>65 años |
| Insuficiencia renal | Abuso drogas y alcohol |
| Antecedentes de malignidad | Embarazo y lactancia |
| Infecciones no controladas | Disfunción hepática severa |
| No posibilidad de seguimiento | Inmunodeficiencia primaria o secundaria |
| Diabetes mellitus | |
| Epilepsia |
Se ha usado con éxito para el tratamiento de UC corticodependiente a dosis de 0,5-2mg/kg/día en 2 tomas. Actúa inhibiendo los linfocitos T y disminuyendo la liberación de citocinas inflamatorias39.
Micofenolato mofetilEl micofenolato mofetil es un fármaco inmunomodulador que actúa inhibiendo la síntesis de ADN en los linfocitos. Es un inhibidor reversible de la inosina monofosfato deshidrogenasa (presente exclusivamente en linfocitos e involucrada en la síntesis de purinas). En la UC inhibe la producción de autoanticuerpos frente al receptor de alta afinidad de IgE o frente a la propia IgE. También reduce la expresión de moléculas de adhesión en células endoteliales e inhibe la migración de linfocitos a la piel40. Se ha visto que el uso de micofenolato mofetil para el tratamiento de la UC (tanto autoinmune como idiopática) puede ser efectivo en la disminución del prurito, la duración, el número de habones y el número de episodios de urticaria/angioedema. En algunos casos se ha comunicado una remisión completa. Se han utilizado dosis de 500mg/12h durante 2-4 semanas. Es un fármaco seguro y con pocos efectos secundarios (principalmente gastrointestinales a las dosis usadas para el tratamiento de la UC, aunque estos mejoran con el tiempo)41.
CiclofosfamidaSe ha descrito algún caso de buenos resultados con ciclofosfamida intravenosa al alcanzar la remisión completa en pacientes con urticaria corticodependiente42.
MetotrexatoPuede ser de utilidad en algunos casos como fármaco ahorrador de corticosteroides en pacientes con UC corticodependiente a dosis de 10-15mg semanales43.La presencia o ausencia de autoanticuerpos en suero no parece relacionarse con la respuesta. Se considera que la respuesta se halla más relacionada con su efecto antiinflamatorio que inmunosupresor. Por lo tanto, es tan eficaz en el tratamiento de la UC idiopática como en el de la autoinmune.
Fármacos anti-factor de necrosis tumoralExiste escasa literatura sobre el tratamiento de la UC con inhibidores de TNF alfa. Magerl et al. describieron el caso de un paciente con psoriasis y UC por presión retardada en el que el tratamiento con etanercept consiguió una mejoría rápida y persistente44.
FototerapiaLa fototerapia reduce el número de mastocitos cutáneos en la dermis superficial45. Se ha utilizado para el tratamiento de la UC idiopática y en el dermografismo sintomático. Puede realizarse con UVA, UVB o UVB de banda estrecha durante 1-3 meses. Con UVB de banda estrecha se han visto buenos resultados como tratamiento complementario junto a antihistamínicos. En algunos casos se ha observado una eficacia a largo plazo (hasta 3 meses después de finalizar el tratamiento)46.
Inmunoglobulinas intravenosasLas indicaciones de las inmunoglobulinas intravenosas aceptadas por la «Food and Drug Administration» son inmunodeficiencias primarias, inmunodeficiencias secundarias, enfermedad de Kawasaki y la púrpura trombocitopénica idiopática47. En el tratamiento de la UC se ha utilizado sobre todo para la UCA refractaria a otros tratamientos. O’Donell et al. trataron a 10 pacientes con UCA severa a dosis de 400mg/kg/día durante 5 días con mejoría clínica en 9 de los 10 pacientes, en 3 de los cuales hubo una mejoría a largo plazo48. También se ha descrito algún caso de buena respuesta en pacientes con urticaria por presión retardada y urticaria solar49. El mecanismo de acción involucrado no está del todo claro, pero se ha propuesto que las inmunoglobulinas intravenosas podrían contener anticuerpos antiidiotípicos que competirían con las IgG endógenas por los receptores H1, bloqueando la liberación de histamina. La saturación de la Fc de los receptores por inmunoglobulinas evita la unión de IgE a los mastocitos cutáneos e impide la liberación de histamina y el desarrollo de habones. Se desconoce el motivo por el cual el efecto se mantiene en el tiempo. Es un tratamiento de elevado coste económico y con una morbilidad importante. No existen estudios controlados.
PlasmaféresisLa plasmaféresis es una técnica de depuración extracorpórea que consiste en la separación del plasma y los elementos de la sangre con el fin de eliminar aquellos patógenos causantes de la enfermedad que, en el caso de la UC, corresponderían a los autoanticuerpos liberadores de histamina. Se ha usado en casos de UC resistente a tratamiento50, aunque no existen ensayos clínicos controlados. Es una terapia cara con una potencial morbilidad y las recurrencias son frecuentes. La plasmaféresis en monoterapia no es suficiente para prevenir la reacumulación de autoanticuerpos liberadores de histamina y debe utilizarse en combinación con fármacos inmunosupresores.
OmalizumabEl omalizumab es un anticuerpo monoclonal recombinante humanizado que se une específicamente al dominio C3¿ de la cadena pesada de IgE, el lugar de unión al receptor de alta afinidad de IgE en la superficie de mastocitos y basófilos. Actualmente solo está autorizado para su uso en el asma bronquial de tipo alérgico severa51.
Existen 2 tipos de receptores para IgE52: el FC¿RI presente en los mastocitos, los basófilos, los monocitos, los eosinófilos y las células de Langerhans, y los receptores de baja afinidad (FC¿RII/CD23), implicados en funciones de presentación del antígeno (FC¿RII de linfocitos B) y en la regulación de la síntesis de IgE. Omalizumab disminuye los niveles de IgE libre circulante y secundariamente disminuye la densidad de receptores de IgE en basófilos y mastocitos cutáneos previniendo su activación y degranulación por autoanticuerpos. La IgE puede modular el grado de expresión de sus propios receptores de alta y baja afinidad. La ocupación por IgE del FC¿RI de los mastocitos y basófilos determina los niveles de expresión del receptor en superficie de manera que a mayor concentración de IgE, aumenta la densidad de sus receptores y la reactividad de los mastocitos y basófilos, que disminuyen con la reducción de sus concentraciones. Cuando se une IgE al FC¿RI se forma una interacción entre el dominio C3 de IgE y la cadena alfa del receptor de alta afinidad52–57. El omalizumab podría actuar también reduciendo el número de autoanticuerpos IgE antitiroperoxidasa e inhibir la degranulación del mastocito al disminuir la densidad de receptores de IgE en su superficie (feedback negativo)57.
Se ha observado que el omalizumab no solo es eficaz en el tratamiento de la UCA, sino que también puede tener su papel en la urticaria crónica idiopática (ASST negativa y ausencia de liberación de histamina por basófilo in vitro). Este efecto podría explicarse por una acción directa sobre mastocitos, eosinófilos o basófilos, incluso en ausencia de autoanticuerpos. Otra posible explicación es que pudiera prevenir la secreción de citocinas y quimiocinas dependientes de FC¿RI por algún estimulo aun desconocido. Se ha observado buena respuesta en urticarias físicas: urticaria solar, urticaria por calor, a frigore, urticaria por presión retardada y urticaria colinérgica, aunque se trata de casos aislados y se precisan un mayor número de estudios sobre su potencial eficacia58–63.
En el tratamiento del asma alérgica grave se administra en forma de inyección subcutánea a una dosis que oscila entre 75 y 375mg dependiendo del peso corporal y los niveles de IgE en sangre. En un estudio reciente de Saini et al.64, se observó que en la UC idiopática, una dosis única de omalizumab de 300 o 600mg, a la semana 4 de tratamiento conseguía una franca mejoría del UAS7 respecto al nivel basal y que era más eficaz que el placebo con unos efectos de inicio rápido (primera semana). Sin embargo, con dosis de 75mg no se observaron diferencias estadísticamente significativas respecto el placebo. Teniendo en cuenta que para el tratamiento del asma alérgica es necesario esperar hasta 16 semanas para observar una respuesta, se ha propuesto que el omalizumab podría tener un efecto directo sobre los mastocitos y no solo sobre la IgE.
En varios estudios se ha objetivado que omalizumab consigue disminuir el urticaria activity score (UAS), y la necesidad de tomar medicación de rescate, aumenta la respuesta terapéutica y mejora la calidad de vida de los pacientes con UC52. Los efectos adversos descritos son mayoritariamente leves (rinofaringitis, diarrea, cefalea, sintomatología local en zona de inyección) aunque en algún caso pueden ser más graves (anafilaxia).
Otros tratamientosNifedipinoLos resultados sobre su utilidad en el tratamiento de la urticaria son contradictorios. Se ha observado su eficacia en la disminución del prurito y en la formación de habones en pacientes con UC cuando se combinan con antihistamínicos a dosis altas65. No obstante, en otros trabajos los efectos del nifedipino sobre la UC han sido poco significativos11. El nifedipino actuaría modificando la entrada de calcio a los mastocitos cutáneos. Puede ser un fármaco a considerar en pacientes con hipertensión arterial, sobre todo en aquellos que toman IECA para controlarla.
Anticoagulación/antifibrinolíticoSe ha visto que en algunos pacientes con UC existe un aumento de la trombina debido a la activación de la cascada de la coagulación por la vía extrínseca y también signos de fibrinólisis con niveles de dímero D aumentados en plasma. Estos serían casos de UC más severas y con peor respuesta al tratamiento de primera línea con antihistamínicos66–69. Se ha propuesto que la trombina podría incrementar la permeabilidad vascular, activando la degranulación de los mastocitos y la cascada del complemento en ausencia de C3. La activación de la cascada de coagulación en estos pacientes se asocia a una pobre respuesta a tratamiento con antihistamínicos a dosis licenciadas. El dímero D podría servir como marcador para discernir este grupo de pacientes con UC idiopática. En estos pacientes, el tratamiento combinado con anticoagulante (heparina) y antifibrinolítico (ácido tranexámico) podría ser de utilidad, ya que se trata de un subgrupo de pacientes en los que estaremos bloqueando un mecanismo de activación de la inflamación70.
DapsonaLa dapsona (4-49-diaminodifenilsulfona) es un derivado de la sulfona que posee efectos antimicrobianos y antiinflamatorios y se ha usado durante muchos años para tratar una gran variedad de enfermedades cutáneas con infiltrado dérmico neutrofílico como la urticaria vasculitis, la enfermedad de Behçet, el pioderma gangrenoso, etc. En el tratamiento de la urticaria, la dapsona sola o combinada con otros tratamientos se considera una alternativa terapéutica. En algunos artículos anecdóticamente se ha visto mejoría de la UC idiopática y la urticaria por presión retardada71.
ColchicinaLa colchicina se ha utilizado ampliamente en el tratamiento de un heterogéneo grupo de enfermedades cutáneas habitualmente caracterizadas por la presencia de infiltrados neutrofílicos dérmicos como la psoriasis, la vasculitis leucocitoclástica y la urticaria vasculitis. La colchicina limita la actividad quimiotáctica y fagocítica de los neutrófilos polimorfonucleares y suprime la función leucocitaria incrementando los niveles de adenosina monofosfato cíclico citoplasmático e inhibiendo la degranulación de los lisosomas72,73. El aumento de los niveles de adenosina monofosfato cíclico libera prostaglandina E la cual suprime la función leucocitaria. Oka et al.74 demostraron que la colchicina es un despolimerizador de microtúbulos crucial para la degranulación de los mastocitos. Los efectos inhibidores de la colchicina en la urticaria podrían ser debidos a un efecto dual: un bloqueo de la quimiotaxis de los neutrófilos y una reducción de la degranulación de los mastocitos. Puntualmente ha sido utilizada en algunos pacientes con urticaria vasculitis.
SulfasalazinaEste fármaco que pertenece al grupo de los antifolatos se ha utilizado durante muchos años para el tratamiento de enfermedades inflamatorias del intestino y de la artritis reumatoide. Sus principales efectos secundarios son la hepatotoxicidad, neurotoxicidad y mielotoxicidad. Se desconoce su mecanismo de acción en la UC. Puede afectar a la liberación de histamina mediada por IgE y da lugar a una reducción de la actividad de la prostaglandina-sintetasa. Podría ser útil como fármaco ahorrador de corticosteroides75. Existen pocos estudios controlados sobre su uso en la UC.
HidroxicloroquinaSe ha utilizado en el tratamiento del síndrome urticaria vasculitis hipocomplementémica76.
Recomendaciones de las guías europeasEl manejo y tratamiento de los pacientes con UC es complejo. Por este motivo se han diseñado guías de consenso en el manejo de esta entidad basadas tanto en evidencias científicas como en la opinión de expertos. Las 2 guías existentes para el manejo de la urticaria crónica, son la «BSACI guidelines for the management of chronic urticaria and angio-oedema» realizada por la «British Society for Allergy and Clinical Immunology»2 (BSACI) y publicada en Clinical and Experimental Allergy en 2007, y las guías Europeas del EAACI/GA2LEN/EDF/WAO publicadas en Allergy en 200910. Estas últimas son el resultado del consenso alcanzado en el panel de discusión de la 3.a Reunión de Consenso Internacional en Urticaria en el año 2008 por la «Dermatology Section of the European Academy of Allergology and Clinical Immunology» (EAACI), la «Global Allergy and Asthma European Network» (GA2LEN), el «European Dermatology Forum» (EDF) y la «World Allergy Organization» (WAO).
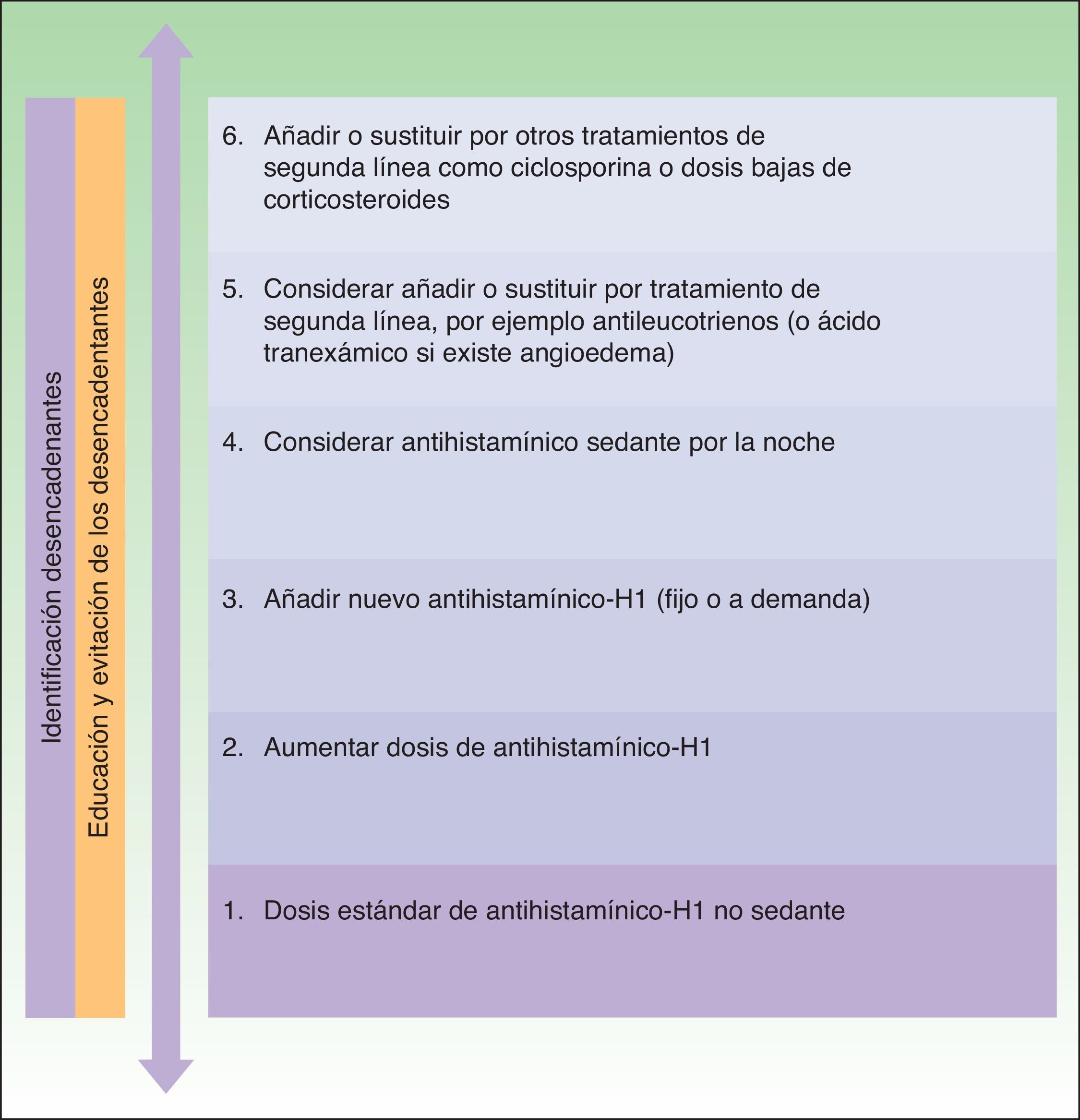
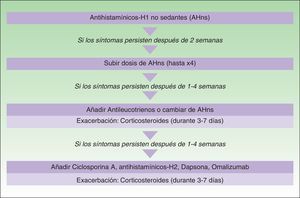
La principal diferencia entre ambas guías en cuanto al algoritmo de tratamiento de la urticaria crónica reside en que en la guía británica se sigue recomendando el uso de antihistamínicos sedantes por la noche si no han sido eficaces los antihistamínicos no sedantes incluso a dosis mayores, mientras que en las europeas no se recomiendan en ningún caso2,10 (figs. 1 y 2).
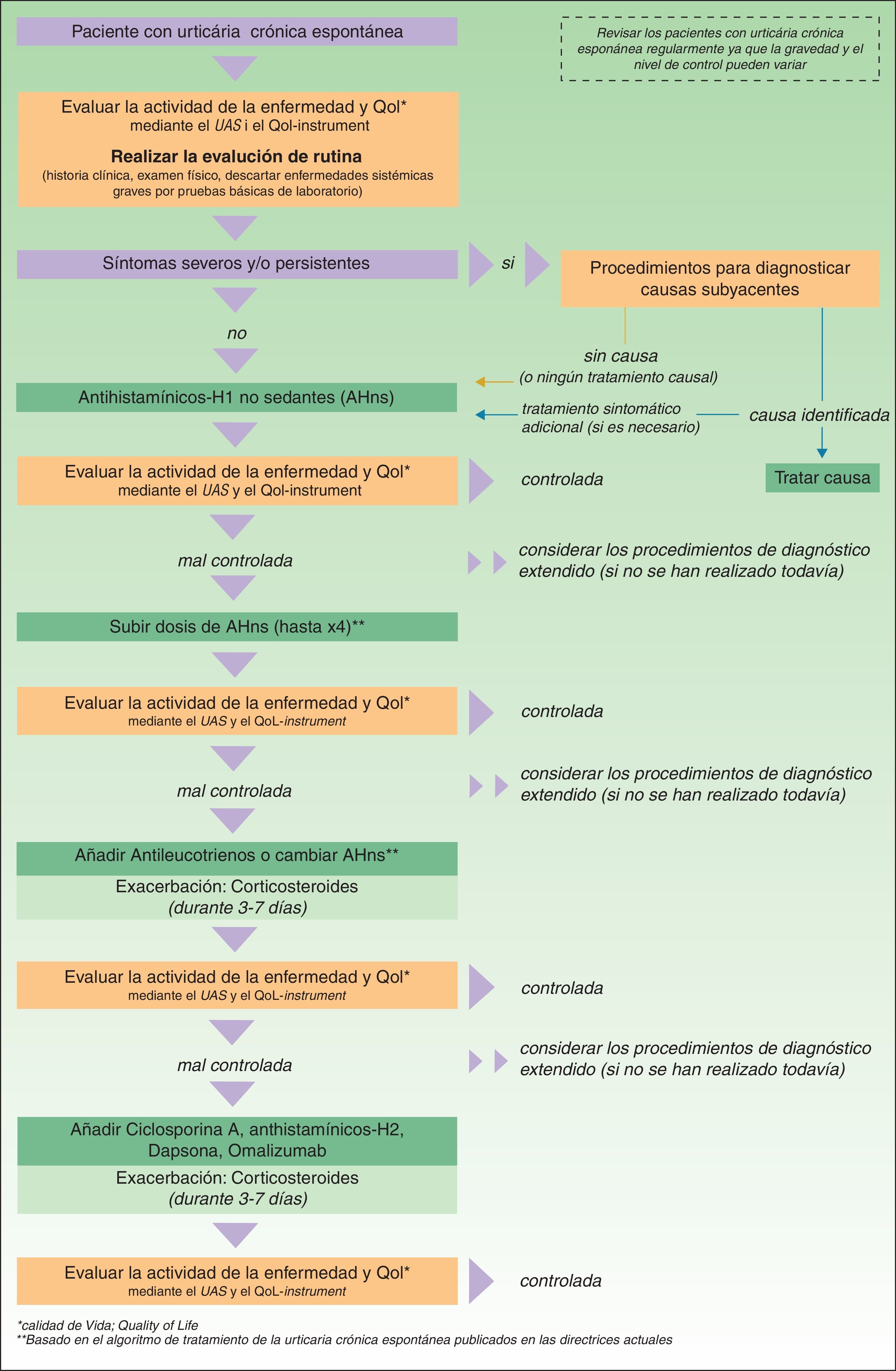
Algoritmo de tratamiento de la urticaria crónica espontánea según las guías europeas de la EAACI/GA2LEN/EDF/WAO de 2009. Reproducida con el permiso de los autores. En la actualización consensuada de 2012 se ha retirado la recomendación del empleo de dapsona así como de los antihistamínicos H2. Se recomienda el aumento de la dosis de los antihistamínicos H1 no sedantes hasta 4 veces la dosis licenciada y se mantiene como segunda línea de tratamiento exclusivamente el empleo de omalizumab, ciclosporina A o antileucotrienos.
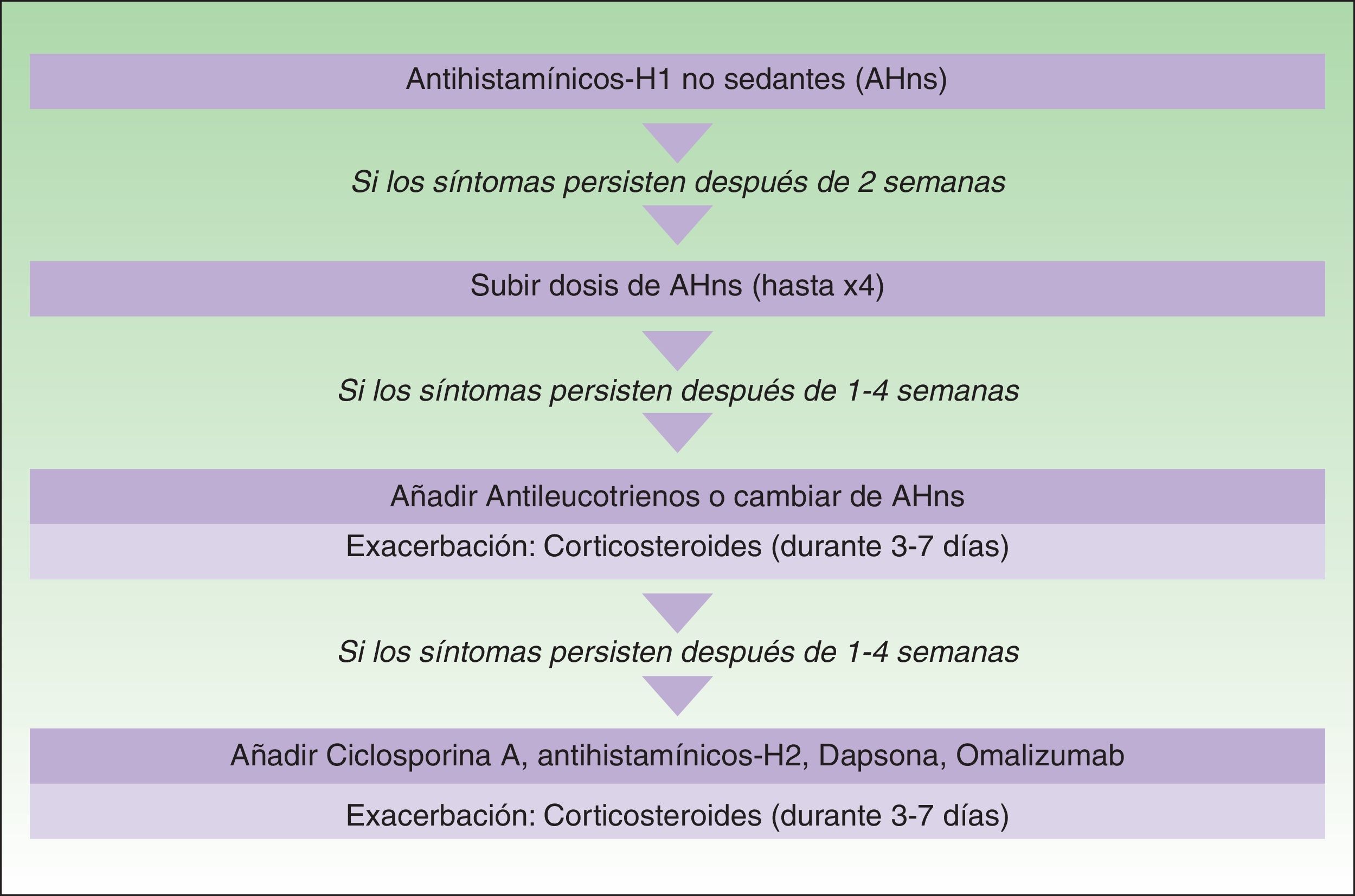
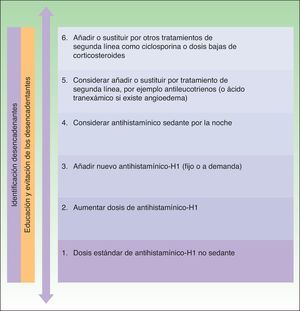
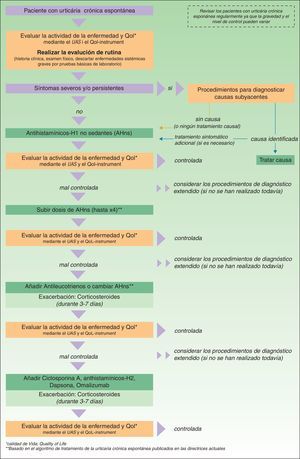
En la cuarta reunión de consenso para la actualización de las guías de la urticaria crónica espontánea realizada el mes de noviembre de 2012 en Berlín, se introdujeron algunos cambios en el algoritmo de manejo de la urticaria crónica. Dado que en el algoritmo sólo se incluyen aquellas opciones terapéuticas avaladas con un grado de recomendación fuerte se retiró del mismo el empleo de dapsona así como de los antihistamínicos-H2. Ante el fracaso del empleo de antihistamínicos-H1 no sedantes a dosis licenciadas se recomienda su aumento hasta un máximo de cuatro veces dicha dosis. Se mantienen como segunda línea de tratamiento el empleo de omalizumab, ciclosporina A o antileucotrienos. Estos fármacos se añaden al empleo de los antihistamínicos-H1. Se recomienda, sin embargo, leer la guía por completo puesto que la no aparición en el algoritmo de otras opciones terapéuticas no las invalida para pacientes concretos (fig. 3).
Algoritmo para el manejo de los pacientes con urticaria crónica espontánea. Reproducido de Maurer et al.5 con permiso de los autores.
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran que no tienen conflicto de intereses