La necrólisis epidérmica tóxica (NET) forma parte, junto con el síndrome de Stevens-Johnson (SSJ), de un espectro de urgencias médicas caracterizadas por el despegamiento epidérmico y el riesgo de una inestabilidad hemodinámica y de una sepsis1. Presenta una mortalidad aproximada del 35% y, aunque en niños la supervivencia es mayor, se ha relacionado con unas tasas mayores de complicaciones a largo plazo2. En la mayoría de las ocasiones, la NET es secundaria a una reacción a fármacos de tipo idiosincrásico, entre los que destacan los anticonvulsivantes, los antibióticos y los antiinflamatorios no esteroideos como desencadenantes más frecuentes. No existen unas guías de actuación estandarizadas y, clásicamente, se han utilizado tanto la corticoterapia sistémica como las inmunoglobulinas intravenosas (IGIV), con unos resultados discutibles. Recientemente, se han probado nuevas opciones terapéuticas, incluidos los inmunosupresores clásicos como ciclosporina y fármacos anti-TNF-α. Consideramos de interés, dadas las escasas referencias bibliográficas actuales, la descripción de un nuevo caso de NET infantil tratada de forma satisfactoria con ciclosporina.
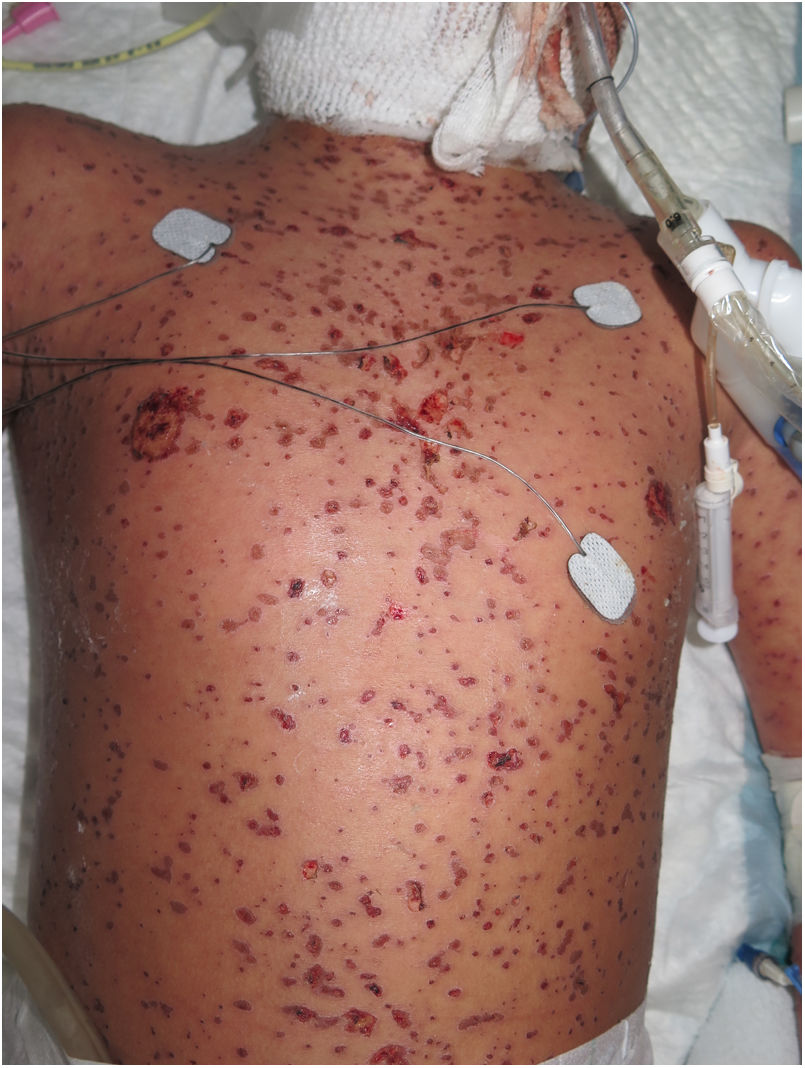
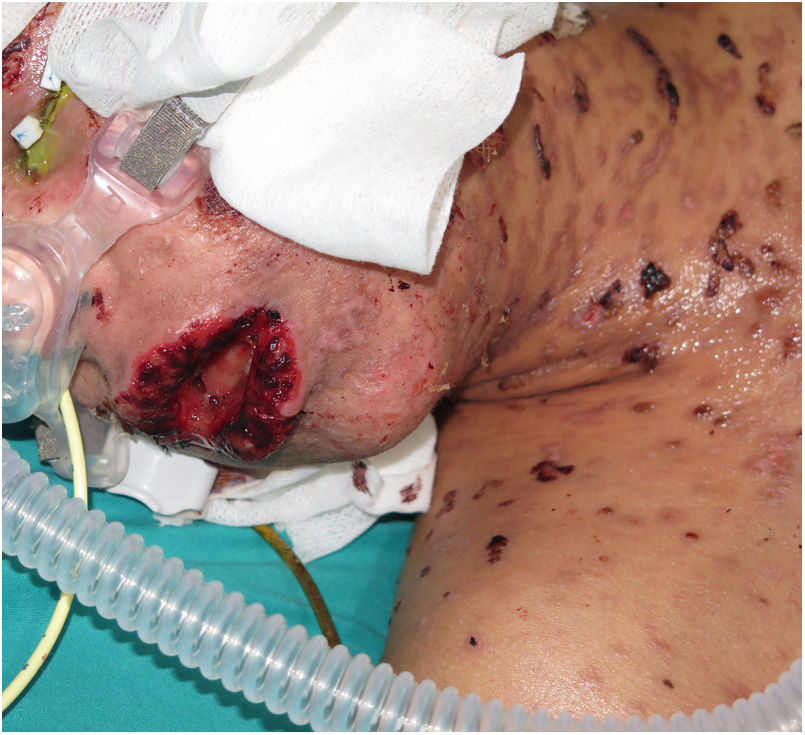
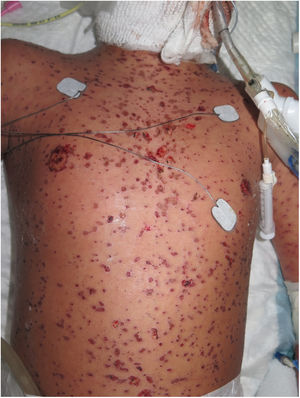
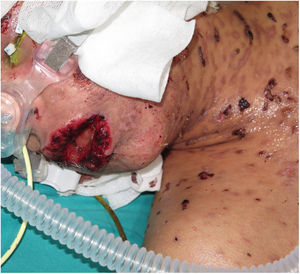
Un niño de 10 años, con antecedentes de epilepsia multifocal en tratamiento con lamotrigina, a las 3semanas del inicio del tratamiento antiepiléptico, inició con una fiebre de 39°C, unas ampollas en la cara, el tronco y las extremidades y con unas áreas de piel denudada, con el signo de Nikolsky positivo, que, en conjunto, abarcaban aproximadamente el 40% de la superficie corporal total y asociaban una afectación importante de las mucosas ocular, oral y genital (figs. 1 y 2). Ante la sospecha de una NET, se suspendió de forma inmediata la lamotrigina y se inició el tratamiento con corticoides sistémicos (1-2mg /kg/día). Sin embargo, el cuadro cutáneo siguió progresando, añadiéndose inestabilidad hemodinámica subsidiaria de soporte vasoactivo y respiratorio. En la Unidad de Cuidados Intensivos Pediátricos de nuestro hospital se instauró el tratamiento con ciclosporina por vía intravenosa a dosis de 4mg/kg/día. Al cuarto día del tratamiento se comenzó a objetivar una detención en la progresión de la enfermedad, sin nuevas lesiones activas ni áreas denudadas. Coincidiendo con una reepitelización parcial de todas las lesiones, 6días después (día 10 de tratamiento), se comenzó a descender la dosis de ciclosporina progresivamente sin nuevos datos de actividad de la enfermedad.
En el tratamiento de los pacientes con una NET, las medidas prioritarias se basan en la suspensión de aquellos fármacos sospechosos y garantizar un tratamiento de soporte hidroelectrolítico, nutricional y respiratorio. Debido a la ausencia de estudios aleatorizados, no existe una evidencia suficiente sobre la eficacia de los diferentes tratamientos en la población pediátrica aquejada de una NET3. La literatura disponible hasta la fecha es escasa y los trabajos publicados se centran en el debate sobre el uso de corticoides e IGIV, la mayoría en la población adulta. Existen varios autores que sostienen que existe una mayor supervivencia y rapidez en la reepitelización en los pacientes tratados con corticoides o IGIV frente a los que reciben exclusivamente un tratamiento de soporte. Sin embargo, estos resultados contrastan con otros estudios en los que se ha objetivado un aumento de la morbilidad con el uso de los mismos. Recientemente, se han publicado varios trabajos de SJS/NET en adultos tratados de forma satisfactoria con ciclosporina (3-5mg/kg/día, por un mínimo de 14 días), donde se muestra que los resultados parecen ser superiores al uso de IGIV en términos de supervivencia, de la rapidez de reepitelización y de una reducción de la estancia hospitalaria4,5.
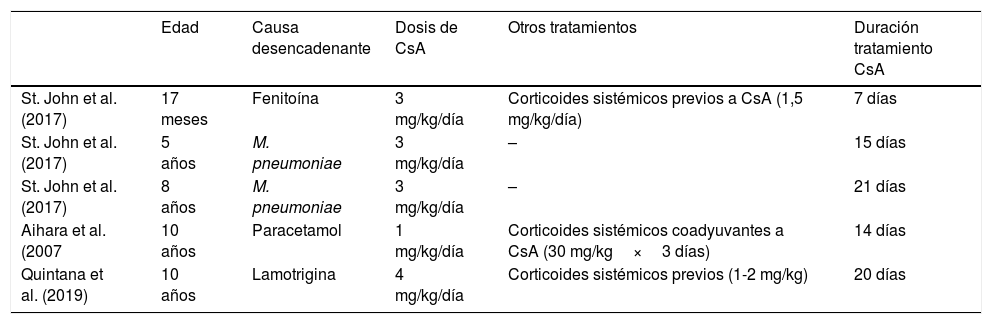
Hasta la fecha, solamente se han publicado 4pacientes en edad pediátrica con SSJ/NET tratados con ciclosporina6,7 (tabla 1). Todos ellos muestran su utilidad en la estabilización de la enfermedad, reepitelización de las lesiones y disminución de la mortalidad en comparación con el tratamiento de soporte. Uno de los hallazgos más llamativos, descrito de forma constante en la literatura, es la rapidez del fármaco en interrumpir la progresión de la enfermedad, con un tiempo de respuesta que varía entre horas hasta un máximo de 3 días desde el inicio del tratamiento, independientemente del retraso desde el inicio de la enfermedad hasta el ingreso hospitalario1,4,6,8.
Características clínicas de pacientes pediátricos tratados con ciclosporina
| Edad | Causa desencadenante | Dosis de CsA | Otros tratamientos | Duración tratamiento CsA | |
|---|---|---|---|---|---|
| St. John et al. (2017) | 17 meses | Fenitoína | 3 mg/kg/día | Corticoides sistémicos previos a CsA (1,5 mg/kg/día) | 7 días |
| St. John et al. (2017) | 5 años | M. pneumoniae | 3 mg/kg/día | – | 15 días |
| St. John et al. (2017) | 8 años | M. pneumoniae | 3 mg/kg/día | – | 21 días |
| Aihara et al. (2007 | 10 años | Paracetamol | 1 mg/kg/día | Corticoides sistémicos coadyuvantes a CsA (30 mg/kg×3 días) | 14 días |
| Quintana et al. (2019) | 10 años | Lamotrigina | 4 mg/kg/día | Corticoides sistémicos previos (1-2 mg/kg) | 20 días |
Por otro lado, y basándose en los resultados demostrados en población adulta9,10, se ha descrito solo un caso de un paciente pediátrico con SSJ tratado con etanercept (2 dosis de 25mg subcutáneas), mostrando resultados comparables a la ciclosporina en términos de reepitelización y detención de la progresión de la enfermedad11. Este fármaco parece ser de especial utilidad en los casos con una insuficiencia renal o con antecedentes de malignidad, situaciones en las que la ciclosporina está contraindicada4,6,11.
El caso descrito apoya los resultados obtenidos en los otros 4pacientes pediátricos publicados previamente y aporta una evidencia adicional sobre el uso de ciclosporina en monoterapia en pacientes con SSJ/NET. La ciclosporina puede ser considerada una buena opción terapéutica con un perfil de seguridad razonable en una situación como esta, que puede comprometer gravemente la vida del paciente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.